Clear Sky Science · es
Síntesis química de nuevos derivados aminopirimidin-4-il-1H-pirazol como inhibidores de la tirosina quinasas esplénicas (SYK)
Por qué bloquear una sola enzima podría ayudar a combatir el cáncer y la inflamación
Nuestro sistema inmunitario depende de una mensajería interna rápida para indicar a las células cuándo atacar a los invasores y cuándo detenerse. Cuando esas señales fallan, pueden alimentar enfermedades autoinmunes y el cáncer. Este estudio explora una vía prometedora para silenciar esas señales defectuosas mediante el diseño de pequeñas moléculas con carácter farmacológico que bloquean selectivamente una enzima clave, la tirosina quinasa esplénica (SYK), que se encuentra en el centro de muchas reacciones inmunitarias.
Un interruptor de señal en el núcleo de muchas enfermedades
SYK actúa como un interruptor maestro dentro de ciertas células inmunitarias. Cuando se activa, contribuye a impulsar la inflamación, la producción de anticuerpos y el crecimiento celular. En contextos sanos esto es útil para combatir infecciones. Pero en condiciones como la artritis reumatoide, el asma y varios cánceres hematológicos y de órgano sólido, la actividad de SYK puede volverse excesiva, manteniendo a las células inmunitarias activadas y favoreciendo la supervivencia tumoral. Debido a este papel central, investigadores de todo el mundo intentan desarrollar fármacos que bloqueen SYK que sean lo bastante potentes para ser eficaces, pero lo bastante precisos para no afectar muchas otras quinasas y provocar efectos secundarios.
Construyendo una familia de pequeñas moléculas a medida
Los autores crearon una nueva serie de moléculas relacionadas basadas en un andamiaje químico común denominado aminopirimidin-4-il-1H-pirazol. A partir de bloques de construcción sencillos, ensamblaron estas piezas paso a paso y luego modificaron una porción de la estructura para producir nueve candidatos finales. Cada molécula se verificó cuidadosamente mediante métodos analíticos estándar para confirmar que su estructura y pureza eran las previstas. Este enfoque modular permitió al equipo sondear cómo afectan al interacción con SYK los cambios sutiles en forma y flexibilidad.
Observando cómo los compuestos se aferran a su objetivo
Antes de ir al banco de laboratorio, los investigadores utilizaron simulaciones por ordenador para ver con qué fuerza podría unirse cada molécula a SYK. Los cálculos de acoplamiento estimaron cuánto encajaban los compuestos en el bolsillo de unión de la enzima, destacando un candidato, etiquetado como 44, como especialmente prometedor. Simulaciones más detalladas de dinámica molecular, en las que el complejo proteína‑fármaco se sigue durante cientos de nanosegundos, mostraron que el 44 forma una asociación particularmente estable con SYK. La proteína permaneció compacta, los contactos clave se mantuvieron y el sistema se asentó en una única conformación de baja energía con múltiples enlaces de hidrógeno fuertes, especialmente con aminoácidos como triptófano y serina que ayudan a acunar la molécula.
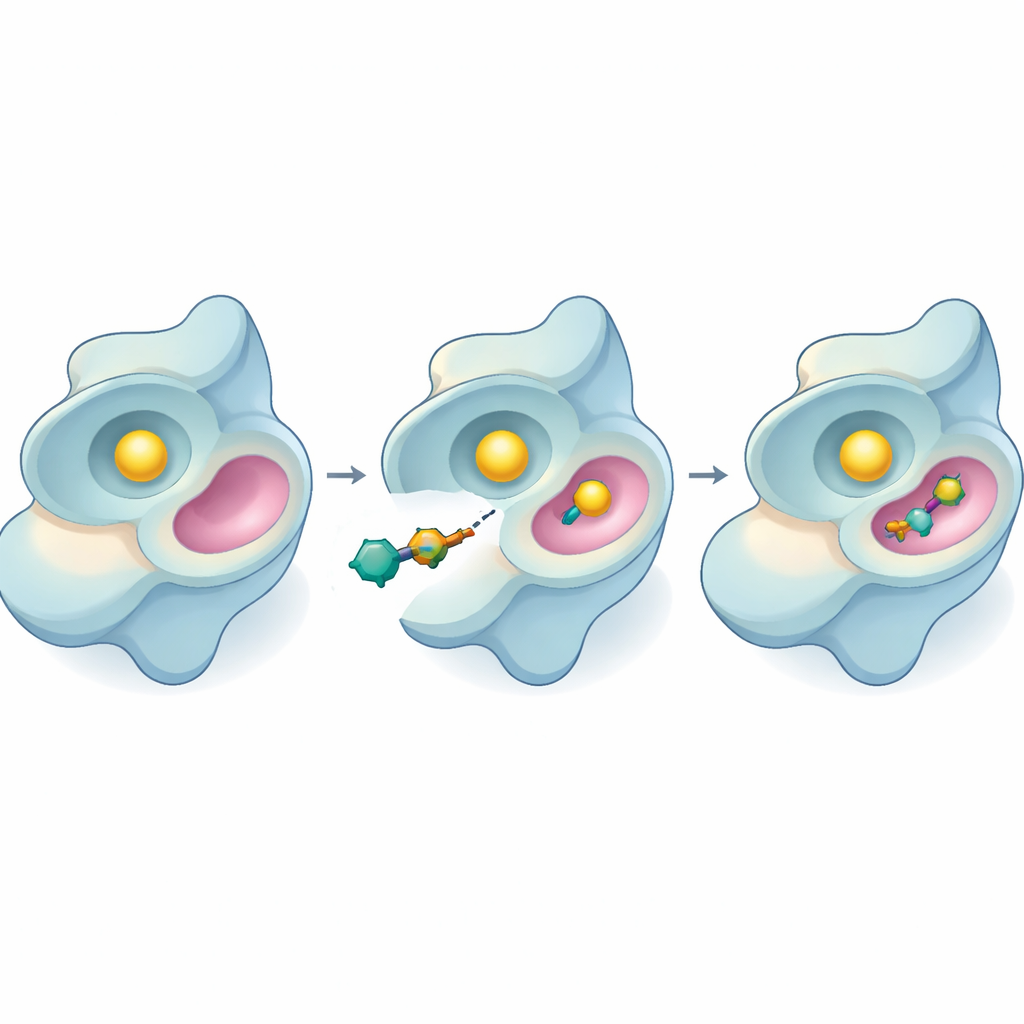
Poniendo a prueba los nuevos inhibidores
El equipo pasó entonces a experimentos de laboratorio utilizando un ensayo basado en luz que mide la actividad de SYK al consumir su molécula combustible, el ATP. Varios de los nuevos compuestos ralentizaron la enzima, pero el 44 volvió a destacarse. Inhibió SYK a concentraciones muy bajas y se mostró más eficaz cuanto más tiempo permanecía unido a la enzima. Al variar la cantidad de sustrato presente, los investigadores pudieron inferir el modo de acción de 44: en lugar de competir directamente con el ATP en el sitio activo principal, parece unirse en un sitio distinto, alostérico, y modificar el comportamiento de la enzima a distancia. Esto es importante porque los inhibidores alostéricos a menudo mantienen su efecto incluso cuando los niveles de ATP son altos o cuando mutaciones alteran el sitio primario.
Qué podría significar esto para tratamientos futuros
En conjunto, los modelos por ordenador y las mediciones de laboratorio dibujan un panorama consistente: la molécula 44 se une fuertemente a SYK, mantiene la enzima en un estado estable y menos flexible, y apaga su actividad mediante un mecanismo indirecto y no competitivo. Para quienes no son especialistas, esto significa que los investigadores han identificado una llave química finamente ajustada que encaja en una cerradura crítica para muchas enfermedades impulsadas por el sistema inmunitario, sin limitarse a bloquear simplemente la apertura principal. Aunque queda mucho trabajo por delante —especialmente pruebas en células, animales y paneles más amplios de quinasas relacionadas—, este andamiaje ofrece un punto de partida prometedor para futuros fármacos destinados a domar la inflamación nociva y frenar ciertos cánceres mediante la diana SYK.
Cita: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
Palabras clave: tirosina quinasa esplénica, inhibidores de quinasas, terapéuticas contra el cáncer, enfermedad autoinmune, fármacos alostéricos