Clear Sky Science · es
ConvAHKG: grafo de conocimiento híbrido basado en acciones con un enfoque convolucional de doble canal para reposicionamiento de fármacos
Encontrar nuevos usos para medicamentos antiguos
Llevar un fármaco completamente nuevo al mercado puede llevar más de una década y costar miles de millones de dólares, y muchos candidatos fracasan en el camino. Este estudio explora un atajo más inteligente: usar datos e inteligencia artificial para descubrir nuevas enfermedades que fármacos ya aprobados podrían tratar de forma segura. Los autores presentan un marco, llamado ConvAHKG, que entrelaza muchos tipos de información biomédica en un único mapa conectado y luego utiliza una red neuronal moderna para detectar emparejamientos prometedores entre fármacos y enfermedades, ofreciendo una vía más rápida y económica hacia nuevas terapias.
Un mapa rico de cómo interactúan fármacos y enfermedades
El núcleo de este trabajo es un “grafo de conocimiento híbrido”, un mapa gigante que conecta fármacos, enfermedades, proteínas, efectos secundarios, estructuras químicas y vías biológicas. En lugar de almacenar solo enlaces sencillos de sí/no (por ejemplo, “el fármaco A trata la enfermedad B”), el mapa registra cómo actúa un fármaco sobre una proteína—si la activa, la inhibe o se une a ella—y cómo las proteínas participan en enfermedades, por ejemplo como biomarcadores o por cambios en su actividad. El grafo contiene más de 11.000 entidades y 59 tipos de relaciones, incluida información detallada sobre clasificaciones de fármacos, efectos secundarios, contactos proteína–proteína y subestructuras químicas. Al capturar estas múltiples capas de contexto, el grafo puede reflejar más de la compleja biología real detrás de los efectos terapéuticos y las reacciones adversas. 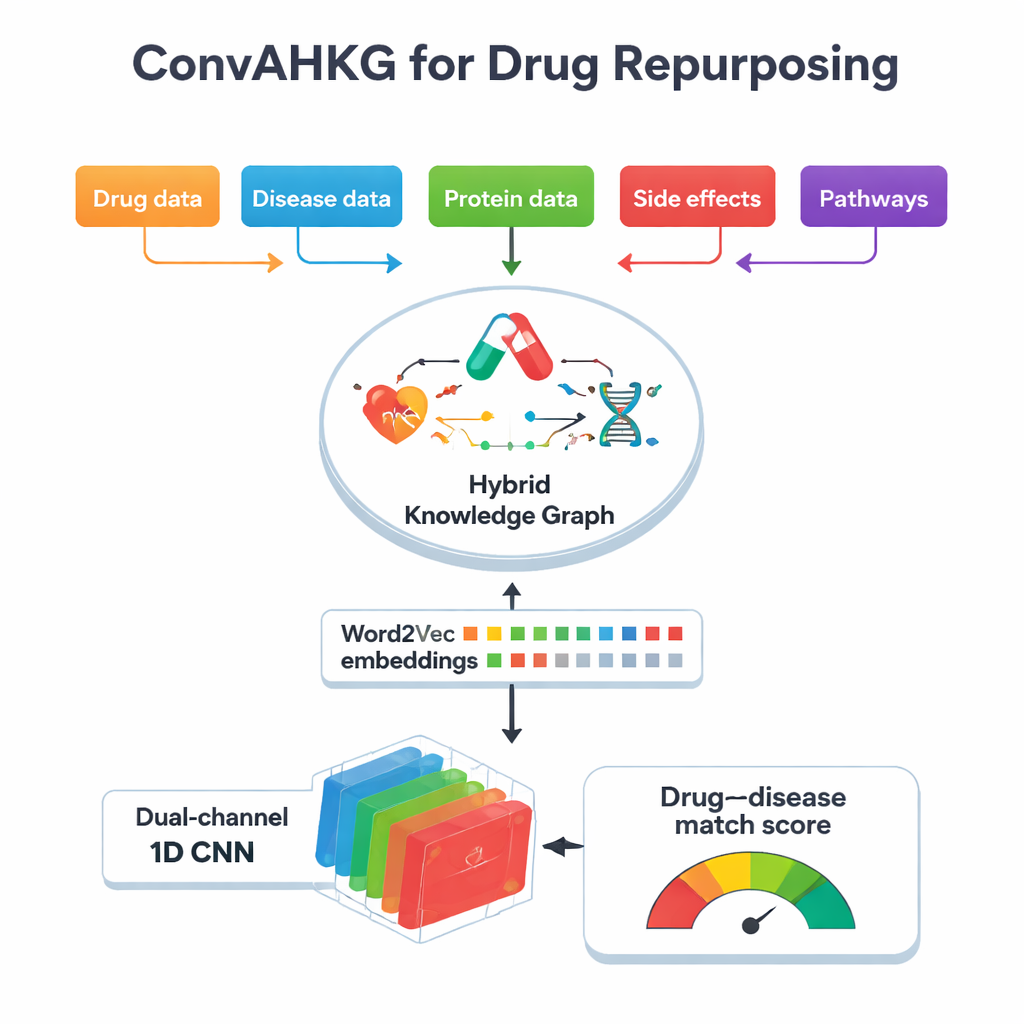
Enseñar al ordenador el lenguaje de la biología
Para hacer este mapa complejo utilizable por el aprendizaje automático, el equipo convierte cada conexión del grafo en una simple “frase” de tres partes: una cabeza (por ejemplo una enfermedad), una relación (por ejemplo biomarcador) y una cola (por ejemplo una proteína). Luego aplican Word2Vec, un método desarrollado originalmente para el procesamiento del lenguaje natural, para aprender “embeddings” numéricos de cada fármaco, enfermedad y proteína. Los elementos que suelen aparecer juntos en estas frases acaban cerca unos de otros en este espacio matemático, de forma similar a las palabras que comparten significados en textos. Este enfoque es mucho más simple y rápido que muchas técnicas de incrustación específicas para grafos, y aun así captura patrones sutiles. En pruebas frente a varios métodos populares de incrustación de grafos, Word2Vec igualó o superó su poder predictivo mientras usaba mucho menos tiempo de cómputo.
Una vía neuronal dual para decisiones de tratamiento sí/no
Una vez que cada fármaco y enfermedad se traduce en un vector numérico, ConvAHKG los introduce en una red neuronal convolucional unidimensional de dos canales. Un canal procesa el vector del fármaco y el otro procesa el vector de la enfermedad mediante una secuencia de filtros convolucionales que detectan patrones locales y motivos más amplios, inspirados en diseños de reconocimiento de imágenes como InceptionNet y AlexNet. Tras este procesamiento por separado, las dos corrientes se fusionan y pasan por varias capas completamente conectadas que producen una única probabilidad: ¿representa esta pareja fármaco–enfermedad un tratamiento efectivo probable, o más bien un efecto secundario dañino? Para manejar el hecho de que los pares positivos conocidos son mucho más raros que los negativos, los autores introducen una función de pérdida ponderada que penaliza con mayor severidad los tratamientos verdaderos perdidos, mejorando el rendimiento en estos casos difíciles de encontrar. 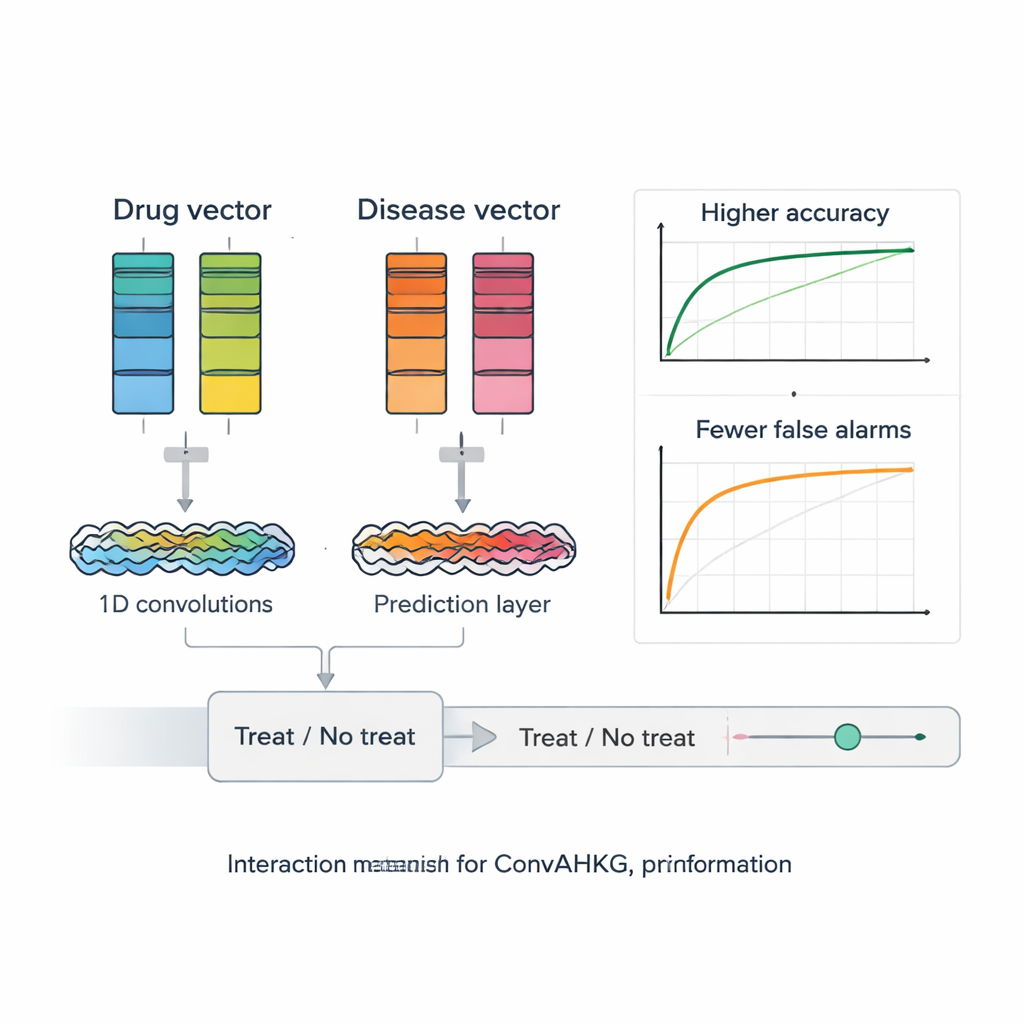
Superando métodos existentes y detectando candidatos para cáncer
Los investigadores prueban rigurosamente su marco frente a varias herramientas de reposicionamiento de fármacos de última generación que usan factorización de matrices, redes neuronales de grafos y autoencoders profundos. ConvAHKG alcanza un área bajo la curva ROC de 0,9836 y un área bajo la curva precisión–recuperación de 0,9686, superando a todos los enfoques competidores en el mismo conjunto de referencia. Luego aplican el modelo al cáncer de pulmón no microcítico, la forma más común y letal de cáncer de pulmón en todo el mundo. ConvAHKG destaca varios fármacos no etiquetados previamente como tratamientos para esta enfermedad, incluida la anticuerpo trastuzumab, que se dirige a la proteína HER2 y ya cuenta con evidencia clínica de apoyo en cáncer de pulmón, así como otros agentes biológicos e incluso el clásico antibiótico bencilpenicilina. Simulaciones de docking sugieren que la bencilpenicilina puede unirse fuertemente al ADN y a la topoisomerasa II alfa, una enzima a menudo elevada en estos tumores, insinuando un posible mecanismo anticancerígeno que ahora merece pruebas en laboratorio.
Por qué esto importa para los pacientes
En términos sencillos, ConvAHKG actúa como un emparejador muy bien informado entre fármacos existentes y enfermedades, usando un mapa detallado de acciones biológicas y un potente motor de reconocimiento de patrones para predecir qué medicamentos antiguos podrían funcionar en contextos nuevos. Tratando a los fármacos ya evaluados en seguridad como bloques reutilizables en lugar de herramientas de un solo uso, este marco podría acelerar el descubrimiento de terapias para afecciones como el cáncer de pulmón, especialmente donde el desarrollo convencional de fármacos es demasiado lento o costoso. Aunque las predicciones aún requieren validación experimental y clínica cuidadosa, el estudio muestra que combinar conocimiento biológico rico con IA moderna puede reducir drásticamente el espacio de búsqueda, acercando tratamientos potencialmente salvavidas con mayor rapidez.
Cita: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
Palabras clave: reposicionamiento de fármacos, grafo de conocimiento, aprendizaje profundo, cáncer de pulmón, descubrimiento de fármacos