Clear Sky Science · es
Transferencia de protones inducida por luz en agua de distintas estructuras: un enfoque EPR para resolver un problema clásico
Por qué importan los viajes ocultos de los protones
Cada vez que respiras, piensas o conviertes la luz solar en energía útil en una célula solar, unas partículas diminutas con carga positiva llamadas protones están en movimiento. Cómo viajan estos protones a través del agua es un rompecabezas de siglos de antigüedad, planteado por primera vez por el científico Theodor Grotthuss en 1806. Este nuevo estudio utiliza una combinación ingeniosa de luz y medidas magnéticas para observar protones moviéndose en aguas de distinta estructura, desde soluciones salinas y abarrotadas hasta mezclas vítreas heladas e incluso dentro de una proteína de membrana. El trabajo ofrece una manera novedosa de poner a prueba ideas clásicas sobre el movimiento de protones y de sondear entornos que son difíciles de estudiar por otros métodos.
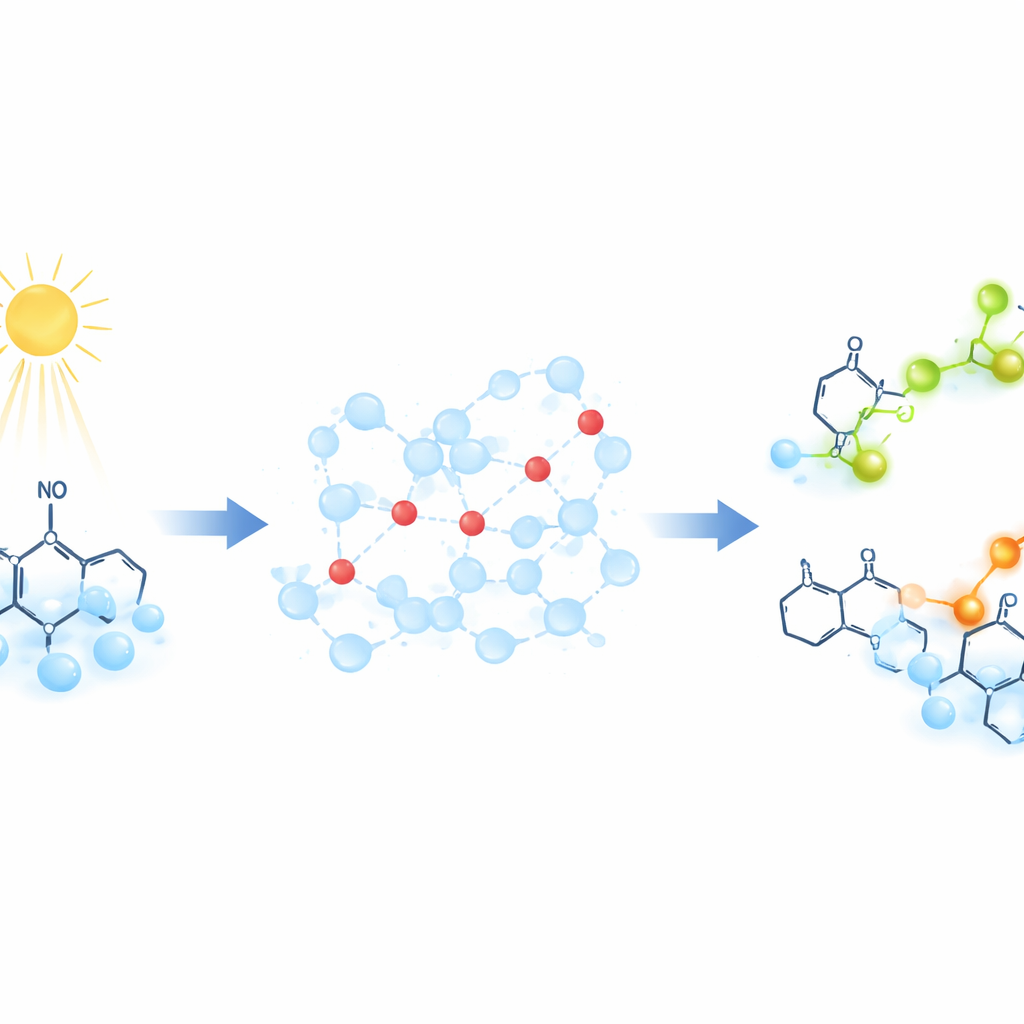
Una nueva forma de observar el movimiento de protones
En lugar de seguir los protones directamente, los investigadores usan moléculas “sonda” especiales que cambian su firma magnética cuando captan un protón. Estas sondas son radicales orgánicos estables cuyo electrón desapareado produce una señal bien definida en la resonancia paramagnética electrónica (EPR), una técnica que detecta cómo responden los electrones desapareados a un campo magnético. Para provocar el movimiento de protones a demanda, el equipo ilumina un compuesto llamado 2‑nitrobenzaldehído. Esta reacción impulsada por la luz libera una ráfaga de protones en menos de una milmillonésima de segundo, bajando repentinamente el pH de la solución. A medida que los protones se extienden por el agua y se unen a las sondas, la señal EPR cambia de forma dependiente del tiempo, permitiendo a los científicos seguir la velocidad de la transferencia de protones.
Cómo los vecinos del agua ralentizan o aceleran el flujo
El agua raramente existe sola; por lo general está llena de sales disueltas u otras moléculas que reorganizan sutilmente su red de enlaces de hidrógeno. El equipo examinó cómo estos aditivos afectan el movimiento de protones comparando agua pura con soluciones que contenían cloruro de potasio, urea o clorhidrato de guanidina, todas a altas concentraciones. Ajustando los cambios en la EPR a modelos cinéticos simples, extrajeron tasas aparentes de transferencia de protones. Encontraron que en 6 molar de clorhidrato de guanidina la transferencia de protones era unas 40 veces más lenta que en agua pura, mientras que 8 molar de urea causó solo una desaceleración moderada, y el cloruro de potasio produjo efectos intermedios. Dado que la tasa a la que los protones reaccionan con las sondas está limitada por cómo se mueven a través de la red de enlaces de hidrógeno, estas diferencias apuntan a cambios sustanciales en cómo se estructura el agua alrededor de los iones y moléculas añadidos.
Movimiento de protones en hielo vítreo y dentro de proteínas
El método no se limita al agua líquida ordinaria. Los autores también estudiaron una mezcla de agua y glicerol enfriada a 160 kelvin, donde forma un vidrio rígido. La difusión libre de moléculas está esencialmente congelada, sin embargo la señal EPR mostró que las sondas seguían siendo protonadas tras la exposición a la luz. Esto sugiere que la transferencia de protones puede proceder sin la difusión clásica, posiblemente mediante tunelamiento cuántico a lo largo de una cadena de enlaces de hidrógeno, remitiendo a refinamientos modernos de la idea de Grotthuss. Para explorar la relevancia biológica, el equipo unió un radical sensible al pH a un sitio específico de la proteína de membrana bacteriorrodopsina, en la frontera entre la proteína y el agua circundante. Cuando desencadenaron la liberación de protones con luz, observaron una respuesta EPR dependiente del tiempo desde este sitio marcado, demostrando que su enfoque puede monitorizar la entrega de protones a una posición definida en la superficie de una proteína.
Conectando estructura, agua y autopistas de protones
Para entender mejor por qué la sonda enlazada a la proteína se comportaba de forma muy similar a una en el agua a granel, los investigadores realizaron simulaciones por ordenador de la bacteriorrodopsina en una membrana y de un péptido pequeño en solución. Calcularon cómo las moléculas de agua rodean el grupo nitroxilo de la etiqueta de espín y encontraron patrones de hidratación local casi idénticos en ambos casos, con solo un apantallamiento leve por el entorno de la membrana. Esto significa que, al menos para el sitio estudiado, los protones tienen acceso a través de una capa de agua que se parece mucho al agua líquida ordinaria. Los autores también muestran que sus sondas pueden utilizarse en experimentos EPR resueltos en el tiempo, abriendo la puerta a rastrear juntos el movimiento de protones y electrones en reacciones donde ambos están estrechamente acoplados.
Lo que nos dice este trabajo en términos sencillos
En esencia, este estudio convierte la luz en una señal de salida nítida para el movimiento de protones y luego usa sondas magnéticas sensibles para observar con qué rapidez esos protones alcanzan distintos objetivos. Al comparar soluciones salinas simples, desnaturalizantes densos, mezclas vítreas y una proteína de membrana, los investigadores demuestran que el flujo de protones está fuertemente condicionado por cómo se disponen las moléculas de agua y por el entorno circundante. Su enfoque no solo apoya la idea de que los protones saltan a lo largo de redes de enlaces de hidrógeno, sino que también revela que este salto puede persistir incluso cuando el movimiento molecular ordinario está casi congelado. Esta nueva caja de herramientas podría ayudar a los científicos a desentrañar cómo se mueven los protones en enzimas, sistemas de conversión de energía y materiales novedosos, acercándonos a controlar a estos portadores de carga diminutos pero potentes.
Cita: Barbon, A., Savitsky, A., Grigoriev, I. et al. Photoinduced proton transfer in differently structured water: an EPR approach to solving a classic problem. Sci Rep 16, 7983 (2026). https://doi.org/10.1038/s41598-026-38650-0
Palabras clave: transferencia de protones, estructura del agua, resonancia paramagnética electrónica, red de enlaces de hidrógeno, bacteriorodopsina