Clear Sky Science · es
Análisis fractal de la vasculatura del carcinoma hepatocelular muestra diferencias regionales independientes de la invasión vascular
Ver el cáncer a través de sus vasos sanguíneos
Los médicos saben que los tumores generan su propia red caótica de vasos sanguíneos y que la disposición de esos vasos puede influir en la eficacia de los tratamientos. En el cáncer de hígado, los fármacos que se dirigen al suministro sanguíneo ya forman parte del tratamiento estándar, pero las medidas actuales en el laboratorio suelen limitarse a contar cuántos vasos hay, no a describir cómo están organizados. Este estudio plantea una pregunta simple pero potente: ¿podemos capturar el “patrón” de los vasos tumorales con solo unos pocos números, y difieren esos patrones entre el tumor, el tejido circundante y el resto del hígado?
Patrones ocultos en redes ramificadas
Los investigadores se centraron en el carcinoma hepatocelular, el cáncer primario de hígado más frecuente. Examinaron muestras de tejido de 29 pacientes cuyos especímenes hepáticos fueron teñidos para que el revestimiento interno de los vasos apareciera marrón al microscopio. En lugar de limitarse a contar vasos, analizaron cómo los vasos llenan colectivamente el espacio, usando herramientas matemáticas aplicadas a menudo a formas naturales complejas como costas o ramas de árboles. Se emplearon dos medidas clave: una que describe cuán “intrincada” es la red vascular y otra que describe cómo se distribuyen los espacios vacíos entre los vasos. Juntas, estas cifras condensan la complejidad visual de la red vascular en una forma que puede compararse entre distintas regiones del hígado.
Convertir imágenes microscópicas en mapas medibles
Para ello, el equipo primero tuvo que separar de manera fiable los vasos del tejido de fondo en grandes preparaciones digitales. Construyeron una tubería automatizada de procesamiento de imágenes que identificó los vasos teñidos de marrón, eliminó ruido y rellenó los interiores de los vasos, produciendo mapas nítidos en blanco y negro de las redes vasculares. Estas segmentaciones automáticas se comprobaron con un experto en patología hepática y mostraron buen acuerdo, especialmente en aspectos relevantes para las medidas globales de organización vascular. A continuación, las laminillas se dividieron en muchos azulejos más pequeños, cada uno asignado a una de tres regiones: tumor, tejido inmediatamente circundante al tumor (peri-tumoral) o hígado no tumoral distante. Se excluyeron cuidadosamente los azulejos que contenían tejido muerto (necrótico) o artefactos mayores, porque pueden imitar patrones vasculares densos e irreales.
Cómo difieren las regiones tumorales del resto
En miles de azulejos, el estudio encontró diferencias claras y estadísticamente robustas en los patrones vasculares entre las tres regiones del hígado. El tejido hepático no tumoral mostró la mayor complejidad, comportándose casi como una red que llena el espacio a escalas mayores. El tejido peri-tumoral quedó en un punto intermedio, mientras que las regiones tumorales presentaron complejidad consistentemente menor. Una medida relacionada de cómo se disponen los espacios vacíos entre vasos también aumentó desde el tejido no tumoral al peri-tumoral y al tumoral, lo que indica que los vasos asociados al tumor están más agrupados y más correlacionados espacialmente. De manera crucial, el hecho de que el tumor hubiera comenzado o no a invadir vasos cercanos —una señal clínica importante— no cambió de forma medible estos patrones globales. La arquitectura de la red vascular se moldeó principalmente por la presencia del tumor en sí, no por este paso de invasión.
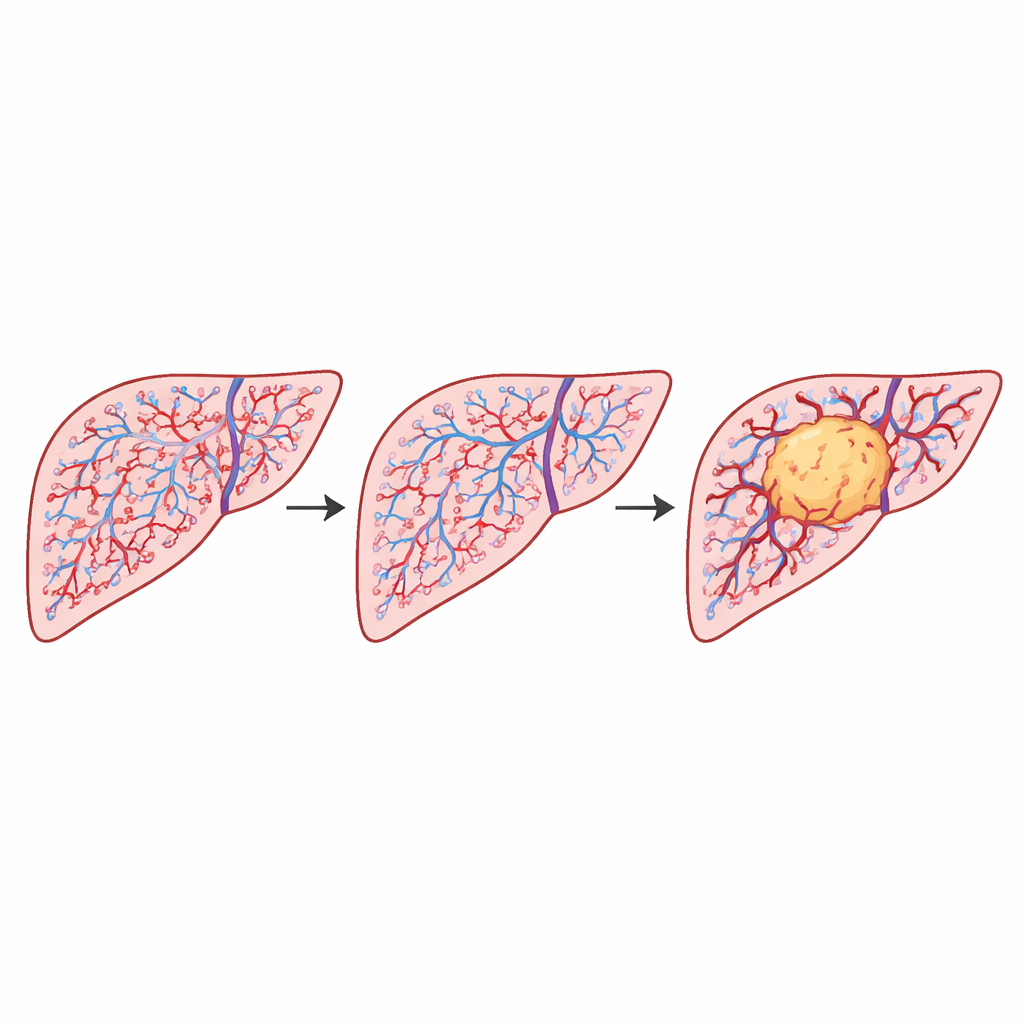
Por qué importan la forma y el tamaño de los vasos
Para entender qué subyacía a estas diferencias numéricas, los autores analizaron más detenidamente las formas y tamaños de vasos individuales. En el hígado sano, había una marcada acumulación de muchos vasos pequeños y redondeados, con algunos de mayor tamaño. En las regiones tumorales, el área vascular total fue similar, pero los vasos se distribuyeron de forma más uniforme entre tamaños y con mayor frecuencia eran alargados o irregulares. Modelos sencillos mostraron que una red rica en muchos vasos diminutos y redondeados obliga a usar más cajitas pequeñas al “cubrir” el patrón, lo que aumenta su medida de complejidad. Por el contrario, una red con menos vasos pequeños y tamaños más uniformes parece menos intrincada, aun cuando contenga aproximadamente la misma área vascular total. Este cambio geométrico concuerda con la reducción observada de complejidad en los tumores y explica cómo variaciones sutiles en la distribución de formas de los vasos pueden remodelar el patrón vascular global.
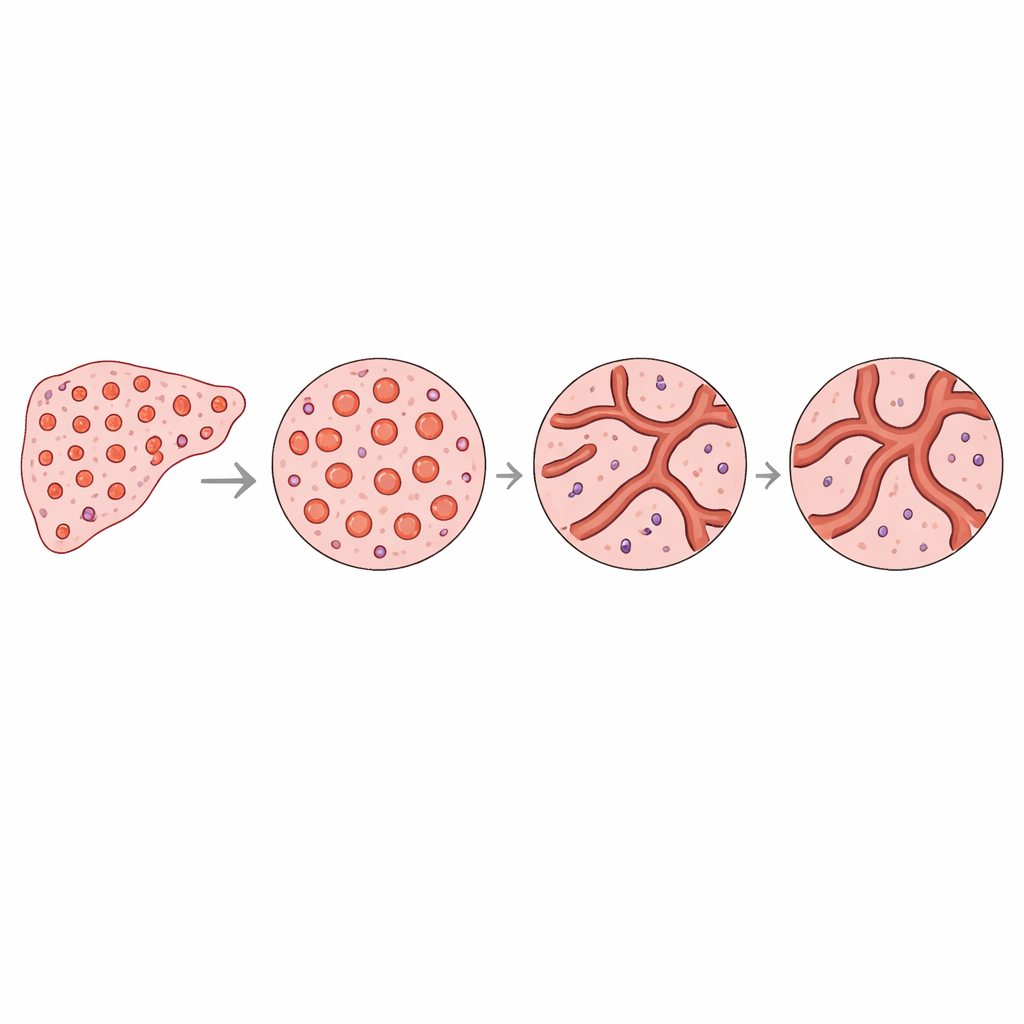
Qué podría significar esto para exploraciones futuras
Para no especialistas, la conclusión principal es que los tumores hepáticos no solo generan más vasos sanguíneos; los reorganizan de una manera distintiva y medible que se extiende al tejido circundante. Estas diferencias pueden capturarse mediante descriptores matemáticos compactos que resumen cómo se ordenan los vasos y los espacios entre ellos. El trabajo sugiere que, en el futuro, métodos avanzados de imagen podrían estimar estos descriptores sin necesidad de biopsia, proporcionando nuevos biomarcadores no invasivos de hasta qué distancia se extiende la influencia de un tumor y de cómo está estructurado su suministro sanguíneo. Al mismo tiempo, el estudio muestra que la invasión microscópica de vasos cercanos no deja necesariamente una huella reconocible en el patrón vascular a gran escala, lo que subraya que no todos los comportamientos tumorales peligrosos son visibles solo a través de la arquitectura vascular.
Cita: Penney, J., Nardon, V., Beaufrere, A. et al. Fractal analysis of hepatocellular carcinoma vasculature shows regional differences independent of vascular invasion. Sci Rep 16, 11049 (2026). https://doi.org/10.1038/s41598-026-38580-x
Palabras clave: vasculatura del cáncer de hígado, arquitectura fractal de vasos, carcinoma hepatocelular, microambiente tumoral, biomarcadores de imagen no invasivos