Clear Sky Science · es
Optimización de agentes ligantes de la galectina‑3 mediante síntesis múltiple in situ y espectrometría de masas nativa
Por qué importa para los medicamentos del futuro
Muchos medicamentos modernos actúan uniéndose a proteínas dentro de nuestro organismo, pero encontrar una pequeña molécula que se adhiera con alta afinidad y selectividad al sitio correcto es lento, costoso y con frecuencia frustrante. Este estudio presenta una forma más rápida de afinar tales moléculas directamente en presencia de la proteína diana y, a continuación, identificar las ganadoras mediante una técnica de pesaje altamente sensible. Los autores ilustran su enfoque con la galectina‑3, una proteína vinculada al crecimiento del cáncer, y obtienen un candidato prometedor de tipo fármaco que se une con tanta fuerza como algunos de los mejores compuestos existentes, pero en un bolsillo inesperado de la superficie proteica.

Repensar cómo buscamos mejores candidatos farmacológicos
La optimización tradicional de fármacos se parece a un costoso juego de adivinanzas. Los químicos modifican un compuesto inicial paso a paso, prueban cada versión y esperan mejorar la afinidad por la proteína diana. Pero las superficies proteicas son flexibles, las moléculas de agua interfieren y el propio evento de unión puede remodelar la proteína, lo que hace que las predicciones por ordenador sean poco fiables. Incluso cuando se dispone de una estructura de alta resolución, no hay garantía de que un cambio sugerido sea beneficioso. Los métodos “guiados por el objetivo” existentes intentan dejar que la proteína elija a sus socios a partir de un conjunto de bloques de construcción, pero estos enfoques aún dependen de análisis complejos y señales indirectas para inferir qué compuesto se une realmente mejor.
Dejar que la proteína elija y luego pesar a las ganadoras
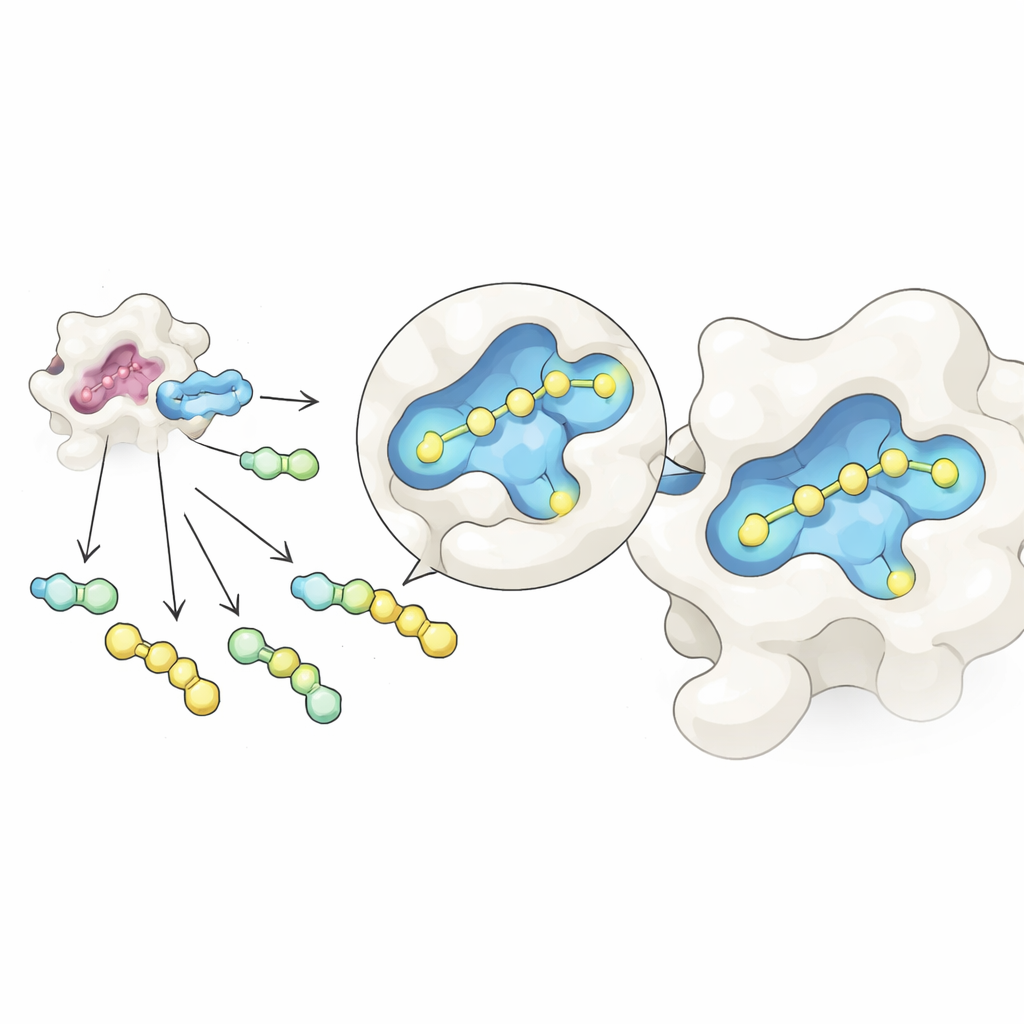
Los investigadores combinaron dos ideas en un flujo de trabajo simplificado. Primero, emplearon una reacción química reversible que enlaza un núcleo común basado en azúcar con muchas piezas laterales distintas en un mismo tubo, formando una mezcla de moléculas relacionadas. Ajustando cuidadosamente las proporciones iniciales, los productos resultantes alcanzan un estado equilibrado gobernado por reglas de concentración simples, lo que ayuda a igualar sus cantidades pese a diferencias en la reactividad bruta. Segundo, expusieron esta mezcla a la galectina‑3 y la analizaron con espectrometría de masas nativa, una modalidad que mantiene los pares proteína–molécula intactos en una solución suave, parecida al agua. Como cada candidato tiene una masa distinta, el instrumento puede detectar directamente qué moléculas están realmente unidas a la proteína, sin etiquetas ni marcadores de referencia.
De mezclas concurridas a un ligando destacado
Con este planteamiento, el equipo creó decenas de ligantes de galectina‑3 al unir diversos grupos laterales a un núcleo azucarado inspirado en un inhibidor conocido, GB1107. Dividieron 35 hidrazidas diferentes en grupos manejables, formaron todas las combinaciones in situ y luego añadieron galectina‑3. La espectrometría de masas nativa resaltó los compuestos que más frecuentemente viajaban asociados con la proteína, señalándolos como impactos principales. Una prueba de estabilidad térmica posterior, que mide cómo un compuesto estabiliza la proteína al calentarse, filtró falsos positivos causados por particularidades de la medición en fase gaseosa. Quedaron tres candidatos principales, y medidas detalladas de unión basadas en calor mostraron que uno, denominado GalAldBZ20, se unía a la galectina‑3 con especial fuerza, en el rango submicromolar.
Descubrir un bolsillo oculto y fortalecerlo
La siguiente sorpresa surgió al examinar cómo se alojaba GalAldBZ20 en la superficie de la galectina‑3. La mayoría de los ligandos conocidos usan un bolsillo “alfa” próximo al sitio de unión del azúcar, pero métodos estructurales y simulaciones por ordenador indicaron que GalAldBZ20 prefería en su lugar un bolsillo vecino “beta”. La cristalografía de rayos X apuntó a ello, la resonancia magnética nuclear en solución reveló múltiples conformaciones locales cerca de ese bolsillo y las simulaciones de dinámica molecular apoyaron un modelo en el que un anillo portador de un grupo nitro del compuesto encaja en el sitio beta. Partiendo de la hipótesis de que podían fijar esta disposición de forma más firme, los químicos rediseñaron el enlazador químico entre el azúcar y el anillo nitro para favorecer nuevos contactos polares con la proteína y reducir la flexibilidad.
Convertir una pantalla ingeniosa en un candidato potente
Con esta intuición, el equipo sintetizó un pequeño conjunto de moléculas de seguimiento más rígidas que conservaban el mismo azúcar y el anillo nitro, pero cambiaban el conector entre ellos. Una versión, una N‑galactósido (compuesto 5), destacó: se unió a la galectina‑3 aproximadamente diez veces más fuertemente que el impacto original, alcanzando una afinidad comparable a la de GB1107, y aun así prefería el bolsillo beta. Una estructura cristalina de ultra‑alta resolución mostró densidad clara para el anillo nitro anidado en ese bolsillo, sostenido por varios enlaces de hidrógeno y un contacto catión‑π con aminoácidos clave. Cuando se eliminó el grupo nitro o se sustituyó por un metilo simple, la unión se debilitó notablemente, subrayando su importancia. Dado que la galectina‑1, una proteína relacionada, carece de este bolsillo beta, el nuevo compuesto podría ofrecer en última instancia mejor selectividad, una cualidad muy valorada en el diseño de fármacos.
Qué significa esto para el descubrimiento de fármacos futuro
En términos accesibles, este trabajo muestra que se puede mezclar muchas moléculas relacionadas, dejar que una proteína relevante para la enfermedad “elija” sus favoritas y luego pesar directamente esos pares proteína–molécula para ver cuáles se adhieren mejor. Aplicado a la galectina‑3, esta estrategia encontró inesperadamente y posteriormente fortaleció la unión a un bolsillo poco explorado, produciendo un compuesto que rivaliza con algunos de los mejores inhibidores existentes y que puede servir como punto de partida para nuevos fármacos anticancerígenos. Más ampliamente, acoplar química in situ con espectrometría de masas nativa ofrece un atajo general para refinar candidatos farmacológicos frente a proteínas con múltiples sitios de unión posibles, ahorrando potencialmente tiempo, material y esfuerzo en las etapas iniciales del descubrimiento de fármacos.
Cita: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
Palabras clave: inhibidores de galectina‑3, espectrometría de masas nativa, descubrimiento de fármacos basado en fragmentos, síntesis guiada por el objetivo, candidatos farmacológicos contra el cáncer