Clear Sky Science · es
Comparación y combinación de xevinapant con inhibición de ATR y PARP para la radiosensibilización de células de CEC de cabeza y cuello negativas para VPH
Por qué es importante potenciar la radiación
La radioterapia es un tratamiento fundamental para los cánceres de boca y garganta, pero muchos tumores se le resisten, lo que obliga a los médicos a emplear dosis altas que pueden dañar tejidos sanos. Este estudio plantea una pregunta práctica con grandes implicaciones para los pacientes: entre varios fármacos modernos diseñados para hacer las células tumorales más vulnerables, ¿cuáles funcionan mejor con la radiación frente a los difíciles cánceres de cabeza y cuello negativos para VPH cultivados en el laboratorio?
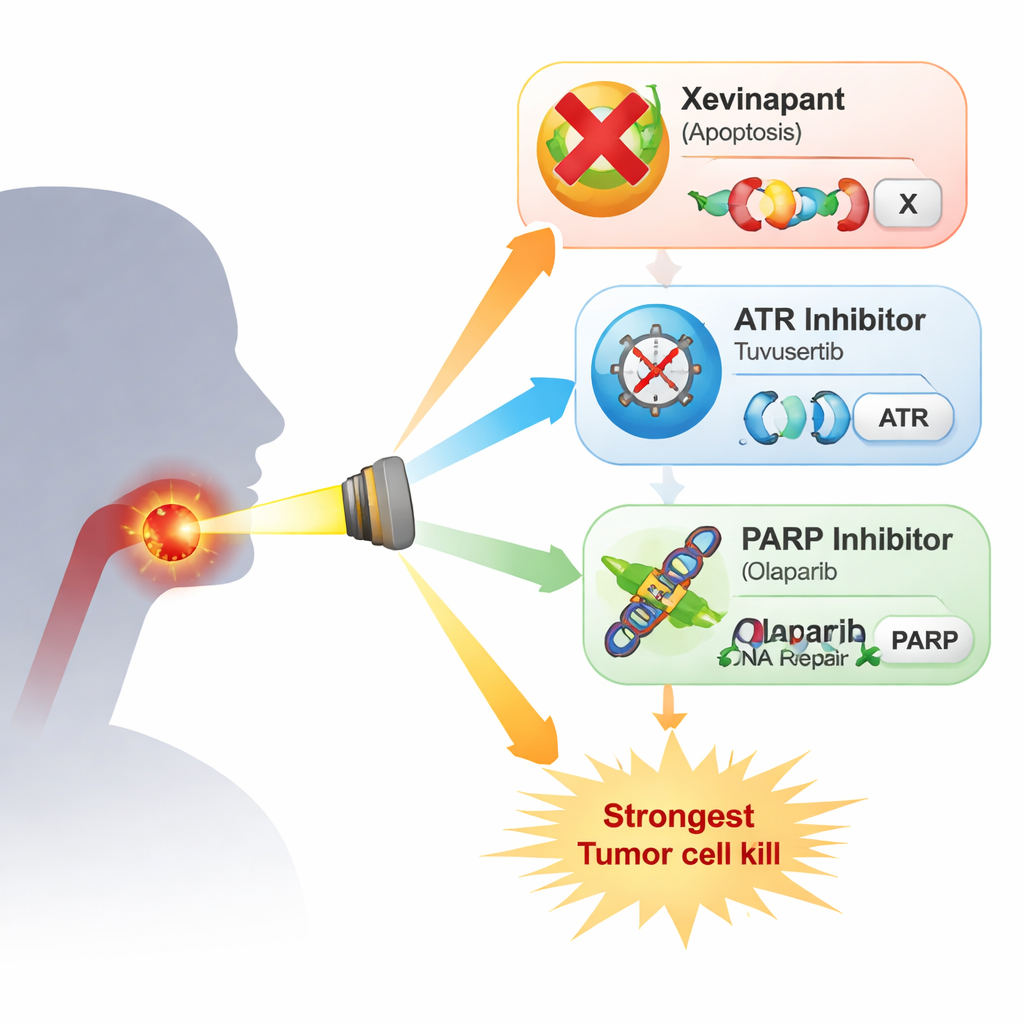
Tratamiento actual y sus límites
Las personas con carcinoma escamoso de cabeza y cuello localmente avanzado suelen recibir una combinación de radiación y el quimioterápico cisplatino, o cirugía seguida de radioterapia. Aunque este enfoque puede controlar el cáncer, frecuentemente deja a los pacientes con efectos secundarios a largo plazo graves, como dificultad para tragar, sequedad bucal, problemas de audición y daño renal. Muchos pacientes de edad avanzada o con fragilidad médica no toleran el cisplatino. Esto ha impulsado un intenso interés en los “radiosensibilizadores”: fármacos que facilitan la eliminación de las células tumorales con radiación para que el tratamiento sea más eficaz o, potencialmente, más suave.
Un fármaco prometedor que tropezó
Uno de estos fármacos, xevinapant, fue inicialmente celebrado como un avance. Imitaba a una proteína natural llamada SMAC y bloqueaba moléculas que ayudan a las células cancerosas a evitar la muerte celular programada. En trabajos anteriores, añadir xevinapant a la quimiorradioterapia estándar mejoró los resultados en un ensayo clínico de fase 2 para cáncer de cabeza y cuello, lo que despertó la esperanza de que pudiera convertirse en un nuevo estándar. Pero un ensayo mucho mayor de fase 3, llamado TrilynX, se detuvo de forma prematura cuando los datos interinos mostraron no solo ausencia de beneficio, sino incluso peor supervivencia y más efectos secundarios en el grupo tratado con xevinapant. Ese fracaso inesperado creó la necesidad urgente de reevaluar hasta qué punto xevinapant ayuda realmente a la radiación y de compararlo con otras estrategias más recientes.
Poniendo tres estrategias cara a cara
Los investigadores estudiaron cuatro líneas celulares de cáncer de cabeza y cuello negativas para VPH resistentes a la radiación. Compararon xevinapant con dos fármacos que dirigen la respuesta al daño del ADN: el inhibidor de ATR tuvusertib y el inhibidor de PARP olaparib, ambos usados a dosis similares a las alcanzables en pacientes. ATR y PARP son actores clave que ayudan a las células a detener el ciclo celular y reparar el ADN tras daños como los provocados por los rayos X. En ensayos simples de crecimiento, cada fármaco por sí solo ralentizó la proliferación celular solo de forma moderada, y los patrones variaron entre las líneas. Cuando se combinaron con radiación en el ensayo más exigente—contar cuántas células individuales aún pueden formar colonias—la imagen se clarificó: xevinapant aportó solo un efecto adicional leve o nulo en varias líneas, mientras que tanto tuvusertib como olaparib consistentemente hicieron la radiación más letal. El mayor impacto se observó al combinar la inhibición de ATR y PARP, que produjo caídas especialmente pronunciadas en la supervivencia de colonias en tres de las cuatro líneas celulares.
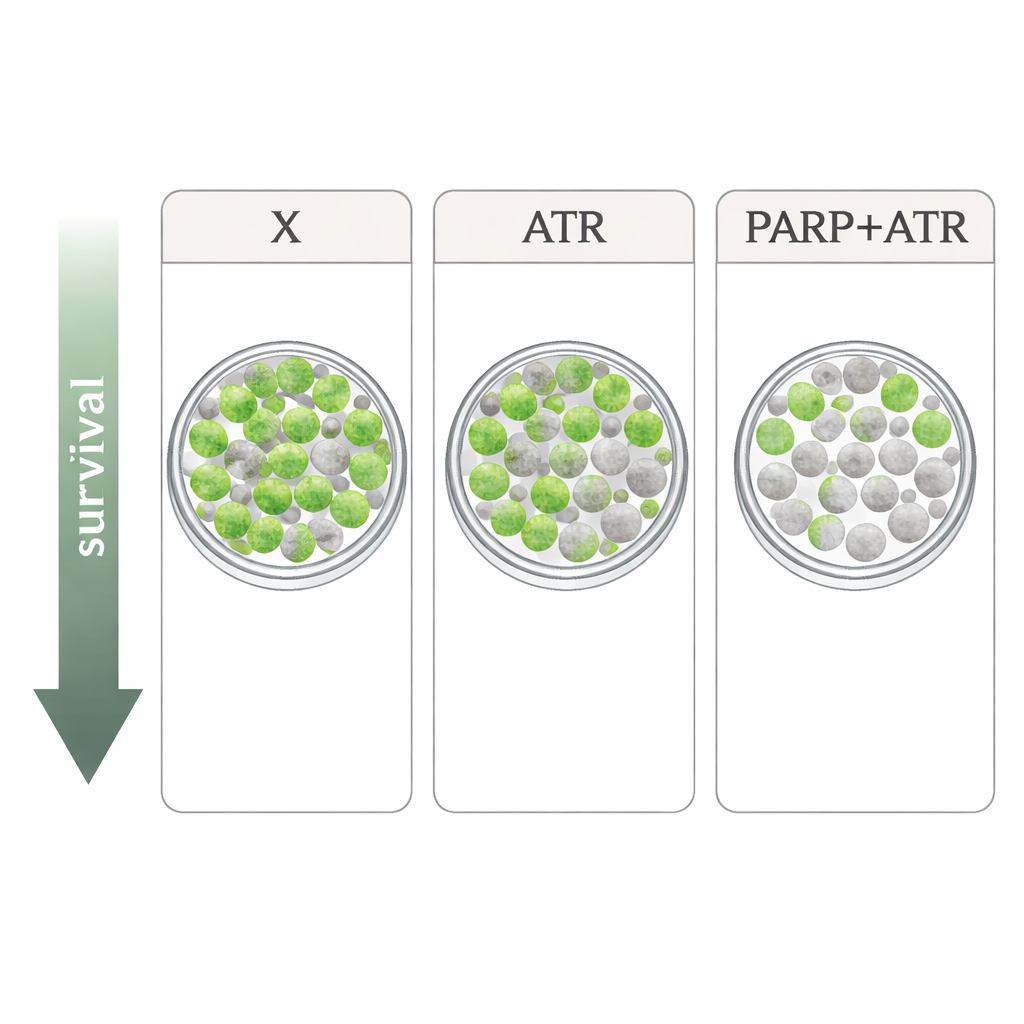
Las señales de muerte celular no explican todo
Dado que xevinapant está diseñado para desencadenar la muerte celular, el equipo también midió cuántas células se volvían apoptóticas o lizadas tras el tratamiento, con y sin radiación. Estos marcadores de muerte aumentaron de forma notable en algunos contextos—particularmente en una línea llamada HSC4 y cuando se combinaron fármacos—pero no se correlacionaron de forma fiable con la capacidad real de la radiación para suprimir la supervivencia a largo plazo. En otras palabras, las lecturas de muerte a corto plazo fueron pobres predictores de la verdadera radiosensibilización. Esta discrepancia subraya una lección clave para el desarrollo de fármacos: solo los ensayos que siguen a las células el tiempo suficiente para observar si pueden volver a crecer—como las pruebas de formación de colonias—pueden juzgar correctamente si un radiosensibilizador es efectivo.
Qué significa esto para futuros tratamientos
De estos experimentos de laboratorio se deduce que xevinapant tiene alguna capacidad para potenciar la radiación en células de cáncer de cabeza y cuello negativas para VPH, pero su efecto fue más débil y menos consistente que el de enfoques que interfieren directamente con el manejo del daño del ADN mediante ATR y PARP. La combinación de inhibidores de ATR y PARP ofreció el efecto más potente, lo que sugiere que combinaciones cuidadosamente dosificadas de estos fármacos con radioterapia pueden ofrecer una vía más prometedora que seguir profundizando en xevinapant, al menos para este tipo de cáncer. Traducir estos hallazgos a la clínica no será sencillo, ya que estos fármacos también pueden afectar a tejidos normales de rápida división y ya han requerido reducciones de dosis en ensayos tempranos. Aun así, el trabajo orienta a clínicos e investigadores hacia estrategias dirigidas a la reparación del ADN como candidatas más convincentes para hacer la radioterapia tanto más eficaz como, potencialmente, más segura para pacientes que no pueden recibir la quimioterapia estándar.
Cita: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
Palabras clave: cáncer de cabeza y cuello, radioterapia, inhibidores de reparación del ADN, xevinapant, radiosensibilización