Clear Sky Science · es
Las adaptaciones termorreguladoras al frío en ratones C3H/HeJ son independientes de la señalización ADRB3
Por qué importan los ratones aficionados al frío para la salud humana
Mantenerse caliente puede no parecer un asunto médico de vanguardia, pero la forma en que el organismo afronta el frío tiene todo que ver con cómo usa y quema energía. Este estudio examina dos tipos comunes de ratones de laboratorio y plantea una pregunta sorprendentemente importante: cuando pasan frío, ¿activan sus “hornos” internos de la misma manera que los humanos? La respuesta ayuda a explicar por qué algunos fármacos antiobesidad que funcionaron en ratones fracasaron en humanos, y apunta a un modelo de ratón más parecido al humano para estudiar el metabolismo.
Dos tipos de ratones, un mismo desafío frío
Los investigadores compararon ratones C57BL/6J, un caballo de batalla de la investigación metabólica, con una cepa menos usada llamada C3H/HeJ. Ambos grupos se mantuvieron primero a unos 30 °C, una temperatura en la que los ratones apenas necesitan gastar energía para mantenerse calientes. Luego los animales se enfriaron gradualmente hasta 10 °C, y su peso corporal, ingesta de alimento y consumo de energía se midieron cuidadosamente dentro de jaulas metabólicas de alta tecnología. Curiosamente, ambas cepas compartieron casi el mismo “punto de confort” para un gasto mínimo de energía —alrededor de 29–30 °C—, lo que significa que partían de una línea base similar antes de enfrentarse al frío.
Cuando llega el frío, una cepa trabaja más
Cuando las temperaturas bajaron, ambos tipos de ratones aumentaron su gasto energético, como era de esperar. Pero los C3H consumieron más energía que los C57, aun cuando comieron cantidades similares de alimento. Este mayor consumo no fue solo una reacción a corto plazo: persistió tanto en las primeras horas como en los días siguientes de exposición al frío. A pesar de ello, los C3H acabaron más ligeros y con menos tejido adiposo marrón en conjunto, lo que sugiere que su grasa existente trabajó más duro en lugar de simplemente crecer. Los análisis de sangre también indicaron que los C3H movilizaron más combustibles, como glicerol, para alimentar esta producción de calor adicional.
La grasa marrón y blanca se suman al equipo térmico
Para ver qué ocurría internamente, el equipo examinó la grasa marrón —el tejido clásico generador de calor— así como dos tipos de grasa blanca. En los C3H, el frío aumentó con fuerza la actividad de genes relacionados con la producción de calor en la grasa marrón, y las proteínas clave que sustentan la quema de combustible y la actividad mitocondrial se activaron más intensamente. La microscopía mostró cambios estructurales coherentes con un tejido más activo. La grasa blanca contó una historia similar: en particular, un depósito alrededor de los testículos, normalmente lento para convertirse en células productoras de calor, mostró una activación llamativa en los C3H. Esto sugiere que en estos animales no solo la grasa marrón, sino también la grasa tradicionalmente «de reserva» puede reclutarse para ayudar a mantener el calor corporal.
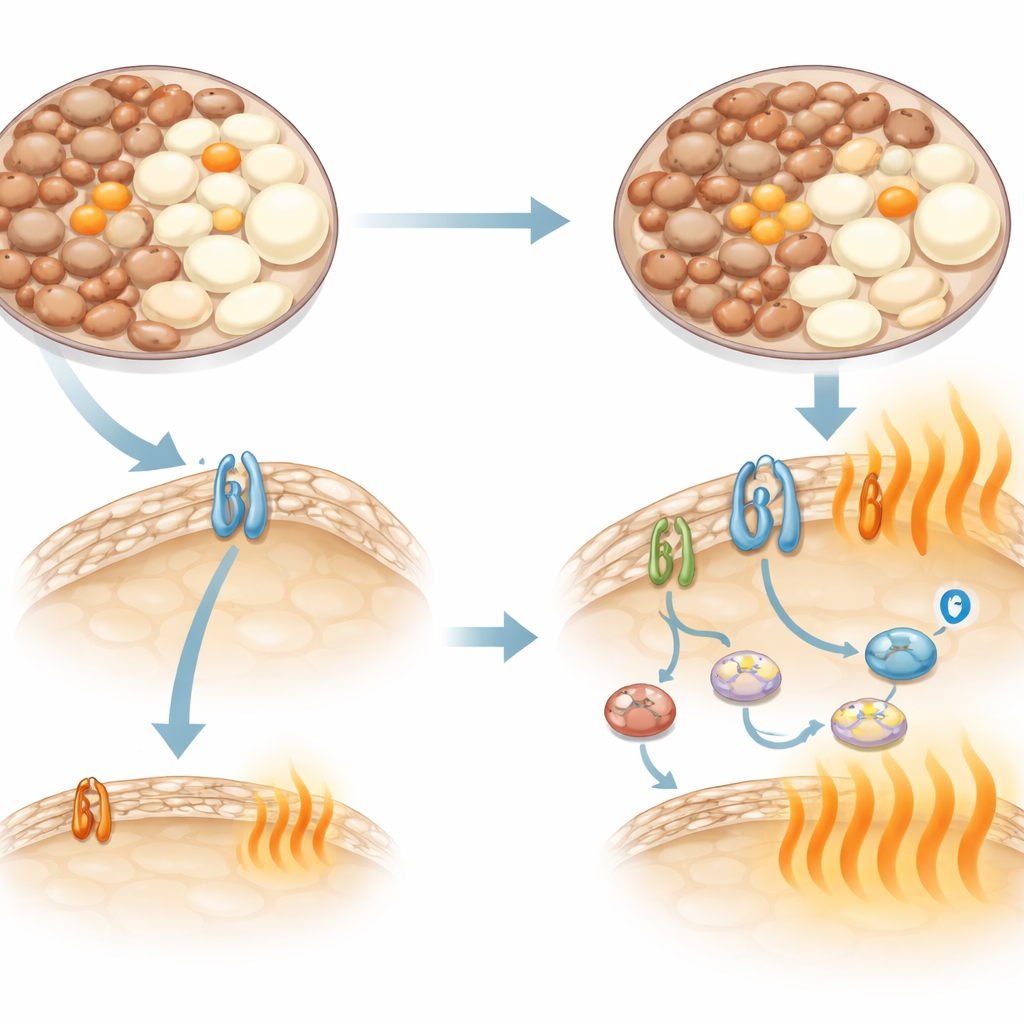
Una conexión nerviosa diferente hacia la grasa
La producción de calor en la grasa suele estar impulsada por señales del sistema nervioso que actúan a través de receptores beta-adrenérgicos en las células grasas. En los ratones C57 estándar, un receptor llamado beta-3 desempeña un papel principal, y los fármacos que lo estimulan aumentan mucho el gasto energético. Los investigadores confirmaron esto: un compuesto selectivo dirigido a beta-3 provocó un aumento grande y sostenido del gasto energético en los C57. Pero en los C3H, ese mismo fármaco solo tuvo un efecto débil y breve. Los análisis genéticos explicaron por qué: estos ratones expresaban apenas el receptor beta-3 en su grasa. Aun así, cuando ambas cepas recibieron noradrenalina, una señal natural que activa varios receptores relacionados, los C3H aumentaron su gasto energético. Bloquear los receptores beta-1 y beta-2 borró en gran medida las diferencias entre cepas, lo que indica que los C3H dependen de estos receptores alternativos y de otras vías no clásicas de producción de calor en lugar de beta-3.
Qué significa esto para estudiar el metabolismo humano
Los humanos, al igual que los C3H, dependen sobre todo de los receptores beta-1 y beta-2 en su grasa marrón, no de beta-3. Esto puede explicar por qué los fármacos dirigidos a beta-3 funcionaron en cepas de ratón típicas pero decepcionaron en ensayos clínicos. Al mostrar que los C3H pueden generar una fuerte termogénesis inducida por frío con casi nula señalización beta-3, este estudio los destaca como un modelo más parecido al humano para investigar cómo la grasa quema energía. Para el lector, la conclusión es que no todos los ratones son iguales: elegir la cepa adecuada y la temperatura de alojamiento correcta puede hacer que la investigación preclínica sea mucho más relevante para la salud humana real y para futuras terapias contra la obesidad y la enfermedad metabólica.
Cita: Beji, S., Mouchiroud, M., Gélinas, Y. et al. Thermoregulatory adaptations to cold in C3H/HeJ mice are independent of ADRB3 signaling. Sci Rep 16, 7859 (2026). https://doi.org/10.1038/s41598-026-38538-z
Palabras clave: tejido adiposo marrón, adaptación al frío, señalización adrenérgica, modelos de ratón, gasto energético