Clear Sky Science · es
Inhibición selectiva de HDAC8 con compuestos no hidroxamato [1,2,4]triazolo[4,3-a]quinolina
Nueva esperanza para un cáncer infantil
El neuroblastoma es un cáncer infantil agresivo que se origina en células nerviosas y que suele ser difícil de tratar una vez que se ha diseminado. Este estudio explora una nueva forma de frenar o eliminar las células de neuroblastoma apagando un interruptor celular clave llamado HDAC8. Al construir una nueva familia de moléculas con carácter farmacológico que actúan de manera muy selectiva sobre este interruptor, los investigadores aspiran a crear tratamientos que sean a la vez más efectivos contra los tumores y más benignos para el resto del organismo.
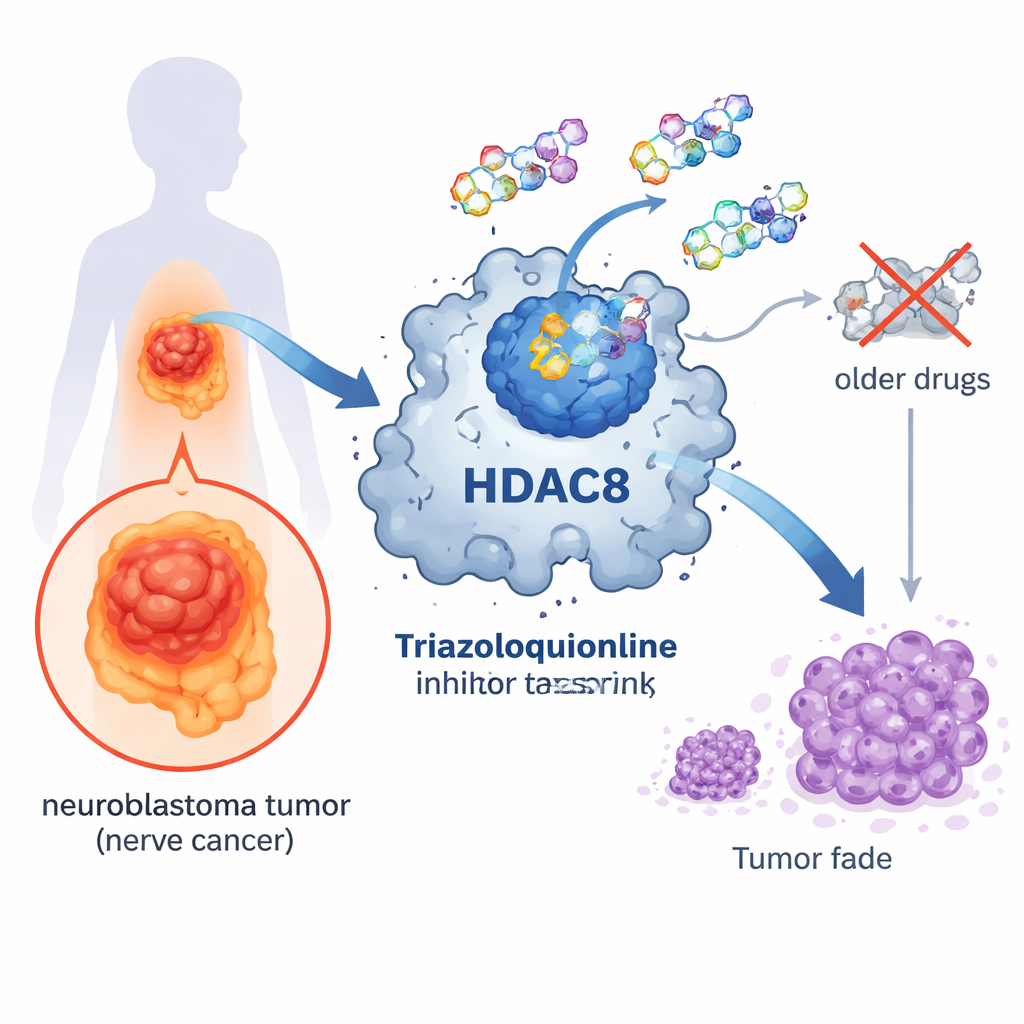
Un interruptor molecular en el corazón del cáncer
Dentro de nuestras células, los genes se encienden y apagan constantemente. Un sistema de control importante depende de pequeñas etiquetas químicas llamadas grupos acetilo que se unen a proteínas asociadas al ADN. Las enzimas llamadas histona deacetilasas (HDAC) eliminan estas etiquetas, compactando el empaquetamiento del ADN y, por lo general, reduciendo la actividad génica. HDAC8 es un miembro de esta familia enzimática y se ha vinculado con varios cánceres, incluido el neuroblastoma. Cuando HDAC8 está sobreactivo, las células cancerosas pueden crecer, sobrevivir y diseminarse con mayor facilidad, lo que lo convierte en un objetivo atractivo para nuevos fármacos.
Limitaciones de los antiguos fármacos contra las HDAC
Varios fármacos que bloquean las HDAC ya están aprobados para algunos cánceres hematológicos, pero tienden a afectar a muchos tipos de HDAC a la vez. La mayoría de estos medicamentos usan un grupo químico hidroxamato para sujetar un ion metálico en el sitio activo de la enzima. Aunque es eficaz, este grupo se une a los metales con tanta fuerza que puede provocar efectos secundarios y limita la capacidad del fármaco para distinguir con precisión entre las diferentes HDAC. Como resultado, los pacientes pueden experimentar toxicidad y las células normales pueden resultar dañadas junto con las cancerosas. Por ello, los investigadores han buscado diseños químicos alternativos que conserven los beneficios antitumorales y reduzcan el daño no deseado.
Diseño de una nueva clase de inhibidores dirigidos
En este trabajo, el equipo diseñó y sintetizó 21 nuevos compuestos construidos alrededor de un armazón de triazoloquinolina, conectado mediante un enlazador flexible a una región de «+amino amida» que puede unirse al átomo de zinc en el sitio activo de HDAC8. Usando diseño asistido por ordenador, eligieron esta arquitectura para encajar en un estrecho “canal de liberación de acetato” único de HDAC8, una característica estructural que ayuda a lograr alta especificidad. Estudios detallados de acoplamiento (docking) y simulaciones de dinámica molecular mostraron que varias de las nuevas moléculas —especialmente las denominadas 9m y 9r— forman interacciones estables y duraderas dentro del bolsillo de HDAC8 y se unen tan fuertemente como, o más que, un inhibidor de referencia bien conocido. De forma importante, las pruebas bioquímicas confirmaron que los mejores compuestos bloquean fuertemente HDAC8 mientras dejan a la mayoría de los demás miembros de la familia HDAC prácticamente intactos.
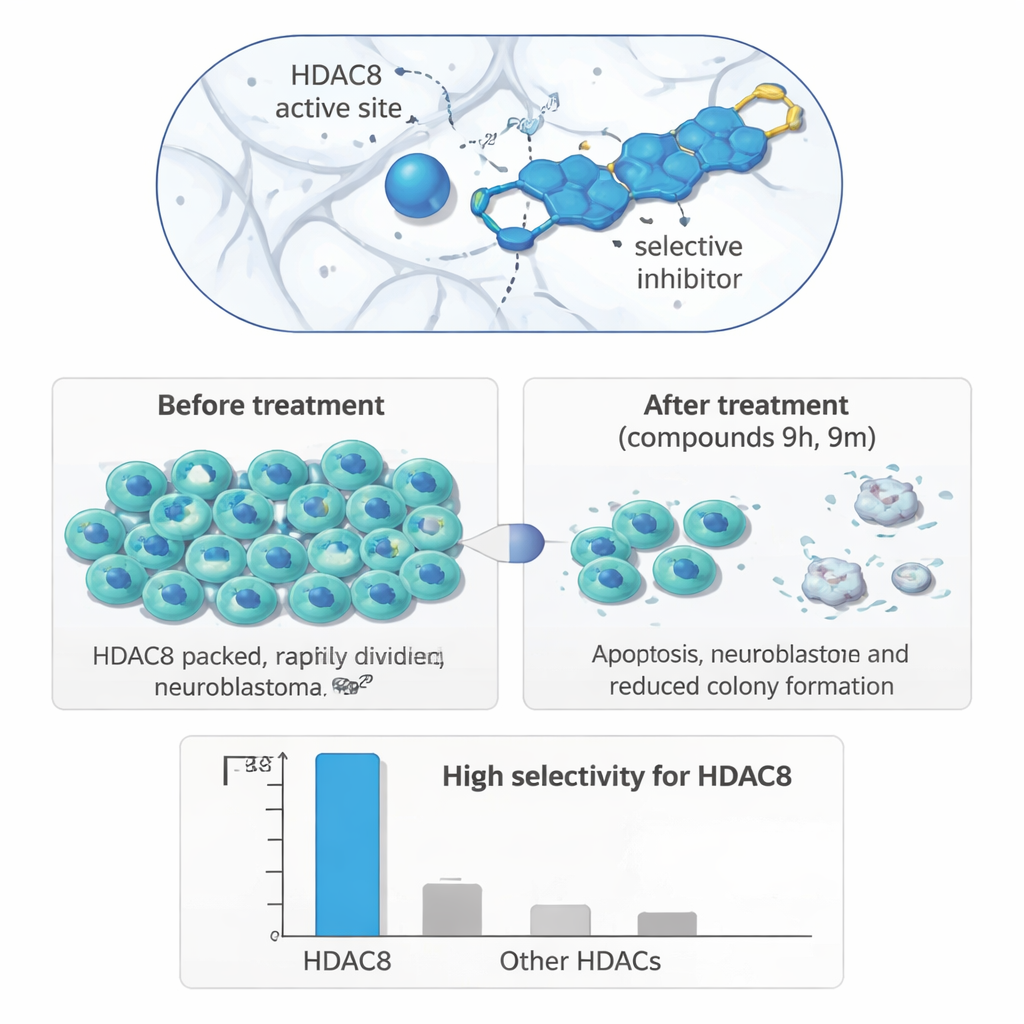
De la probeta a las células tumorales
Para comprobar si este apuntado enzimático preciso se traduce en efectos biológicos útiles, los investigadores probaron sus compuestos en un panel de líneas celulares humanas. En células de neuroblastoma (IMR‑32), dos moléculas, 9h y 9m, destacaron claramente: redujeron el crecimiento celular a concentraciones micromolares y lo hicieron de forma más pronunciada en neuroblastoma que en células de cáncer de mama o colon, o en células renales no cancerosas. Experimentos de formación de colonias a largo plazo mostraron que las células de neuroblastoma tratadas perdieron gran parte de su capacidad para volver a crecer tras la exposición al fármaco. En un ensayo de cicatrización de heridas, que mide la rapidez con que las células migran para cerrar una grieta en una capa celular, ambos compuestos ralentizaron el movimiento de las células de neuroblastoma, lo que sugiere una reducción del potencial metastásico.
Investigando cómo los compuestos matan a las células cancerosas
Experimentos de citometría de flujo revelaron que 9h y 9m inducen la muerte celular programada (apoptosis) en las células de neuroblastoma y provocan una acumulación de células en una fase del ciclo celular asociada con daño en el ADN o muerte (Sub‑G1). Para confirmar que estos efectos se derivan realmente del bloqueo de HDAC8, el equipo midió el estado de acetilación de una proteína llamada SMC3, un objetivo conocido de HDAC8 implicado en mantener emparejadas las cromátidas hermanas durante la división celular. Cuando HDAC8 está inhibida, la SMC3 acetilada se acumula. Tras el tratamiento con 9h o 9m, los niveles de SMC3 acetilada aumentaron drásticamente, mientras que la proteína SMC3 total permaneció sin cambios, lo que constituye una fuerte evidencia de que estos compuestos afectan directamente a HDAC8 en células vivas y alteran su función normal en el control cromosómico.
Qué podría significar esto para tratamientos futuros
En conjunto, la química, la modelización por ordenador, las pruebas enzimáticas y los experimentos celulares dibujan un panorama coherente: los compuestos triazoloquinolina desarrollados son bloqueadores potentes y altamente selectivos de HDAC8 que pueden frenar el crecimiento y la diseminación de células de neuroblastoma mientras preservan otras enzimas HDAC. Al evitar el grupo hidroxamato convencional, podrían ofrecer una vía más segura para aprovechar HDAC8 como objetivo terapéutico. Aunque queda mucho trabajo por delante —especialmente estudios en animales y, eventualmente, ensayos clínicos— esta investigación sienta una base sólida para desarrollar fármacos más precisos contra el neuroblastoma infantil y, posiblemente, otras enfermedades impulsadas por HDAC8.
Cita: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Palabras clave: inhibidores de HDAC8, neuroblastoma, terapia epigenética, triazoloquinolina, fármacos oncológicos dirigidos