Clear Sky Science · es
Corrientes mediadas por GluN2A y señal de calcio en neuronas humanas derivadas de iPSC
Por qué importan las pequeñas células cerebrales cultivadas en el laboratorio
Cada vez más, los científicos recurren a células cerebrales humanas cultivadas en el laboratorio para estudiar cómo se desarrolla nuestro cerebro y para investigar qué falla en condiciones como el autismo, la epilepsia y el Alzheimer. Este estudio plantea una pregunta simple pero crucial: ¿se desarrollan estas neuronas creadas en laboratorio y establecen conexiones de manera que realmente se parezcan al cerebro humano, especialmente en cómo manejan una señal química clave llamada glutamato? La respuesta indica cómo construir modelos de “mini-cerebro” más realistas y señala nuevas vías para examinar la salud y la enfermedad cerebral.
Construir neuronas a partir de células reprogramadas
Los investigadores partieron de células madre pluripotentes inducidas humanas—células ordinarias que han sido “reprogramadas” de nuevo a un estado de célula madre. A partir de ahí, guiaron las células para que se convirtieran en precursoras neurales y, finalmente, en redes de neuronas y astrocitos de apoyo, imitando la corteza humana en desarrollo. Compararon dos protocolos de cultivo ampliamente usados. Uno, llamado medio BrainPhys, está diseñado para promover neuronas activas y eléctricamente responsivas y tiende a producir más astrocitos. El otro, un medio de mantenimiento neuronal más tradicional, favorece neuronas con menos astrocitos. Durante sesenta días, el equipo siguió cómo cambiaban estas culturas en apariencia, actividad génica y tipos celulares, encontrando que las cultivos en BrainPhys desarrollaron morfologías neuronales más elaboradas y una proporción neurona/astrocito más cercana a la del cerebro humano real.
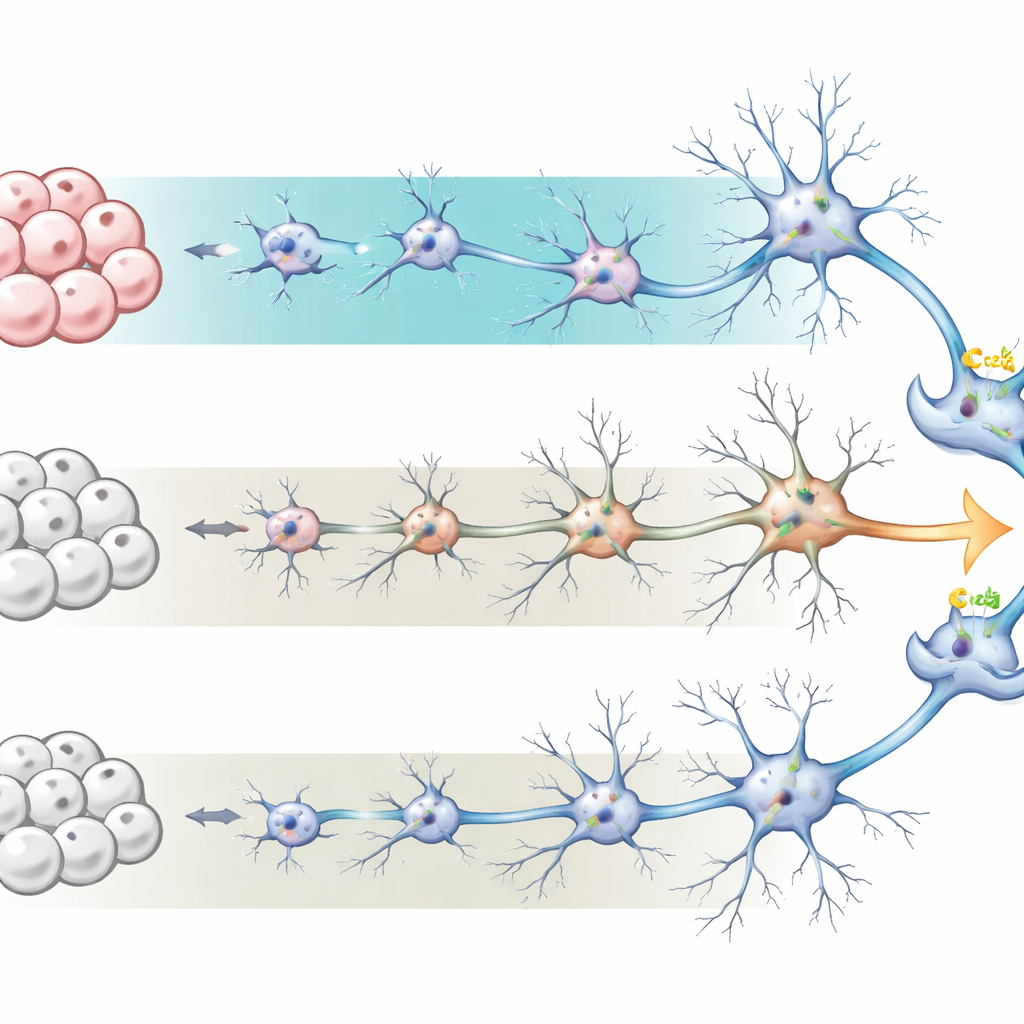
Señales de que las células están madurando
Para evaluar cuán “maduras” eran las neuronas, el equipo midió la actividad génica global mediante secuenciación de ARN al día 60. Las células cultivadas en BrainPhys mostraron casi dos mil genes expresados a niveles diferentes en comparación con el medio estándar, muchos vinculados a la diferenciación neuronal, la formación de sinapsis y la actividad eléctrica. También aumentaron los genes asociados a la función de astrocitos y a la inflamación, reflejando la mayor población de astrocitos. En conjunto, estos patrones sugieren que las culturas en BrainPhys recapitulan mejor etapas posteriores del desarrollo cerebral, con puntos de comunicación entre neuronas más refinados y un entorno de apoyo que se parece más al tejido vivo.
Interruptores clave en la comunicación química
Una característica de la maduración cerebral es un cambio en la composición de los receptores NMDA—puertas moleculares en las neuronas que se abren en respuesta al glutamato y ayudan a establecer conexiones relacionadas con el aprendizaje. Temprano en el desarrollo domina una subunidad llamada GluN2B; más tarde, GluN2A toma el relevo, cambiando cuánto tiempo y con qué intensidad permanecen abiertos los receptores. Mediante microscopía, el equipo mostró que con el tiempo más receptores NMDA se incorporaron en las sinapsis, los puntos de contacto entre neuronas, especialmente en las culturas BrainPhys. Mediciones génicas dirigidas revelaron una caída de la subunidad “temprana” GluN2B y un aumento de la subunidad “tardía” GluN2A, lo que indica que las neuronas estaban experimentando este clásico cambio del desarrollo.
Siguiendo corrientes y calcio dentro de las células
Las pruebas funcionales confirmaron que estos cambios moleculares importaban. Con electrodos de punta fina, los investigadores registraron corrientes eléctricas desencadenadas por NMDA, un compuesto que activa selectivamente los receptores NMDA. Las neuronas de ambos métodos de cultivo mostraron corrientes robustas, pero bloquear la subunidad GluN2A redujo estas corrientes aproximadamente a la mitad, demostrando que GluN2A era ahora un actor principal en el flujo de señal. El equipo siguió luego el calcio, un mensajero interno clave, usando un tinte fluorescente. Al exponerse a NMDA, una fracción mucho mayor de neuronas cultivadas en BrainPhys mostró fuertes picos de calcio, y la amplitud de la señal fue mayor. El análisis génico sugiere por qué: las culturas BrainPhys regulaban al alza múltiples componentes de canales de calcio y vías de liberación, equipando a las células para traducir la activación de receptores NMDA en señales de calcio amplias y coordinadas.
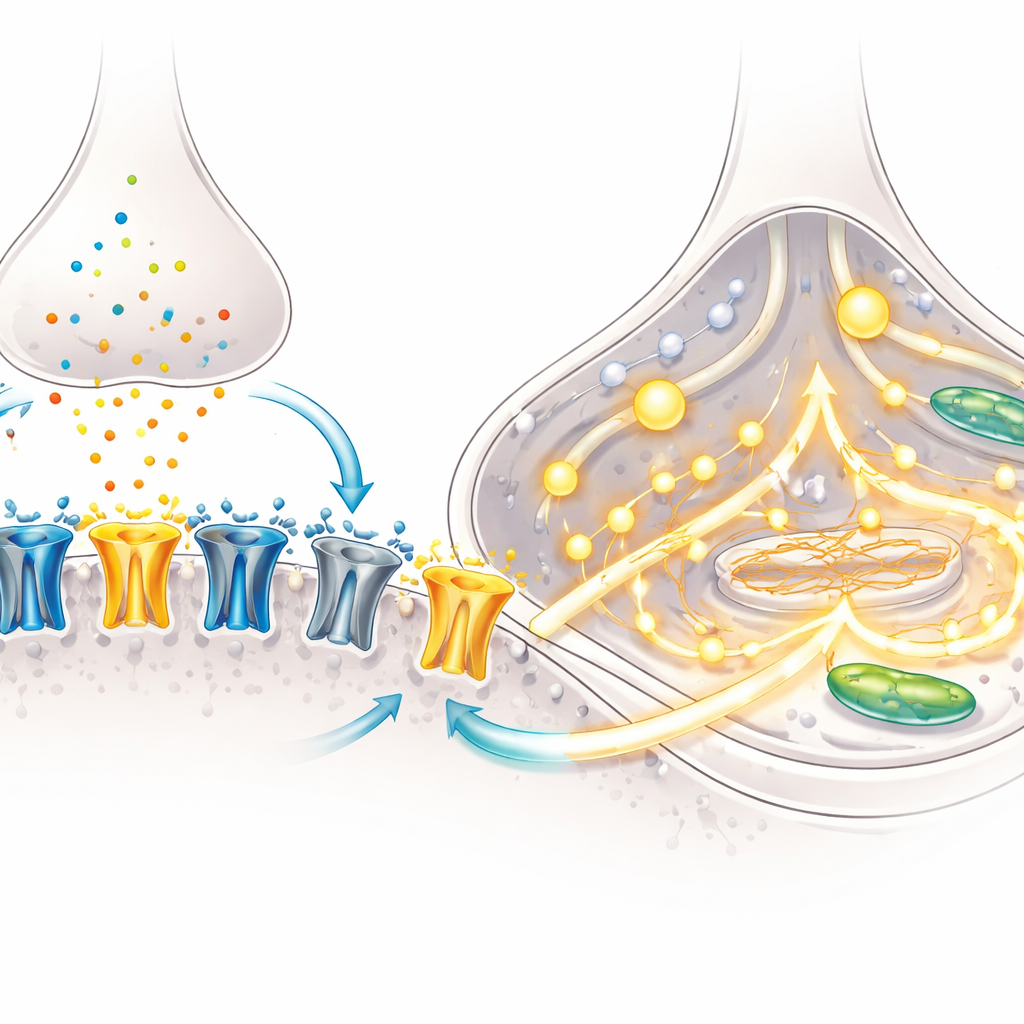
Qué significa esto para el estudio de los trastornos cerebrales
En conjunto, estos hallazgos muestran que las neuronas humanas derivadas de células madre pueden alcanzar un estado funcionalmente maduro en apenas dos meses, especialmente cuando se cultivan en condiciones que favorecen redes activas y una mezcla realista de neuronas y astrocitos. En este estado, la subunidad «similar a la adulta» GluN2A domina las corrientes de los receptores NMDA y contribuye de forma importante a la señalización por calcio, tal como en el cerebro humano en desarrollo. Para el público no especializado, la conclusión es que los investigadores disponen ahora de un modelo de laboratorio más fiel de cómo las neuronas excitadoras humanas maduran, se conectan y responden al glutamato. Esto hace posible investigar cómo cambios genéticos sutiles o procesos patológicos alteran estos interruptores finamente ajustados, abriendo una ventana a condiciones que van desde la epilepsia hasta la enfermedad de Alzheimer y orientando el diseño y la prueba de futuras terapias.
Cita: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Palabras clave: Receptores NMDA, neuronas de células madre, desarrollo cerebral, señalización de calcio, maduración sináptica