Clear Sky Science · es
El inhibidor dual de G9a y antagonista del receptor de histamina H3 A-366 mejora comportamientos repetitivos y sociales y atenúa la neuroinflamación en ratones BTBR T + tf/J
Por qué importa este estudio en ratones para el autismo
Las familias que conviven con el trastorno del espectro autista (TEA) a menudo se enfrentan a un mosaico de tratamientos que alivian solo algunos síntomas a la vez. Este estudio explora un nuevo compuesto experimental, llamado A-366, diseñado para actuar sobre dos sistemas biológicos muy diferentes al mismo tiempo. En un modelo murino ampliamente utilizado de comportamientos similares al autismo, A-366 redujo las conductas repetitivas, mejoró la interacción social y calmó la inflamación cerebral, lo que sugiere un porvenir en el que un solo fármaco podría abordar varias características centrales del TEA a la vez.
Una condición con muchas piezas en movimiento
El TEA no es una única enfermedad con una única causa. Implica dificultades en la comunicación social, conductas repetitivas y, con frecuencia, otros retos como ansiedad o problemas de atención. Detrás de estos signos externos se esconde una maraña de cambios en la química cerebral y en la regulación génica. Los fármacos actuales, como el antipsicótico aripiprazol, actúan principalmente sobre sistemas mensajeros cerebrales como la dopamina y la serotonina, y están aprobados solo para síntomas asociados como la irritabilidad. Al mismo tiempo, la investigación ha revelado que la forma en que el ADN se empaqueta y se marca químicamente dentro de las células cerebrales—la epigenética—también cambia en el TEA, al igual que la actividad de las propias respuestas inmunes e inflamatorias del cerebro. Estas múltiples capas sugieren que un enfoque de “un objetivo a la vez” puede ser demasiado estrecho.
Golpear tanto los interruptores génicos como los mensajeros cerebrales
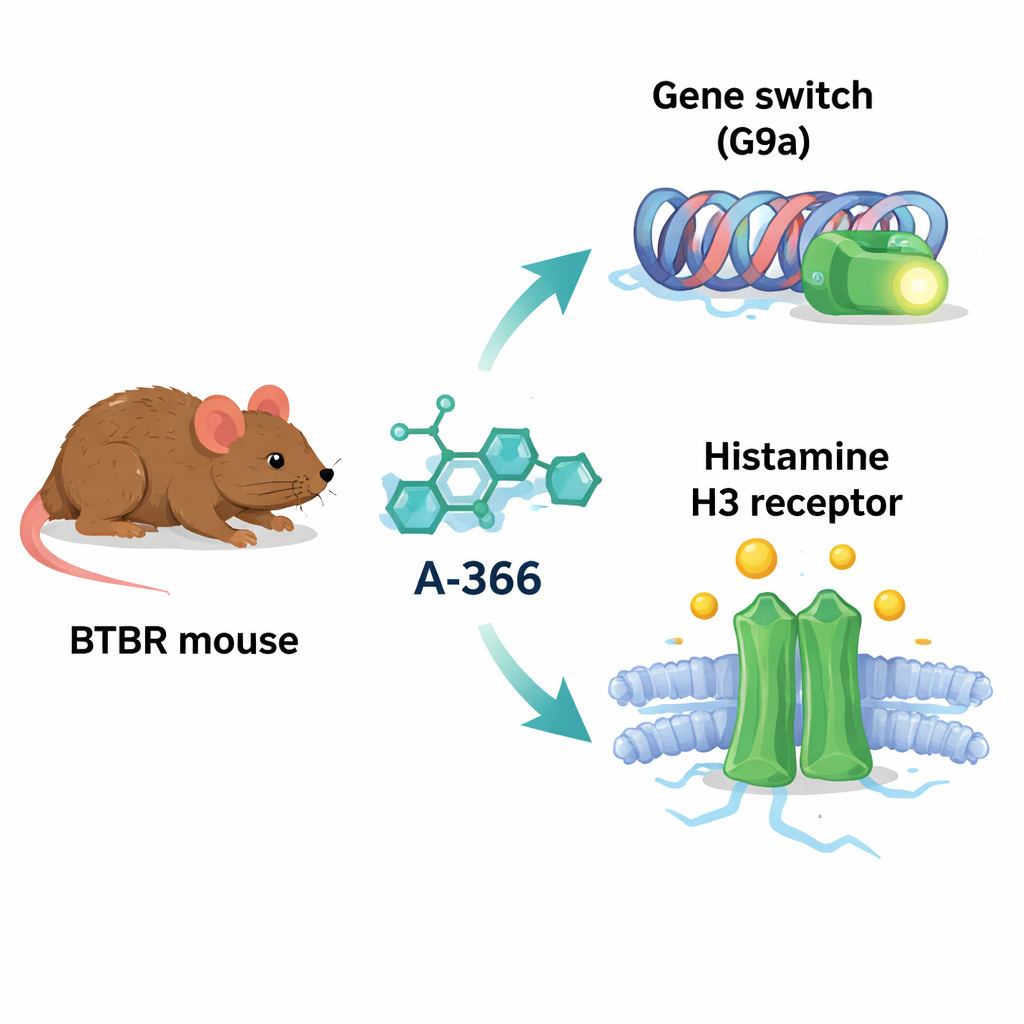
A-366 se desarrolló originalmente para bloquear una proteína llamada G9a, una enzima que añade marcas químicas a las histonas y tiende a silenciar genes. En varios trastornos cerebrales, la actividad de G9a y sus marcas aumentan, silenciando potencialmente genes importantes para el aprendizaje, la memoria y el cableado cerebral saludable. De forma intrigante, la forma química de A-366 también se asemeja a la de fármacos que bloquean el receptor de histamina H3, un regulador de la liberación de histamina y otros neurotransmisores que se ha vinculado con la atención, la vigilia y el comportamiento social. Debido a este solapamiento, los autores sospecharon que A-366 podría actuar como un “agente dual”: aflojando el silenciamiento génico nocivo mediante la inhibición de G9a y, al mismo tiempo, potenciando la señalización de la histamina al bloquear los receptores H3.
Poner a prueba A-366 en ratones con rasgos autistas
El equipo trabajó con ratones BTBR T+tf/J, una cepa que muestra de forma natural baja sociabilidad, un intenso acicalamiento y excavación repetitiva, y elevada inflamación cerebral—rasgos que reflejan aspectos clave del TEA. Ratones macho BTBR recibieron inyecciones diarias de A-366 durante tres semanas en tres dosis distintas, y su comportamiento se comparó con ratones C57 típicos y con BTBR tratados con pitolisant (un bloqueador estándar del receptor H3) o aripiprazol. En varias pruebas, A-366 redujo la excavación repetitiva, el destrozo y el acicalamiento autocausado de forma dependiente de la dosis y mejoró el rendimiento en un laberinto en Y para memoria espacial de trabajo. En la prueba social de tres cámaras, A-366 no solo restauró la preferencia de los ratones por pasar tiempo con otro ratón frente a una jaula vacía, sino que, en la dosis más alta, elevó las puntuaciones sociales al nivel de los ratones típicos y superó los efectos de pitolisant y aripiprazol.
Calmar la inflamación y confirmar los objetivos
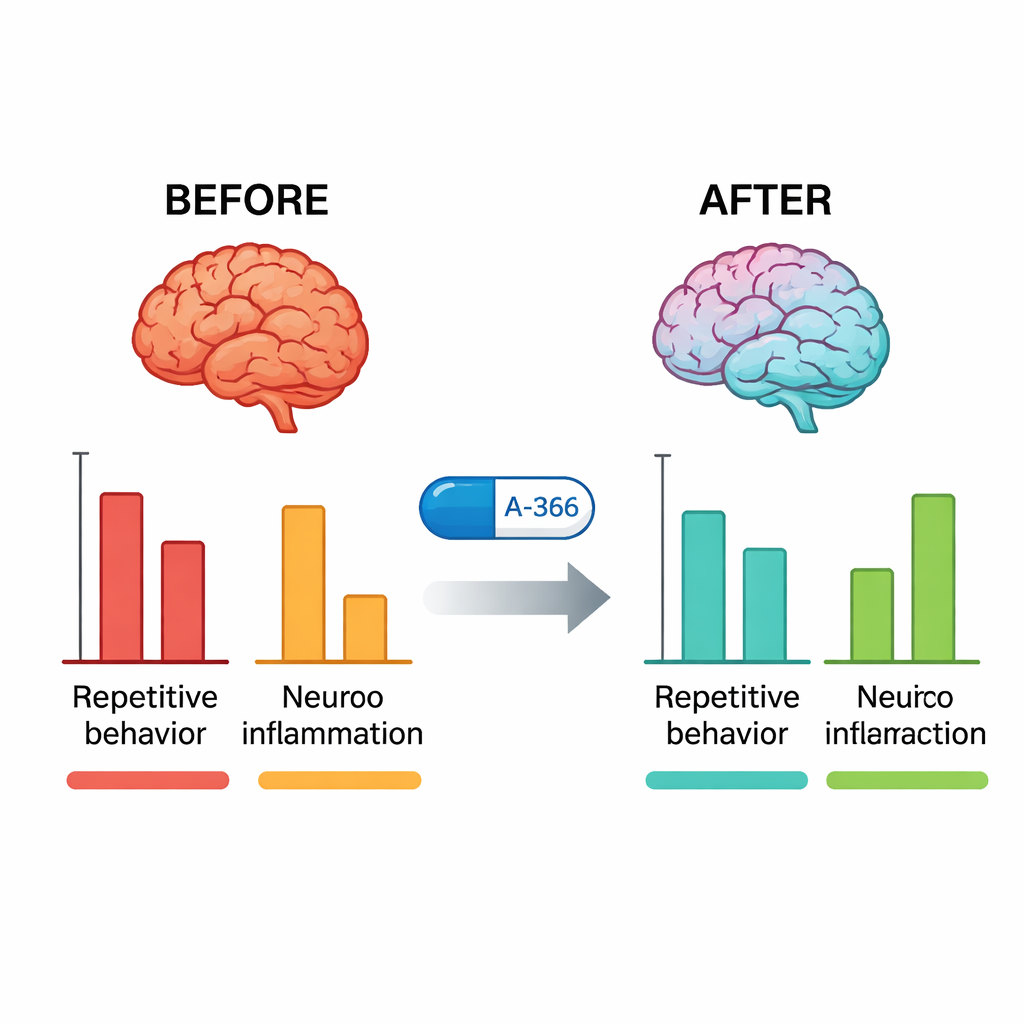
Tras las pruebas conductuales, los investigadores examinaron los cerebros de los ratones. En los BTBR no tratados, la actividad de G9a en el hipocampo y el cerebelo fue notablemente mayor que en ratones típicos. El tratamiento con A-366 redujo marcadamente esta actividad acercándola a niveles normales, mientras que el pitolisant por sí solo no lo hizo, confirmando que A-366 realmente actúa sobre su diana epigenética. Al mismo tiempo, moléculas inflamatorias clave—TNF-α, IL-6 e IL-1β—estaban muy elevadas en los BTBR y se redujeron significativamente con A-366, más que con aripiprazol. Cuando los científicos añadieron un fármaco que activa los receptores H3 (RAMH) junto con A-366, los beneficios conductuales y antiinflamatorios se revirtieron solo en parte, y la caída de la actividad de G9a se mantuvo. Este patrón respalda un mecanismo combinado: alivio epigenético estable mediante la inhibición de G9a, más una contribución mediada por histamina a través del bloqueo del receptor H3.
Qué podría significar esto para tratamientos futuros
Para un no especialista, estos hallazgos sugieren que podría ser posible diseñar fármacos que actúen a la vez sobre el “software” y el “sistema de mensajería” del cerebro. En este modelo murino de conductas similares al autismo, A-366 alivió acciones repetitivas, mejoró el compromiso social y redujo signos de inflamación cerebral crónica al aflojar simultáneamente apagones génicos dañinos y ajustar la señalización de la histamina. A-366 fue desarrollado para otras enfermedades y necesitaría optimización y pruebas de seguridad extensas antes de cualquier uso en humanos. Aun así, ofrece un plano para una nueva clase de fármacos de objetivos múltiples orientados a la compleja biología del TEA, donde abordar una sola vía a la vez hasta ahora ha ofrecido alivio limitado.
Cita: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Palabras clave: trastorno del espectro autista, terapia epigenética, receptor de histamina H3, neuroinflamación, modelo murino