Clear Sky Science · es
aFGF rescata fibroblastos senescentes inducidos por glucosa alta y mejora la cicatrización de heridas diabéticas regulando la vía SIRT1/STAT3
Por qué importan las heridas de curación lenta
Para muchas personas con diabetes, un pequeño corte en el pie o la pierna puede convertirse en una herida persistente que dura meses y, a veces, desemboca en infección o incluso amputación. Estas úlceras crónicas no son solo un problema superficial: las células de la piel que deberían reconstruir el tejido dañado a menudo envejecen prematuramente y dejan de funcionar correctamente. Este estudio explora una vía prometedora para “rejuvenecer” algunas de esas células mediante una señal de reparación de origen natural, con el objetivo de ayudar a que las heridas diabéticas cierren más rápido y de forma más completa.
Células que envejecen demasiado pronto
La piel sana depende de los fibroblastos, células de soporte que se hallan en las capas profundas de la piel, para multiplicarse, desplazarse hacia una herida y depositar un andamiaje nuevo para el tejido. En la diabetes, la hiperglucemia crónica y las moléculas dañadas por el azúcar empujan a estos fibroblastos a un estado llamado senescencia celular. Los fibroblastos senescentes ya no se dividen bien, producen menos proteínas estructurales necesarias para la reparación y, en cambio, liberan un cóctel de factores que promueven la irritación y alimentan la inflamación persistente. Los autores muestran que en ratas diabéticas la piel alrededor de una herida contiene más de estos fibroblastos envejecidos y menos proteínas de matriz útiles, lo que se correlaciona con una cicatrización mucho más lenta.
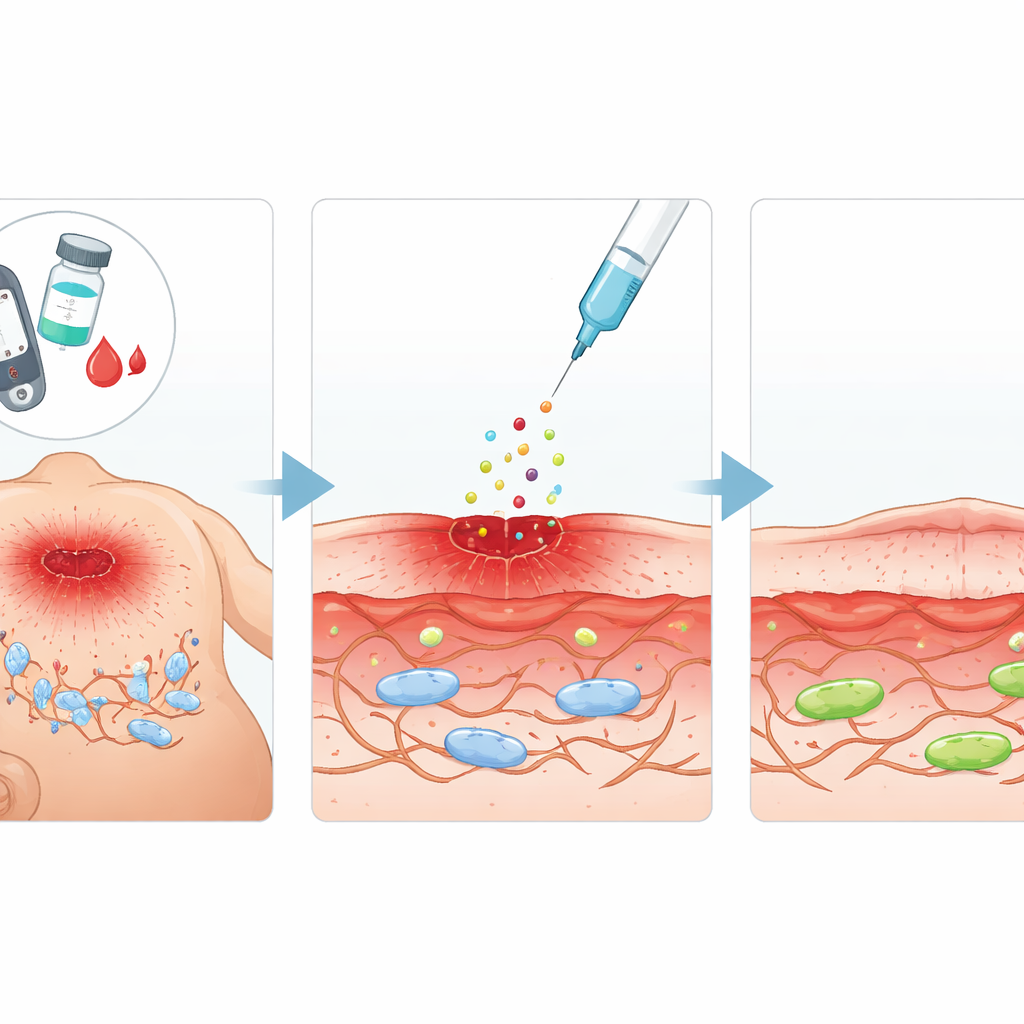
Una señal reparadora prometedora
El equipo se centró en el factor de crecimiento de fibroblastos ácido (aFGF), una proteína de origen natural conocida por estimular el crecimiento celular y la reparación tisular. Se preguntaron si el aFGF podría no solo potenciar la actividad de los fibroblastos, sino también revertir los cambios semejantes al envejecimiento inducidos por la glucosa alta. En ratas diabéticas, crearon heridas cutáneas estandarizadas e inyectaron aFGF alrededor del área lesionada cada pocos días. En comparación con animales diabéticos no tratados, las ratas tratadas con aFGF mostraron una contracción más rápida de la superficie de la herida, mejor reconstrucción del tejido subyacente y niveles más bajos de marcadores que señalan senescencia celular. En experimentos de laboratorio paralelos con una línea celular de fibroblastos de ratón expuestos a glucosa muy alta, el aFGF restauró la capacidad de las células para dividirse y migrar, dos comportamientos esenciales para cerrar una herida.
Calmar el estrés oxidativo dentro de las células
La hiperglucemia hace más que sólo bañar a las células con combustible extra: también provoca la sobreproducción de especies reactivas de oxígeno, moléculas inestables que dañan proteínas, lípidos y ADN. Este estrés oxidativo es un desencadenante clave para que los fibroblastos entren en senescencia. Los investigadores midieron varios indicadores estándar de este estrés en su modelo celular, incluidos subproductos dañinos y la actividad de las enzimas antioxidantes propias de la célula. Bajo glucosa alta, los fibroblastos mostraron más daño y defensas antioxidantes más débiles. Cuando se añadió aFGF, el equilibrio cambió: los marcadores dañinos disminuyeron y las enzimas protectoras se activaron más. Esto sugiere que el aFGF ayuda a restablecer un entorno interno más sano, reduciendo la probabilidad de que los fibroblastos caigan en un estado de envejecimiento irreversible.
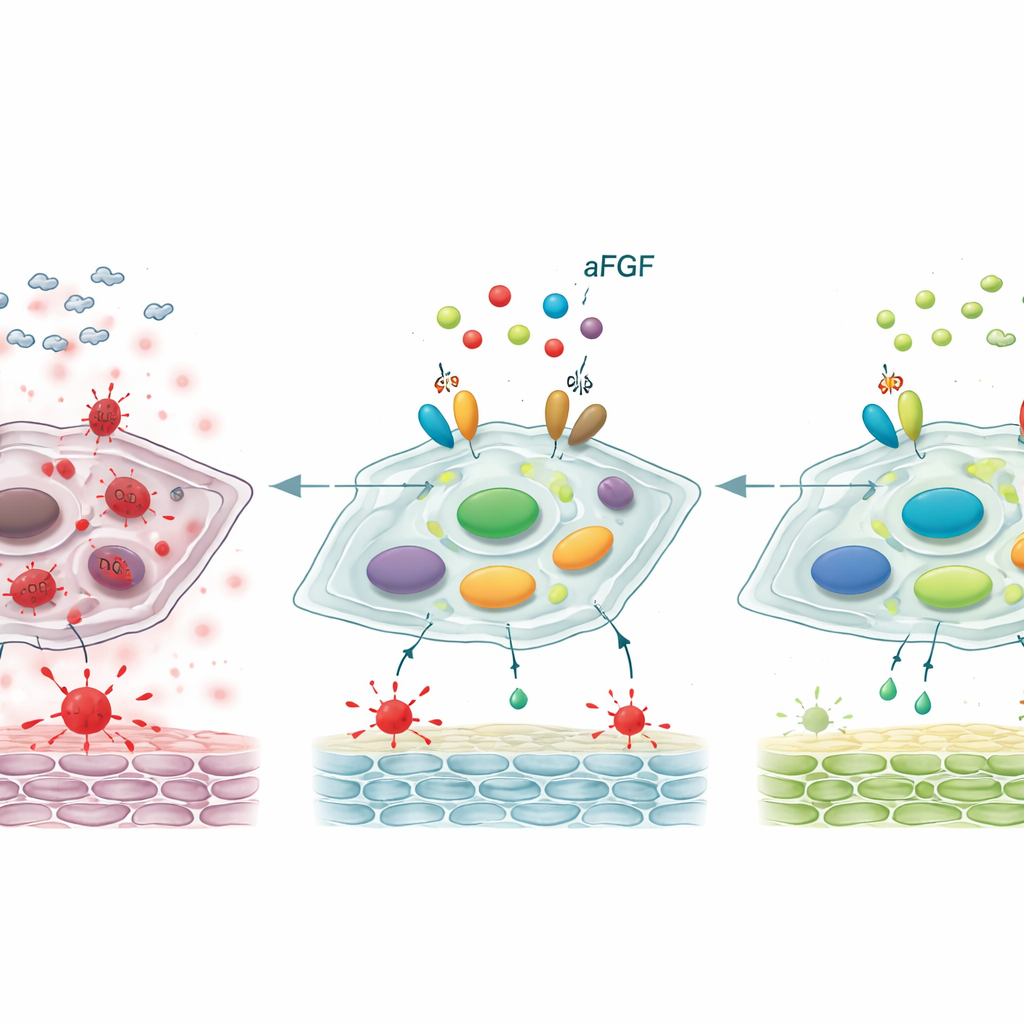
Reajustar un interruptor de control clave
Ahondando más, los científicos examinaron un eje de control molecular que involucra dos proteínas, SIRT1 y STAT3, que en conjunto influyen en si los fibroblastos se mantienen juveniles o se vuelven senescentes. En las heridas diabéticas y en las células tratadas con glucosa alta, los niveles de SIRT1, un guardián asociado con la resistencia al estrés, estaban reducidos, mientras que la forma activada de STAT3 —un impulsor del envejecimiento y del comportamiento inflamatorio— aumentaba. El tratamiento con aFGF invirtió este patrón: SIRT1 aumentó y STAT3 activado disminuyó. Cuando el equipo bloqueó SIRT1 con un inhibidor específico, el aFGF perdió en gran medida su capacidad para reducir el estrés oxidativo, atenuar los marcadores de envejecimiento y acelerar el cierre de las heridas en las ratas. Esto indica que los efectos beneficiosos del aFGF dependen en gran medida de reactivar SIRT1, que a su vez controla STAT3 y el dañino programa de envejecimiento que éste regula.
Qué podría significar para los pacientes
En conjunto, los hallazgos sugieren que el aFGF hace más que simplemente estimular el crecimiento celular. Parece rescatar a fibroblastos sobrecargados en heridas diabéticas de un ciclo destructivo de envejecimiento, aliviando el estrés oxidativo y reajustando un interruptor molecular clave para que estas células puedan nuevamente contribuir a la reconstrucción del tejido. Aunque el trabajo se realizó en ratas y en células en cultivo, y las heridas diabéticas reales son aún más complejas que los modelos usados aquí, los resultados señalan al aFGF como un candidato prometedor para tratamientos futuros. Si se confirman beneficios similares en humanos, una terapia con aFGF cuidadosamente dirigida podría algún día ayudar a que las úlceras diabéticas crónicas sanen más rápido, reduciendo el dolor, el riesgo de infección y la probabilidad de complicaciones graves.
Cita: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Palabras clave: cicatrización de heridas diabéticas, envejecimiento de los fibroblastos, estrés oxidativo, terapia con factores de crecimiento, vía SIRT1 STAT3