Clear Sky Science · es
Seguridad y eficacia preliminar de añadir tocilizumab a cisplatino/docetaxel para el tratamiento de pacientes con cáncer de mama triple negativo localmente avanzado: ensayo clínico prospectivo fase 1/2
Por qué este estudio importa a pacientes y familias
El cáncer de mama triple negativo es una de las formas más difíciles de tratar. Suele crecer rápido, vuelve con más frecuencia y carece de los “mangos” hormonales o del receptor HER2 que aprovechan muchos fármacos modernos. Este estudio investigó si añadir un fármaco inmunomodulador llamado tocilizumab, ya usado para la artritis y otras enfermedades inflamatorias, podría mejorar la eficacia y la seguridad de la quimioterapia estándar en personas con cáncer de mama triple negativo localmente avanzado en la mama y los ganglios linfáticos cercanos.
Un cáncer difícil con opciones limitadas
El cáncer de mama triple negativo representa solo aproximadamente una de cada cinco casos de cáncer de mama, pero causa una proporción desproporcionada de muertes porque es agresivo y tiene menos tratamientos dirigidos eficaces. Para muchos pacientes cuyos tumores son grandes o se han extendido a los ganglios linfáticos cercanos, la opción principal es una quimioterapia intensa administrada antes de la cirugía para reducir el tumor. Incluso con regímenes modernos que incluyen fármacos de platino como el cisplatino, un número significativo de pacientes conserva tumor residual tras el tratamiento, lo que se asocia con un mayor riesgo de recaída.
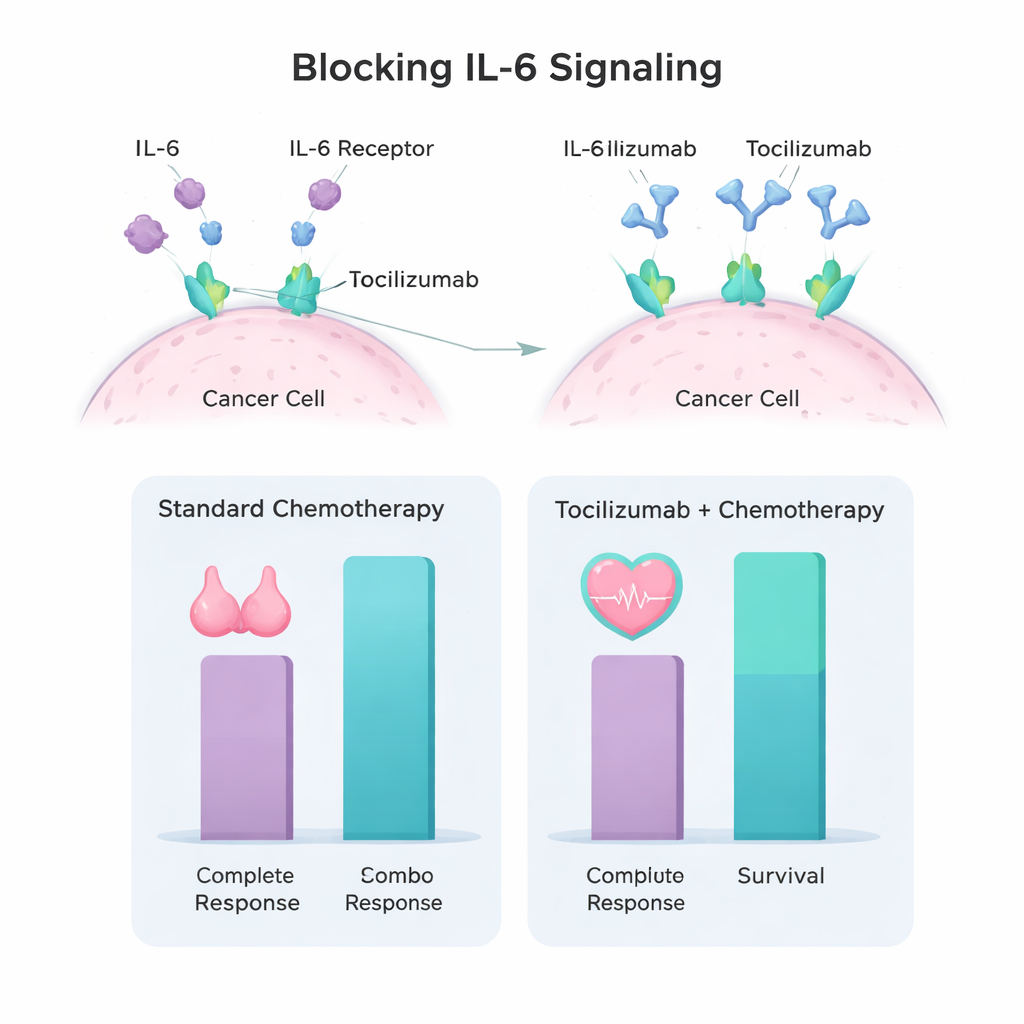
Apagar una señal dañina
Los científicos han descubierto que los tumores triple negativos y las células que los rodean a menudo producen altos niveles de una proteína señal llamada interleucina‑6 (IL‑6). La IL‑6 funciona como un mensaje constante de “crece y resiste el tratamiento” para el cáncer. El tocilizumab es un anticuerpo que bloquea el receptor de IL‑6, interrumpiendo esa señal. Estudios previos en laboratorio y en animales del mismo grupo demostraron que administrar tocilizumab antes de cisplatino hacía que las células del cáncer de mama triple negativo fueran más sensibles a la quimioterapia y ralentizaba el crecimiento tumoral. Estos hallazgos llevaron al equipo a diseñar un ensayo clínico en humanos de primera vez para evaluar si este enfoque era seguro y mostraba señales tempranas de beneficio en pacientes.
Cómo se llevó a cabo el ensayo
El estudio fue un ensayo fase 1/2 monocéntrico en Riad que incluyó a 30 mujeres con cáncer de mama triple negativo localmente avanzado (tamaño tumoral al menos 4 cm, sin diseminación a distancia). Todas las pacientes recibieron tocilizumab por vía intravenosa el día 1, seguido de cisplatino y docetaxel el día 2, cada cuatro semanas durante seis ciclos. La primera parte del ensayo utilizó un diseño estándar de escalada de dosis “3+3” para encontrar una dosis de quimioterapia segura para combinar con una dosis fija de tocilizumab. Una vez seleccionada esa dosis, más pacientes fueron tratados en una fase de expansión. Tras la quimioterapia, las pacientes pasaron a cirugía, y los patólogos examinaron cuidadosamente el tejido mamario y los ganglios linfáticos para determinar si quedaba cáncer invasivo. Los objetivos principales fueron evaluar la seguridad y medir cuántas pacientes lograban una respuesta patológica completa—es decir, ausencia detectable de cáncer invasivo en la mama o en los ganglios axilares.
Qué encontraron los investigadores
De las 30 pacientes incluidas, 28 completaron el tratamiento y 26 se sometieron a cirugía. El grupo era relativamente joven (edad mediana 42 años) y la mayoría presentaba enfermedad en estadio III y afectación ganglionar al inicio—características generalmente asociadas a peores resultados. En global, el 62% de las pacientes no presentaba cáncer invasivo residual tras el tratamiento, y el 81% no tenía cáncer en los ganglios linfáticos. Cuando se incluyeron las respuestas casi completas (pequeñas zonas residuales de tumor con ganglios limpios), el 81% de las pacientes encajaron en la categoría de respuesta completa o casi completa, y ninguna de estas pacientes tuvo recurrencia durante el periodo de seguimiento. Las pacientes portadoras de mutaciones hereditarias BRCA1 o BRCA2 obtuvieron resultados especialmente buenos: todas lograron respuesta completa. Los resultados de supervivencia temprana fueron alentadores, con una supervivencia libre de enfermedad estimada a tres años del 80% y una supervivencia global del 90%, a pesar de que muchas pacientes comenzaron con enfermedad local muy avanzada.
Efectos secundarios y seguridad
La seguridad fue un foco clave porque el régimen combinaba un biológico con quimioterapia intensiva. Entre las 28 pacientes evaluadas, no hubo muertes relacionadas con el tratamiento. Los efectos secundarios leves a moderados más comunes fueron náuseas, dolor en articulaciones y músculos, vómitos, diarrea, erupción cutánea y cambios temporales en las cifras sanguíneas. Los eventos más serios incluyeron neutropenia y fiebre, elevaciones de enzimas hepáticas e incrementos significativos pero controlables del colesterol y los triglicéridos—cambios conocidos con tocilizumab y manejados con medicación estándar. Solo unas pocas pacientes necesitaron reducciones de dosis de quimioterapia, y los problemas renales por cisplatino fueron raros y reversibles, lo que sugiere que la combinación en conjunto era tolerable.
Qué podría significar esto en el futuro
Para pacientes y familias frente al cáncer de mama triple negativo, estos resultados tempranos sugieren que añadir un fármaco que bloquea IL‑6 antes de la quimioterapia estándar puede aumentar de forma sustancial las probabilidades de no encontrar cáncer en la cirugía, especialmente en personas con mutaciones BRCA, y hacerlo sin añadir efectos secundarios peligrosos. Sin embargo, el estudio fue pequeño, realizado en un solo centro y no permitió ciertos tratamientos complementarios modernos para pacientes con enfermedad residual. El tocilizumab también se suspendió tras la cirugía, por lo que los beneficios a más largo plazo aún deben definirse completamente. Serán necesarios ensayos aleatorizados más amplios para confirmar si este enfoque debe incorporarse a la práctica estándar, pero este trabajo abre una vía prometedora: dirigir señales inflamatorias dentro y alrededor del tumor para ayudar a que la quimioterapia existente actúe con más fuerza y precisión contra un cáncer muy difícil de tratar.
Cita: Al-Tweigeri, T., Tulbah, A., Akhtar, S. et al. Safety and preliminary efficacy of adding tocilizumab to cisplatin/docetaxel for the treatment of locally advanced triple-negative breast cancer patients: prospective phase 1/2 clinical trial. Sci Rep 16, 7029 (2026). https://doi.org/10.1038/s41598-026-38465-z
Palabras clave: cáncer de mama triple negativo, tocilizumab, bloqueo de IL-6, quimioterapia neoadyuvante, respuesta patológica completa