Clear Sky Science · es
Akkermansia muciniphila afecta la colitis al inhibir la vía de señalización de la ferroptosis
Por qué importa un diminuto habitante intestinal
Los problemas intestinales crónicos, como la colitis ulcerosa, pueden convertir actos cotidianos —comer, ir al baño— en experiencias dolorosas. Los médicos saben que tanto el sistema inmunitario como los microbios intestinales participan, pero los detalles siguen emergiendo. Este estudio se centra en una bacteria en particular, Akkermansia muciniphila, y plantea una pregunta simple pero crucial: ¿puede este microbio proteger el intestino bloqueando una forma de daño celular impulsada por el hierro? La respuesta podría abrir la puerta a nuevos tratamientos basados en bacterias para la enfermedad inflamatoria intestinal.
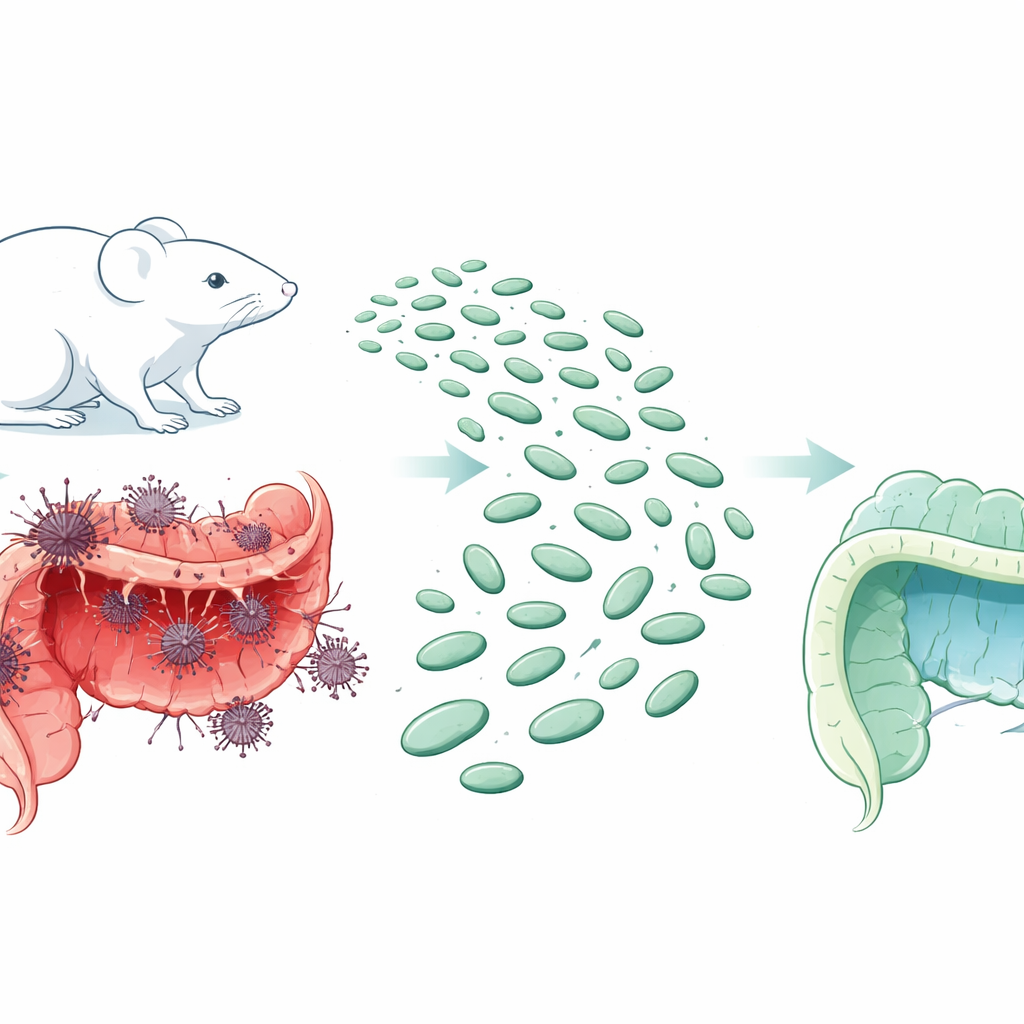
Un revestimiento delicado bajo ataque
La colitis se caracteriza por hinchazón y daño en el intestino grueso. La pared interna, normalmente formada por células compactas y células caliciformes productoras de mucosidad, se erosiona y se vuelve permeable. En este estudio con ratones, los investigadores provocaron colitis con un químico que imita muchas características de la enfermedad humana: pérdida de peso, diarrea, sangrado y daño generalizado en el revestimiento del colon. Al microscopio, el equipo observó adelgazamiento de las capas tisulares, pérdida de vellosidades en forma de dedos, reducción de células caliciformes e infiltración de células inflamatorias, todos signos de que la barrera intestinal se estaba rompiendo.
El daño celular impulsado por el hierro como culpable oculto
Los investigadores se centraron en la «ferroptosis», un tipo de muerte celular reconocido recientemente en el que el hierro alimenta la acumulación de lípidos oxidados tóxicos en las membranas celulares. En el modelo de colitis encontraron niveles altos de marcadores de estrés oxidativo, como especies reactivas de oxígeno y productos de degradación de lípidos dañados, junto con exceso de hierro en el tejido del colon. Al mismo tiempo, las proteínas protectoras que normalmente defienden a las células contra este daño estaban reducidas, mientras que aumentaba una proteína que favorece el daño lipídico. Cuando el equipo administró a los ratones un fármaco que potencia específicamente la ferroptosis, las lesiones del colon empeoraron aún más, lo que sugiere que el daño de membrana impulsado por el hierro no solo está presente, sino que intensifica activamente la colitis.
Interviene una bacteria beneficiosa
Mediante estudios genéticos del microbioma intestinal, los científicos observaron que la abundancia de Akkermansia muciniphila disminuyó drásticamente en la colitis. Luego administraron por vía oral dosis de esta bacteria a algunos ratones enfermos durante varias semanas. Estos animales perdieron menos peso, presentaron heces más firmes con menos sangrado y mostraron un tejido del colon mucho más sano en las tinciones. La superficie intestinal se veía más íntegra, con estructuras criptales mejor preservadas y capas musculares más organizadas. La microscopía electrónica reveló que los ratones tratados tenían mitocondrias con apariencia más normal y menos signos de colapso estructural. Las pruebas químicas mostraron que el hierro, las especies reactivas de oxígeno y los marcadores de daño lipídico disminuyeron tras el tratamiento con Akkermansia, mientras que las proteínas protectoras clave contra la ferroptosis aumentaron de nuevo. Incluso cuando se administró el fármaco que potencia la ferroptosis, Akkermansia revirtió en parte sus efectos nocivos sobre el revestimiento intestinal.
Cambios en la química y los genes intestinales
Para entender cómo ejerce su efecto protector esta bacteria, el equipo examinó tanto la actividad génica en el tejido del colon como las pequeñas moléculas producidas en el intestino. La colitis alteró de forma dramática la actividad de cientos de genes vinculados a la inflamación, el metabolismo y la supervivencia celular. El tratamiento con Akkermansia corrigió muchas de estas alteraciones hacia niveles más normales, sobre todo genes implicados en la adhesión celular y las respuestas al estrés. En el ámbito metabólico, la bacteria aumentó ácidos grasos de cadena corta beneficiosos y varios compuestos relacionados con aminoácidos, mientras que redujo ciertos alcoholes y fenoles que pueden irritar el intestino. Al superponer los datos de genes y metabolitos, encontraron 19 rutas biológicas afectadas conjuntamente, muchas relacionadas con el manejo de lípidos y la peroxidación —los mismos procesos que alimentan la ferroptosis. Este patrón sugiere que Akkermansia ayuda a calmar la colitis en parte al remodelar tanto la química intestinal como la respuesta genética del colon al estrés.
Qué podría significar esto para los pacientes
En conjunto, el estudio muestra que restaurar una sola bacteria benigna puede aliviar la colitis en ratones al reforzar la barrera intestinal y reducir el daño de membrana impulsado por el hierro dentro de las células intestinales. Aunque este trabajo aún está en fase preclínica y de laboratorio, apunta a un futuro en el que microbios dirigidos o sus metabolitos podrían complementar los fármacos actuales para la enfermedad inflamatoria intestinal. Al frenar la ferroptosis y restaurar una química intestinal más saludable, tales enfoques podrían ayudar a proteger el frágil revestimiento del intestino y reducir los brotes dolorosos en personas que viven con colitis crónica.
Cita: Zhang, L., Liu, Y., Wei, K. et al. Akkermansia muciniphila affects colitis by inhibiting ferroptosis signaling pathway. Sci Rep 16, 9250 (2026). https://doi.org/10.1038/s41598-026-38452-4
Palabras clave: colitis ulcerosa, microbioma intestinal, Akkermansia muciniphila, ferroptosis, inflamación intestinal