Clear Sky Science · es
Explorando los perfiles subyacentes de expresión génica en fenotipos de diferencias del desarrollo sexual mediante análisis del transcriptoma
Por qué esta investigación nos importa a todos
La mayoría aprendemos en la escuela que el sexo biológico se determina de forma simple y dicotómica: cromosomas XX forman ovarios, cromosomas XY forman testículos. Este estudio cuestiona esa imagen ordenada. Al leer qué genes están encendidos o apagados en las gónadas de personas con diferencias del desarrollo sexual (DSD), los investigadores descubren una historia más rica en la que el desarrollo sexual humano se parece menos a un interruptor y más a un espectro. Su trabajo ofrece una ventana sobre cómo se forman los cuerpos, por qué algunas personas no encajan en las categorías típicas de hombre o mujer y cómo la medicina podría entenderlas y cuidarlas mejor.
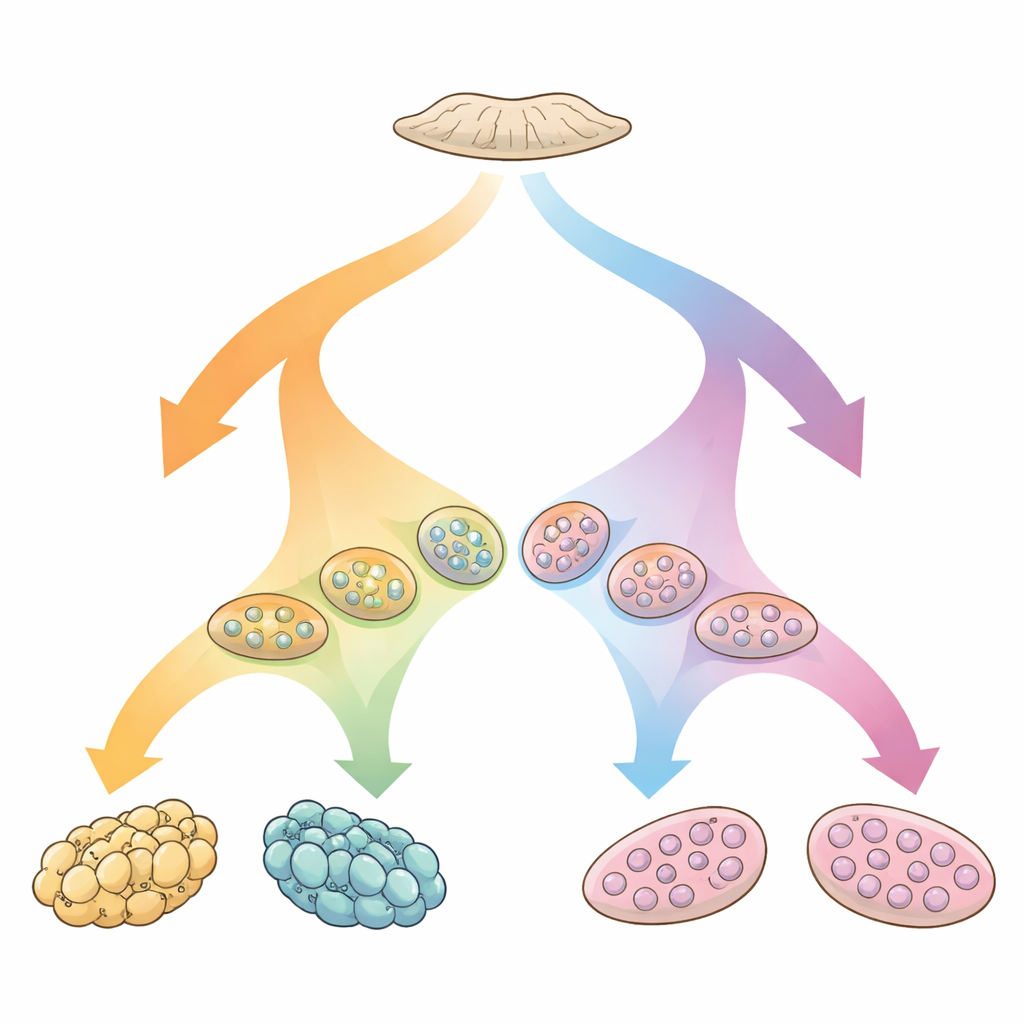
Un punto de partida flexible en la vida temprana
Las gónadas comienzan la vida como una estructura flexible “bipotente” que puede convertirse en testículos u ovarios. Una red de genes y señales empuja suavemente ese tejido temprano en una u otra dirección, acabando por conformar la producción hormonal y la anatomía visible. Cuando cualquiera de las partes de esta red se altera, el resultado puede ser una DSD, en la que cromosomas, gónadas y anatomía no coinciden de la manera habitual. Muchas de estas condiciones siguen sin explicación a nivel del ADN. El equipo de este estudio razonó que observar directamente la actividad génica dentro del tejido gonadal podría revelar patrones que las pruebas genéticas clásicas pasan por alto, arrojando luz sobre cómo estos órganos realmente eligen, o no logran elegir, un camino.
Escuchando a los genes gonadales
Los investigadores analizaron tejido gonadal de 11 personas con distintas condiciones DSD: disgenesia gonadal parcial, insensibilidad completa a los andrógenos y una forma llamada DSD ovotesticular, en la que una persona presenta tejido tanto tipo testicular como ovárico. Empleando secuenciación de ARN, midieron los niveles de actividad de decenas de miles de genes y compararon esos patrones con datos de referencia de testículos y ovarios sanos en etapas fetales, infantiles y adultas. Un método de visualización que agrupa muestras por similitud en genes clave del desarrollo sexual mostró que las muestras DSD no encajaban limpiamente en los clústeres masculinos o femeninos. En su lugar, ocuparon una zona intermedia, formando su propio grupo entre testículos y ovarios típicos. Algunas muestras se situaron más cerca del grupo testicular, otras más próximas al ovárico, lo que sugiere un rango graduado de identidades gonadales.
Señales mixtas dentro de las gónadas
Cuando el equipo se centró en genes bien conocidos que dirigen las gónadas hacia testículo u ovario, encontró que estas “señales” a menudo se salían de sus rangos habituales. En individuos 46,XY con disgenesia gonadal parcial o insensibilidad a los andrógenos, genes necesarios para un desarrollo testicular sano y la producción de esperma estaban atenuados, y genes de desarrollo más generales estaban aumentados, consistente con una formación testicular detenida o incompleta. En personas 46,XX con DSD ovotesticular, el panorama fue aún más mixto: genes que normalmente impulsan el desarrollo testicular estaban parcialmente activados, mientras que varios genes asociados al ovario estaban reducidos. Un análisis de vías a gran escala reflejó este patrón. Procesos específicos del testículo, como la formación de espermatozoides, la división celular y el metabolismo energético, se vieron debilitados en muchos casos 46,XY, mientras que los casos 46,XX ovotesticulares mostraron activación simultánea de vías relacionadas tanto con el testículo como con el ovario, en consonancia con las estructuras mixtas observadas al microscopio.
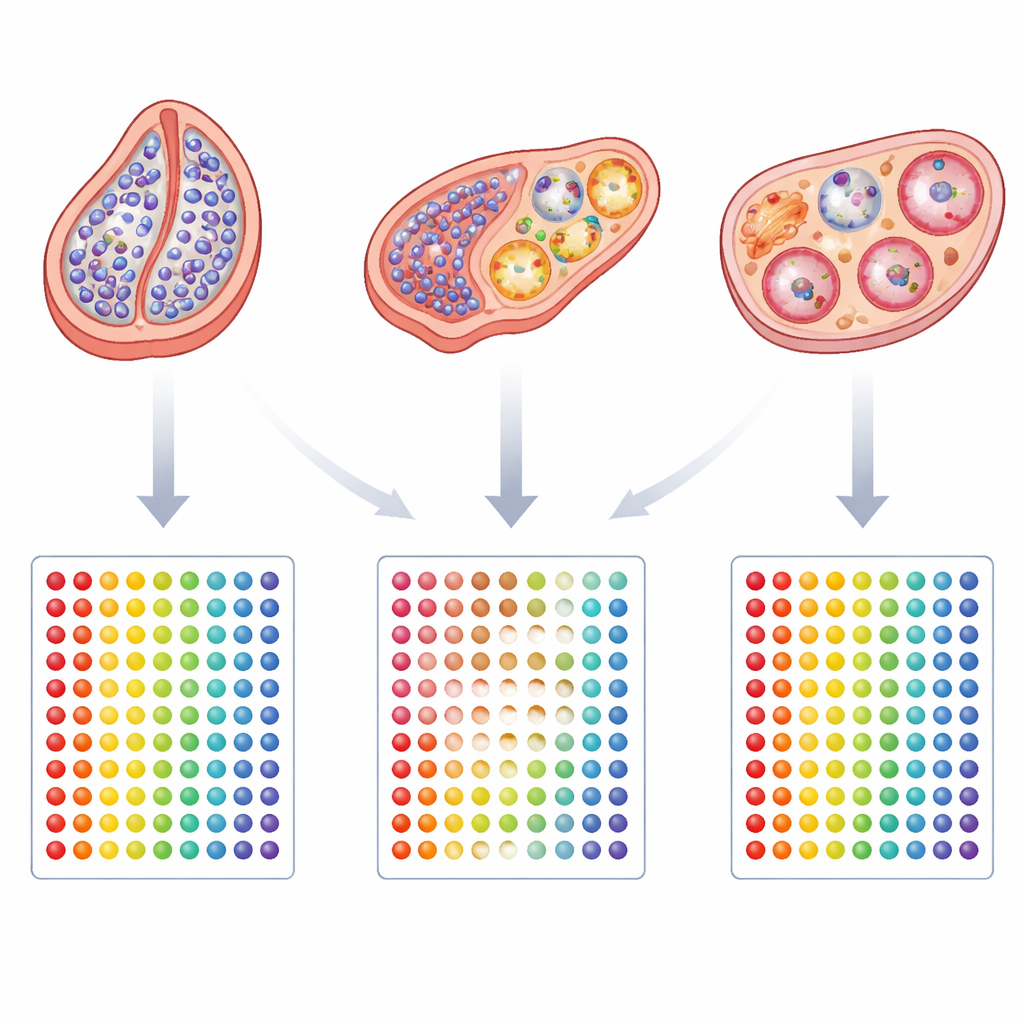
Un tema común entre distintas condiciones
A pesar de la diversidad de presentaciones clínicas, emergió una característica recurrente: la disminución de la actividad de un gen llamado CBX2, que ayuda a organizar el empaquetamiento del ADN y controla grandes conjuntos de genes determinantes del sexo. Experimentos en animales ya habían demostrado que alterar este regulador puede difuminar la frontera entre el desarrollo testicular y ovárico. Su regulación a la baja consistente en todos los grupos DSD sugiere que la inestabilidad en este nivel regulatorio puede favorecer que las gónadas se alejen de una identidad clara de testículo u ovario y se sitúen en un punto intermedio. El estudio también destaca que algunos pacientes más jóvenes aún muestran señales de flexibilidad del desarrollo, con señales más fuertes en vías de crecimiento y de células germinales tempranas que los adultos, lo que insinúa que el momento puede influir en cuán firmemente se fija el destino gonadal.
Repensando el interruptor simple
Para un observador no especializado, esta investigación indica que las gónadas humanas no se limitan a conmutar entre dos ajustes fijos. En su lugar, siguen un espectro de patrones de actividad génica que pueden situarse en estados fuertemente testiculares, fuertemente ováricos o intermedios. Para las personas con DSD, esto significa que lo que importa biológicamente no son solo los cromosomas que portan o la apariencia externa de su cuerpo, sino también cómo se ha desarrollado su tejido gonadal a nivel molecular. Al mapear esos paisajes internos, el estudio aboga por ir más allá de una visión estrictamente binaria del desarrollo sexual y por añadir pruebas basadas en ARN junto con la secuenciación del ADN en futuros protocolos clínicos. Al hacerlo, ofrece una comprensión más matizada y fundamentada en la biología del sexo que se ajusta mejor a la diversidad real observada en los pacientes.
Cita: Fabbri-Scallet, H., Calonga-Solís, V., Guerra-Júnior, G. et al. Exploring the underlying gene expression profiles of differences of sex development phenotypes through transcriptome analysis. Sci Rep 16, 8801 (2026). https://doi.org/10.1038/s41598-026-38435-5
Palabras clave: espectro del desarrollo sexual, transcriptoma gonadal, diferencias del desarrollo sexual, perfilado de expresión génica, DSD ovotesticular