Clear Sky Science · es
Descubrimiento in silico de un inhibidor multitarget derivado de compuestos naturales para la terapia de la enfermedad de Huntington
Un nuevo enfoque para una enfermedad cerebral devastadora
La enfermedad de Huntington es un trastorno cerebral raro pero devastador que, de forma progresiva, priva a las personas de movimiento, capacidades cognitivas e independencia. Los medicamentos disponibles hoy pueden aliviar algunos síntomas, pero no detienen ni revierten la enfermedad. Este estudio explora una nueva vía impulsada por ordenador para buscar tratamientos, buscando un único compuesto natural que pueda actuar sobre varios puntos débiles del proceso patológico a la vez —un enfoque que podría ser más eficaz que los fármacos dirigidos a un solo objetivo.
Por qué la enfermedad de Huntington es tan difícil de tratar
La enfermedad de Huntington se debe a un gen defectuoso que provoca la degeneración gradual de las neuronas, por lo general a partir de la mediana edad. Al principio, las personas pueden notar cambios sutiles en el estado de ánimo, pequeños movimientos involuntarios o leves dificultades en la planificación y la atención. En el transcurso de 10 a 12 años, esto puede evolucionar hasta graves problemas de movimiento, pérdida del habla, demencia y dependencia total de cuidadores. Los científicos saben que muchas cosas fallan dentro de las células cerebrales en la enfermedad de Huntington: la producción de energía se deteriora, las proteínas dañinas se agregan y las señales químicas entre células se vuelven tóxicas. Debido a que tantos procesos están alterados a la vez, la estrategia de “una proteína, un fármaco” ha tenido dificultades para producir avances reales.
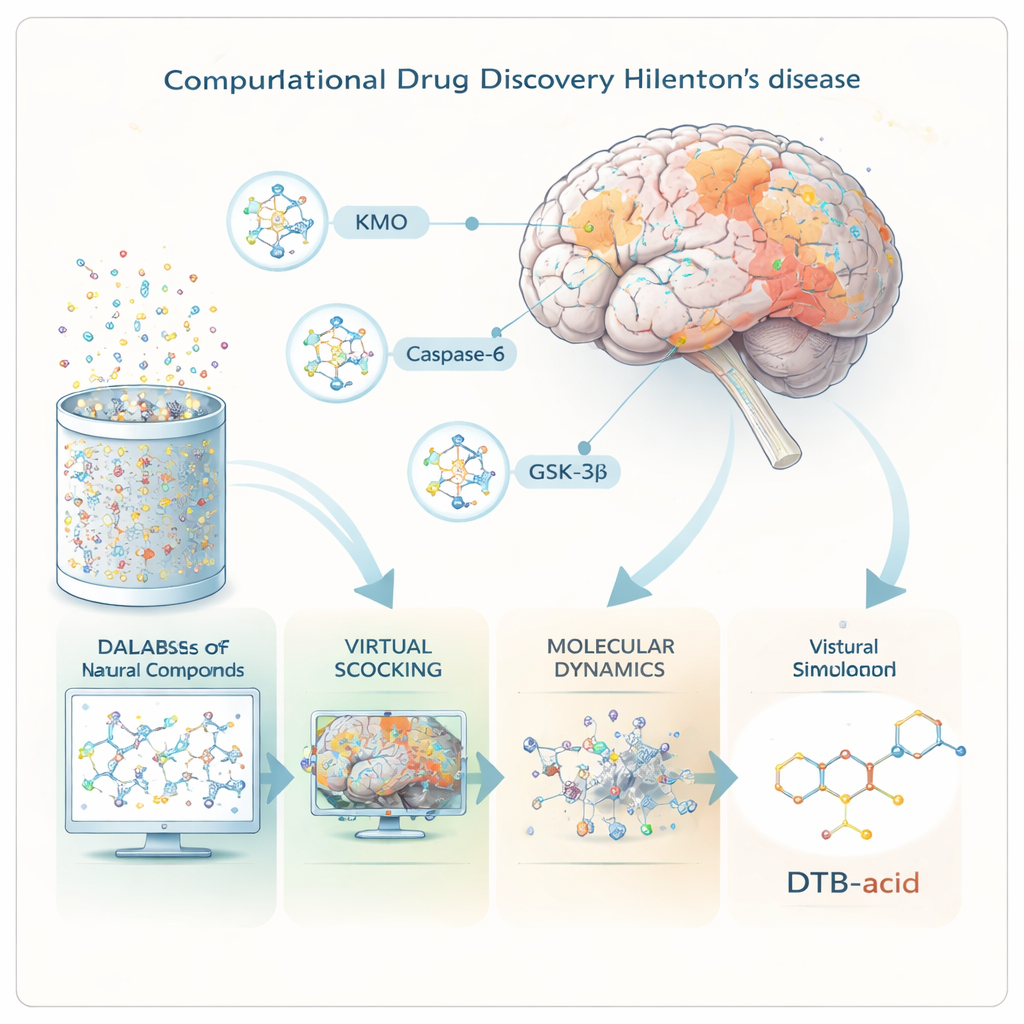
Tres puntos críticos de presión en el cerebro
Los investigadores se centraron en tres proteínas que ocupan puntos de control clave en la enfermedad de Huntington. La primera, KMO, orienta la degradación del aminoácido triptófano hacia subproductos tóxicos o protectores; cuando este equilibrio se inclina hacia los tóxicos, las neuronas sufren. La segunda, caspasa‑6, corta la proteína huntingtina mutante en fragmentos más pequeños y altamente tóxicos que se acumulan en las etapas tempranas de la enfermedad. La tercera, GSK‑3β, es una enzima de señalización asociada a ovillos proteicos anómalos y muerte celular en varios trastornos cerebrales. Al encontrar una molécula que pueda reducir simultáneamente la actividad perjudicial de las tres, el equipo esperaba diseñar una terapia mejor adaptada a la complejidad de la enfermedad.
Cribado de la biblioteca de la naturaleza con superordenadores
En lugar de mezclar químicos en tubos de ensayo, los científicos trabajaron completamente “in silico”, usando software avanzado para modelar el comportamiento de las moléculas. Comenzaron con más de 695.000 compuestos naturales extraídos de una base de datos pública, preparando cada uno en forma tridimensional. Potentes herramientas de cribado virtual predijeron qué compuestos tenían más probabilidades de atravesar la barrera sangre‑cerebro, comportarse como fármacos reales en el organismo y evitar problemas de seguridad importantes. Solo alrededor de 60.000 superaron estos filtros y se probaron, en el ordenador, para ver qué tan bien podrían encajar en las cavidades de unión de las tres proteínas objetivo.
Una molécula destacada: DTB‑ácido
De esta búsqueda masiva, una molécula —llamada DTB‑ácido, un alcaloide natural relacionado con el ácido matrínico— emergió como la mejor candidata. Estudios de acoplamiento detallados mostraron que DTB‑ácido podía formar contactos fuertes y bien situados dentro de las tres proteínas. A continuación, el equipo realizó largas simulaciones de dinámica molecular, que imitan cómo se mueven los átomos en agua a lo largo del tiempo, para comprobar si el compuesto se mantendría estable en lugar de desplazarse. A lo largo de 100 milmillonésimas de segundo de movimiento simulado, los complejos proteína‑fármaco permanecieron estables. Cálculos energéticos adicionales sugirieron que la unión a KMO era especialmente fuerte, mientras que un análisis separado de las moléculas de agua en los sitios de unión indicó que las interacciones con GSK‑3β también eran termodinámicamente favorables.
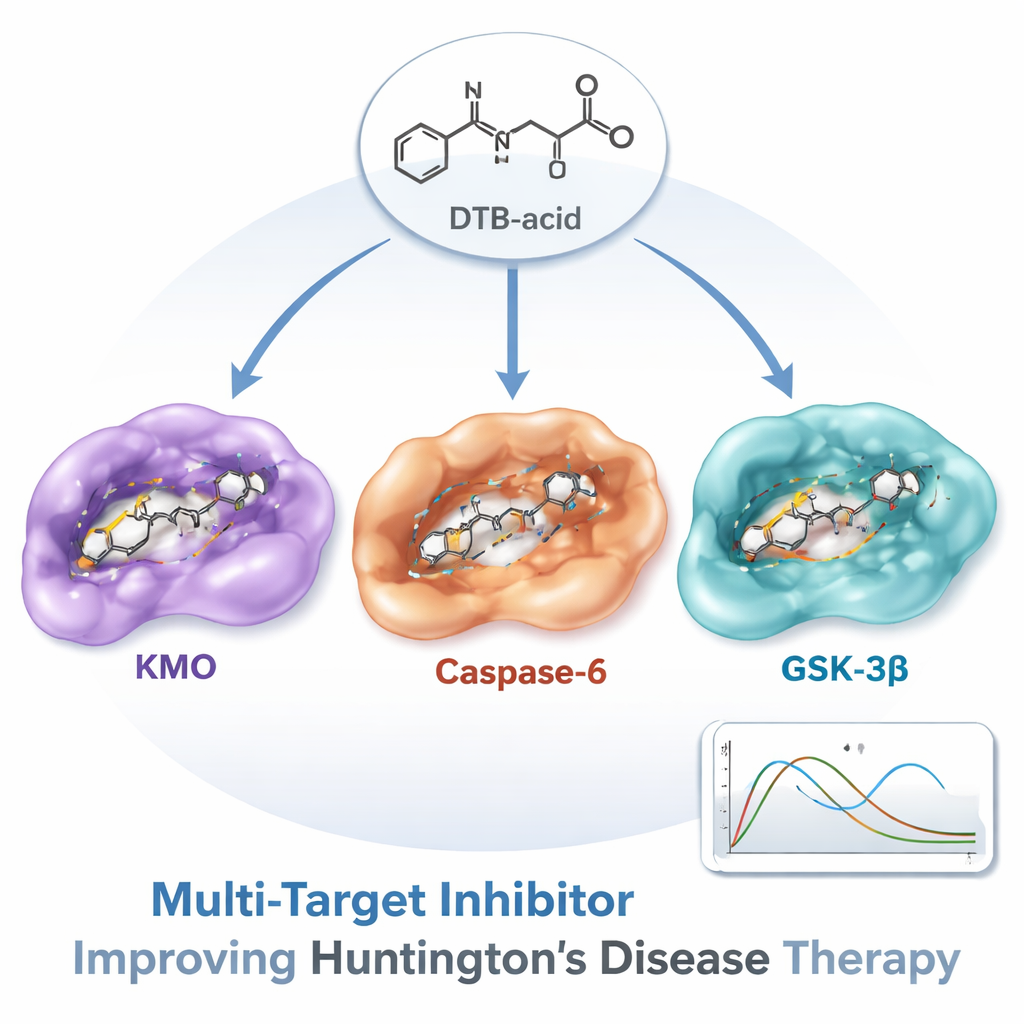
Del hallazgo computacional a un futuro medicamento
Por supuesto, una molécula que parece prometedora en una pantalla es solo un primer paso. Los autores enfatizan que DTB‑ácido aún debe probarse en células y en animales para confirmar que llega al cerebro, alcanza sus objetivos previstos y realmente protege a las neuronas sin efectos secundarios perjudiciales. Aun así, este trabajo demuestra una vía potente y eficiente para descubrir fármacos multitarget para enfermedades cerebrales complejas. Para los no especialistas, el mensaje clave es que, en lugar de tratar la enfermedad de Huntington con una serie de fármacos separados y de enfoque estrecho, puede ser posible diseñar un compuesto cuidadosamente ajustado como DTB‑ácido que ataque varios factores causantes del daño a la vez —ofreciendo una nueva esperanza para frenar o alterar el curso de este trastorno implacable.
Cita: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
Palabras clave: Enfermedad de Huntington, fármaco multitarget, descubrimiento computacional de fármacos, compuestos naturales, neurodegeneración