Clear Sky Science · es
Cribado integrado de múltiples conjuntos de datos para predecir el pronóstico e identificar genes diana de inmunoterapia en pacientes con carcinoma hepatocelular
Por qué importa esto para las personas con cáncer de hígado
El carcinoma hepatocelular, la forma más común de cáncer primario de hígado, causa la muerte de cientos de miles de personas cada año. Muchos pacientes con el mismo estadio de enfermedad responden de forma muy distinta al tratamiento, especialmente a las inmunoterapias modernas que buscan aprovechar el propio sistema inmune del cuerpo. Este estudio plantea una pregunta simple pero crucial: ¿podemos leer la actividad génica de un tumor como si fuera una huella dactilar para predecir quién tendrá un mal pronóstico, quién responderá a fármacos inmunitarios y qué genes podrían ser las mejores dianas terapéuticas nuevas?
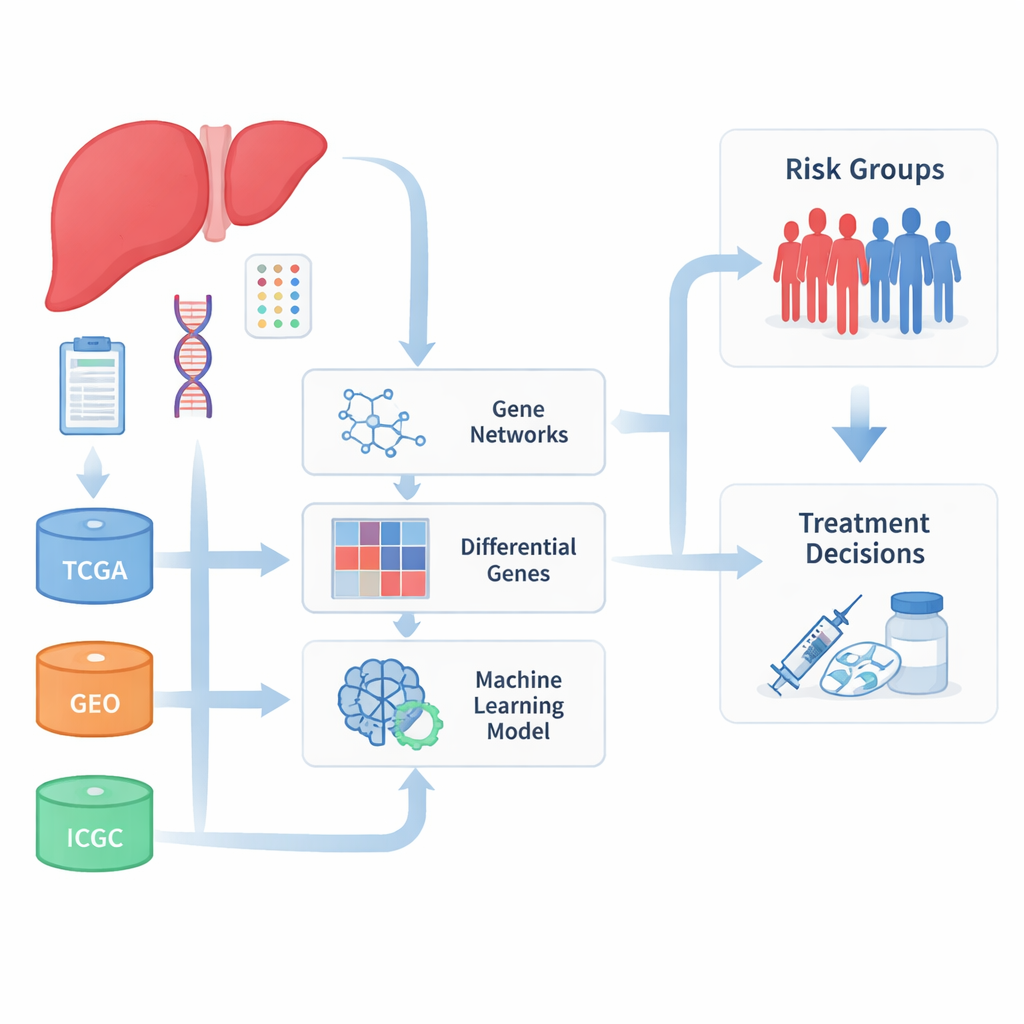
Reuniendo muchos conjuntos de datos
Los investigadores comenzaron agrupando grandes colecciones de muestras de cáncer de hígado procedentes de varias bases de datos internacionales que almacenan la actividad génica tumoral y los resultados clínicos. Al combinar datos de The Cancer Genome Atlas, el International Cancer Genome Consortium y múltiples estudios del Gene Expression Omnibus, ensamblaron un conjunto de pacientes mucho mayor y más diverso que el que podría aportar cualquier hospital o proyecto individual. Dado que estos conjuntos de datos se produjeron en distintos laboratorios y con métodos diferentes, el equipo empleó primero un esfuerzo considerable en corregir las diferencias técnicas para que fuesen las señales biológicas reales, y no el ruido de laboratorio, las que impulsaran sus resultados.
Encontrando patrones génicos ligados al resultado
Con los datos depurados en mano, el equipo buscó grupos de genes que tendieran a activarse y desactivarse juntos y que además se asociaran con el devenir de los pacientes. Usando un enfoque de tipo red, agruparon miles de genes en módulos y luego se centraron en aquellos módulos más fuertemente vinculados al comportamiento tumoral y a la supervivencia de los pacientes. También compararon tumores con tejido no tumoral para encontrar genes claramente más o menos activos en el cáncer. La intersección entre estas dos perspectivas produjo un conjunto de 93 genes que estaban alterados en el carcinoma hepatocelular y conectados de forma estrecha con características clave de la enfermedad, muchas relacionadas con cómo el hígado procesa fármacos y maneja sustancias tóxicas.
Construyendo una puntuación de riesgo de diez genes
Para convertir estas listas de genes en algo que los médicos pudieran usar en el futuro, los autores recurrieron al aprendizaje automático. Probaron más de cien combinaciones de algoritmos de selección de características y de predicción de supervivencia, evaluándolos por la precisión con la que separaban a los pacientes en grupos de mejor y peor pronóstico en múltiples cohortes independientes. De esta extensa búsqueda destilaron una firma compacta de diez genes que, en conjunto, formaron una puntuación de riesgo. Los pacientes con puntuaciones altas mostraron de forma consistente una supervivencia global, libre de enfermedad y libre de progresión más corta, tanto en los conjuntos de datos principales como en grupos de validación externos. Entre estos genes, TYMS destacó como un fuerte indicador de mal pronóstico, mientras que APOL3 y FBXO2 se asociaron con resultados más favorables.
Pistas desde el vecindario inmune del tumor
El estudio fue más allá de la predicción para preguntar por qué importan estos genes. Usando varias herramientas computacionales, el equipo estimó qué tipos de células inmunitarias estaban presentes en cada tumor y en qué medida la puntuación de diez genes se relacionaba con ese paisaje inmunológico. Los tumores de alto riesgo tendieron a mostrar patrones inmunes y cambios génicos asociados con más mutaciones y con signos de escape inmune, incluyendo vínculos con moléculas de control bien conocidas como PD-1 y CTLA-4. También examinaron los perfiles reales de mutación y encontraron que los tumores de alto riesgo presentaban con mayor frecuencia alteraciones en oncogenes clásicos como TP53. Finalmente, análisis de sangre en pacientes y voluntarios sanos confirmaron que TYMS estaba elevado y FBXO2 reducido en personas con cáncer de hígado, lo que respalda la idea de que estos genes están biológicamente activos en la enfermedad y no son solo artefactos estadísticos.
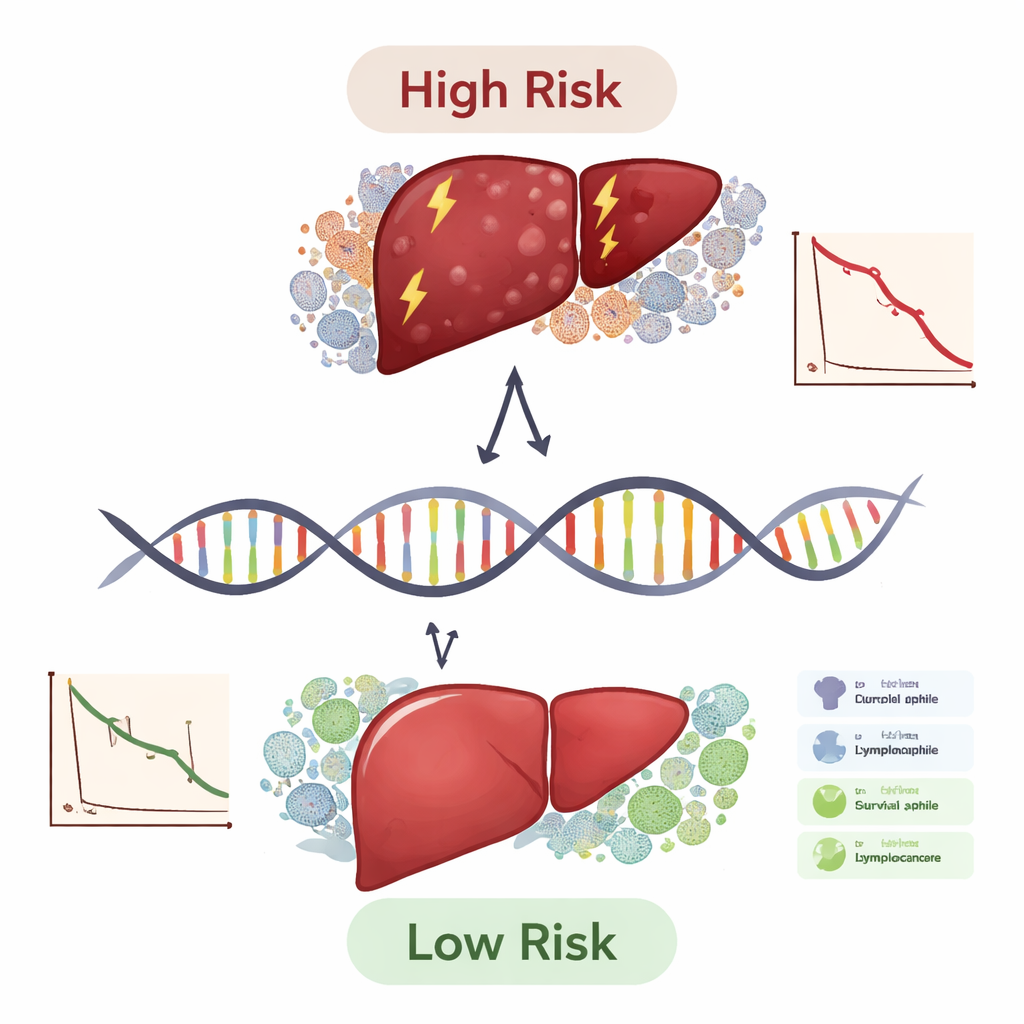
Qué significa esto para pacientes y médicos
En términos prácticos, este trabajo ofrece un plan para utilizar un panel pequeño de genes que clasifique a los pacientes con cáncer de hígado en grupos de riesgo y sugiera quién podría beneficiarse más de tratamientos basados en el sistema inmune. La puntuación de diez genes aún no es una prueba lista para la clínica, pero superó a los sistemas de estadificación habituales por sí solos y se mantuvo útil en distintos subgrupos de pacientes. Así como los paneles de colesterol orientan la prevención de enfermedades cardiovasculares, un panel génico como este podría algún día ayudar a los oncólogos a elegir terapias más agresivas para pacientes de alto riesgo, ahorrar a los de bajo riesgo efectos secundarios innecesarios y señalar a los desarrolladores de fármacos nuevas dianas como TYMS, APOL3 y FBXO2. Serán necesarios estudios prospectivos más amplios y experimentos de laboratorio, pero este análisis integrado marca un paso significativo hacia una atención del cáncer de hígado más personalizada y guiada por la biología.
Cita: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
Palabras clave: carcinoma hepatocelular, firma génica, inmunoterapia, pronóstico, microambiente tumoral