Clear Sky Science · es
La señalización CNOT2 / c-Myc / STAT3 participa de forma crítica en la apoptosis mediada por glucólisis del isotiocianato de bencilo en el carcinoma hepatocelular
Un ingrediente anticáncer en tu plato
El isotiocianato de bencilo, o BITC por sus siglas en inglés, es un compuesto natural que se encuentra en verduras conocidas como el brócoli, la col y la col rizada. Aunque los médicos llevan tiempo observando que las personas que consumen más de estos alimentos tienden a tener tasas más bajas de cáncer, aún se están descifrando los mecanismos por los que ingredientes vegetales concretos frenan o matan células cancerosas. Este estudio investiga cómo afecta el BITC a células de cáncer de hígado en el laboratorio y revela un vínculo sorprendente entre la forma en que las células cancerosas queman azúcar y cómo son empujadas a autodestruirse.
Por qué el cáncer de hígado necesita mejores opciones
El cáncer de hígado es uno de los más mortales en todo el mundo, y el carcinoma hepatocelular es su forma más común. Incluso con cirugía, quimioterapia y fármacos dirigidos, muchos tumores vuelven a aparecer o dejan de responder al tratamiento. Una razón es que las células cancerosas reconfiguran cómo usan la energía: en lugar de depender principalmente del oxígeno en sus centrales energéticas (mitocondrias), queman grandes cantidades de azúcar muy deprisa en un proceso a menudo llamado «efecto Warburg». Este uso desviado de la glucosa ayuda a las células cancerosas a crecer más rápido y a resistir la muerte. Encontrar maneras seguras de interrumpir este suministro de energía, sobre todo con moléculas derivadas de alimentos, es una estrategia atractiva.
Probando un compuesto vegetal en células de cáncer de hígado
Los investigadores trataron dos líneas celulares humanas de carcinoma hepatocelular, SK-Hep1 y Huh7, con dosis crecientes de BITC. A medida que la dosis aumentó, menos células sobrevivieron, lo que demuestra que el BITC es tóxico para las células de cáncer de hígado en estas condiciones. Al examinar más de cerca lo que ocurría dentro de las células, observaron signos clásicos de muerte celular programada, o apoptosis. Proteínas clave que normalmente existen en forma «inactiva» antes de ser cortadas durante la apoptosis, como PARP y caspasa-3, disminuyeron en sus formas intactas o «pro-». Pruebas de citometría de flujo también mostraron más células en la fracción sub-G1 del ciclo celular y más células positivas para Annexina V, ambos indicios de que las células cancerosas estaban sufriendo apoptosis activamente en lugar de estar simplemente dañadas.
Apagando el apetito de azúcar del cáncer
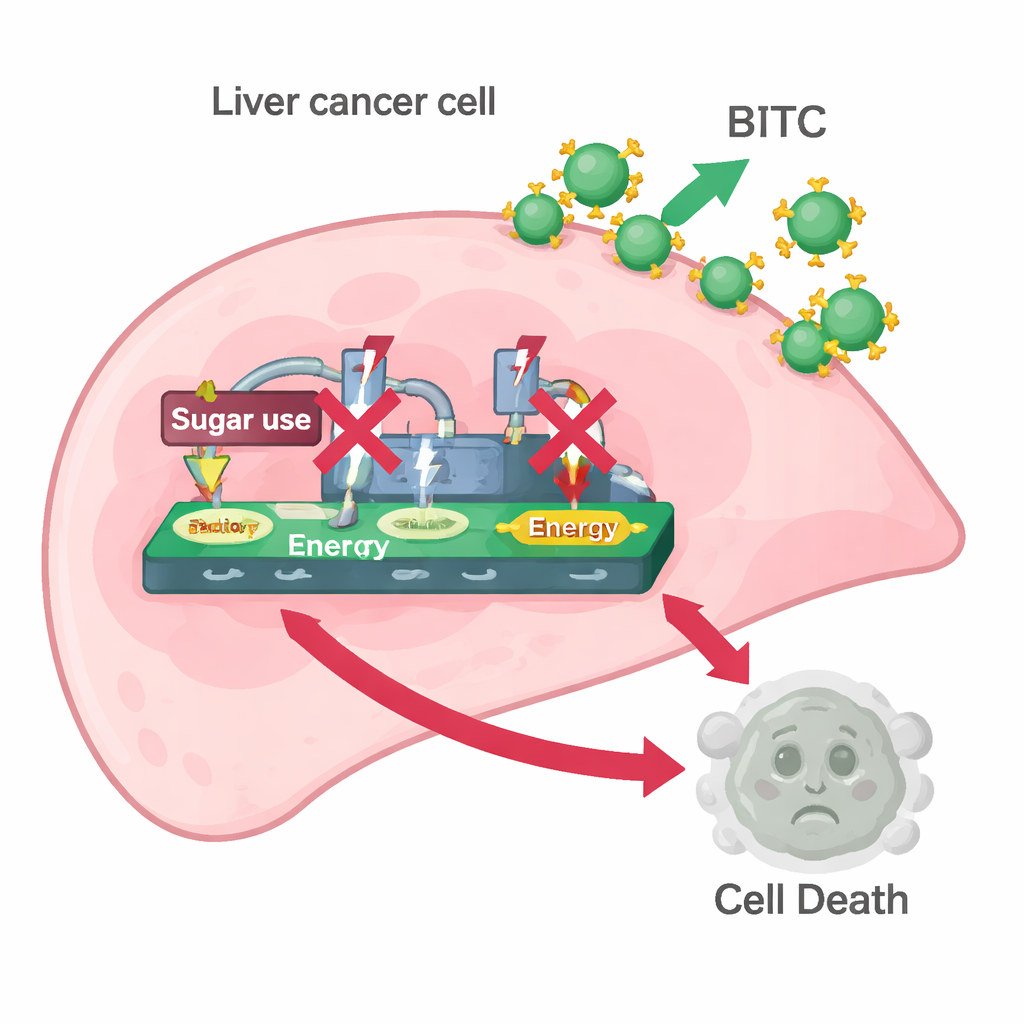
El equipo exploró entonces si el BITC afectaba el efecto Warburg. Midieron proteínas que ayudan a las células cancerosas a captar glucosa y convertirla en energía y lactato —específicamente HK2, PKM2 y LDH. El tratamiento con BITC redujo los niveles de las tres en ambas líneas celulares y disminuyó la cantidad de lactato liberado y de glucosa consumida del medio de cultivo. En otras palabras, el BITC hizo que las células de cáncer de hígado fueran menos capaces de mantener su maquinaria de quema rápida de azúcar. Cuando los científicos añadieron piruvato, un producto aguas abajo de la degradación de la glucosa que aún puede alimentar el metabolismo celular, muchos de los efectos del BITC se invirtieron: las células recuperaron niveles más altos de PARP, caspasa-3 y las enzimas glucolíticas. Esta reversión sugiere que la interferencia con el procesamiento de la glucosa es una parte clave de cómo el BITC desencadena la muerte celular.
Desentrañando los interruptores de control dentro de la célula
Para entender niveles de control más profundos, los investigadores se centraron en un trío de señalización: CNOT2, c-Myc y STAT3. Estas proteínas ayudan a impulsar el crecimiento, la supervivencia y la reprogramación metabólica en muchos tumores. Los datos de pacientes con cáncer de hígado mostraron que CNOT2 tiende a estar más elevado en personas con peores pronósticos. En el laboratorio, el tratamiento con BITC redujo la forma activa fosforilada de STAT3, su activador upstream JAK1, la proteína promotora del crecimiento c-Myc y el propio CNOT2. El uso de herramientas genéticas para disminuir los niveles de CNOT2 o STAT3 potenció aún más el efecto letal del BITC, reduciendo adicionalmente PARP y caspasa-3. Experimentos de unión proteica revelaron que el BITC también interrumpió las asociaciones físicas entre CNOT2 y STAT3 y entre CNOT2 y c-Myc. Cuando CNOT2 o c-Myc se sobreexpresaron de forma artificial, el BITC perdió gran parte de su capacidad para inhibir las enzimas de la glucólisis y desencadenar la apoptosis, subrayando que este eje de señalización actúa como un interruptor maestro que vincula el metabolismo de la glucosa y la supervivencia.
Qué podría significar esto para terapias futuras
En conjunto, los hallazgos dibujan una imagen coherente: el BITC ataca las células de cáncer de hígado cortando su vía de combustible basada en glucosa preferida y activando interruptores de muerte celular que dependen del eje CNOT2/c-Myc/STAT3. Al bloquear tanto las señales de crecimiento como el uso de glucosa, el BITC empuja a las células cancerosas más allá de un punto de inestabilidad metabólica hacia la apoptosis. Estos resultados provienen de experimentos en cultivo celular, no de pacientes, y solo se estudiaron dos tipos de células de cáncer de hígado, por lo que se necesita mucho más trabajo en animales y humanos. Aun así, la investigación refuerza la idea de que ciertos compuestos presentes en vegetales cotidianos podrían ser refinados o combinados con otros tratamientos para privar con mayor precisión a los tumores hepáticos de su alimento mientras se fomenta su autodestrucción.
Cita: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Palabras clave: cáncer de hígado, isotiocianato de bencilo, metabolismo del cáncer, apoptosis, vegetales crucíferos