Clear Sky Science · es
Modelo pronóstico basado en aprendizaje automático de genes relacionados con la plasticidad (stemness) y la angiogénesis para predecir el pronóstico e infiltración inmune en pacientes con CHC
Por qué esta investigación importa para los pacientes con cáncer de hígado
El carcinoma hepatocelular, la forma más común de cáncer de hígado, suele reaparecer o diseminarse incluso después del tratamiento. Este estudio explora por qué sucede eso y cómo los médicos podrían predecir mejor qué pacientes tienen mayor riesgo. Combinando grandes conjuntos de datos genéticos con aprendizaje automático moderno, los investigadores desarrollaron una herramienta que vincula dos rasgos tumorales potentes —la «plasticidad» o stemness (células que se comportan como semillas resistentes) y el crecimiento de nuevos vasos sanguíneos— con las probabilidades de supervivencia de los pacientes y su probable respuesta a terapias basadas en el sistema inmune.
Células “semilla” del cáncer y nuevos vasos sanguíneos
Muchos tumores contienen un pequeño grupo de células que actúan como semillas. Estas células madre cancerosas pueden autorrenovarse, resistir los tratamientos y reiniciar el tumor tras cirugía o quimioterapia. Al mismo tiempo, los tumores necesitan formar nuevos vasos sanguíneos para aportar oxígeno y nutrientes que les permitan crecer y diseminarse. Trabajos recientes muestran que estos dos procesos están interrelacionados: las células con rasgos de stemness liberan señales que fomentan la angiogénesis, mientras que un entorno rico en vasos ayuda a que esas células semilla sobrevivan. Entender y atacar conjuntamente esta asociación es especialmente importante en el cáncer de hígado, que es muy vascularizado y proclive a la recurrencia.
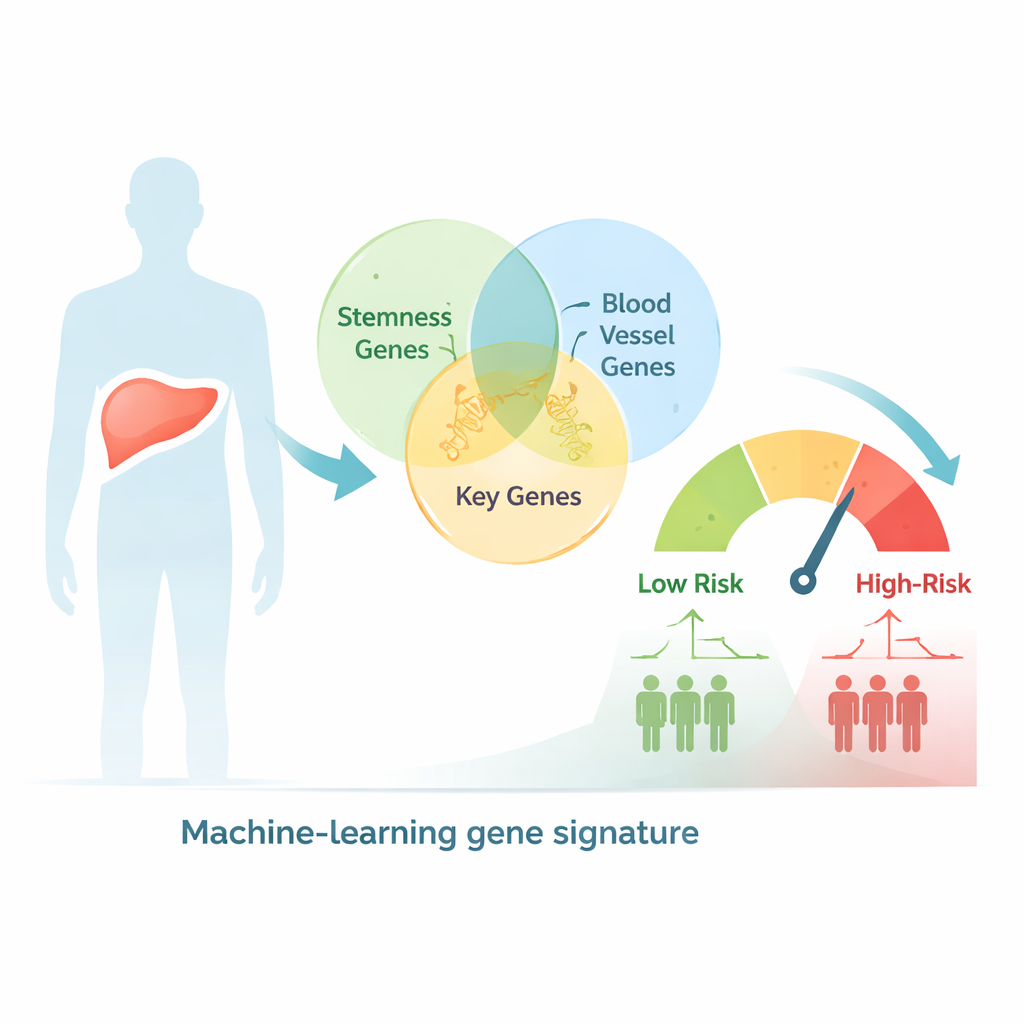
Usar big data para clasificar a los pacientes según riesgo
Los investigadores comenzaron buscando en una gran base de datos genética humana genes relacionados tanto con el comportamiento tipo stemness como con la formación de vasos, obteniendo más de 2.600 candidatos superpuestos. Luego examinaron muestras de cáncer de hígado de cientos de pacientes cuyos perfiles de expresión génica y resultados clínicos estaban registrados en bases de datos públicas. Con pruebas estadísticas y métodos de agrupamiento, clasificaron a los pacientes en dos subtipos genéticos que mostraron diferencias claras en estadio, tamaño tumoral y supervivencia, lo que sugiere que las señales combinadas de stemness y angiogénesis capturan biología relevante en esta enfermedad.
Construcción de una puntuación de riesgo de nueve genes
A partir de este amplio conjunto de genes, el equipo empleó un enfoque de aprendizaje automático para reducirlo a solo nueve genes clave cuya actividad combinada predijo mejor la duración de la supervivencia. Estos nueve genes se usaron para calcular una puntuación de riesgo para cada persona. Los pacientes cuyos tumores tenían una puntuación alta presentaron supervivencia global significativamente menor, tanto en el conjunto de datos original como en un grupo independiente de validación. La precisión del modelo fue competitiva o superior a la de muchas herramientas existentes y, cuando la puntuación se combinó con información clínica sencilla como el estadio tumoral en una herramienta llamada nomograma, la predicción de supervivencia a 1, 3 y 5 años mejoró aún más.
Vínculos con el sistema inmune y la respuesta al tratamiento
El equipo también investigó qué revelaba la puntuación de nueve genes sobre el entorno inmunitario del tumor. Los tumores de bajo riesgo tendían a estar más «inflamados», con mayores niveles de diversas células inmunitarias y señales más fuertes de vías de ataque. En contraste, los tumores de alto riesgo mostraron patrones compatibles con evasión inmune y tasas de mutación mayores en genes importantes como TP53. Usando herramientas computacionales establecidas que estiman la probabilidad de respuesta a fármacos inmunoterapéuticos modernos, el estudio sugirió que los pacientes de bajo riesgo podrían responder mejor a inhibidores de puntos de control inmunitario que los de alto riesgo. Aunque estas predicciones deben validarse en entornos clínicos reales, apuntan a una vía práctica para identificar a los pacientes que podrían beneficiarse más de estos fármacos.
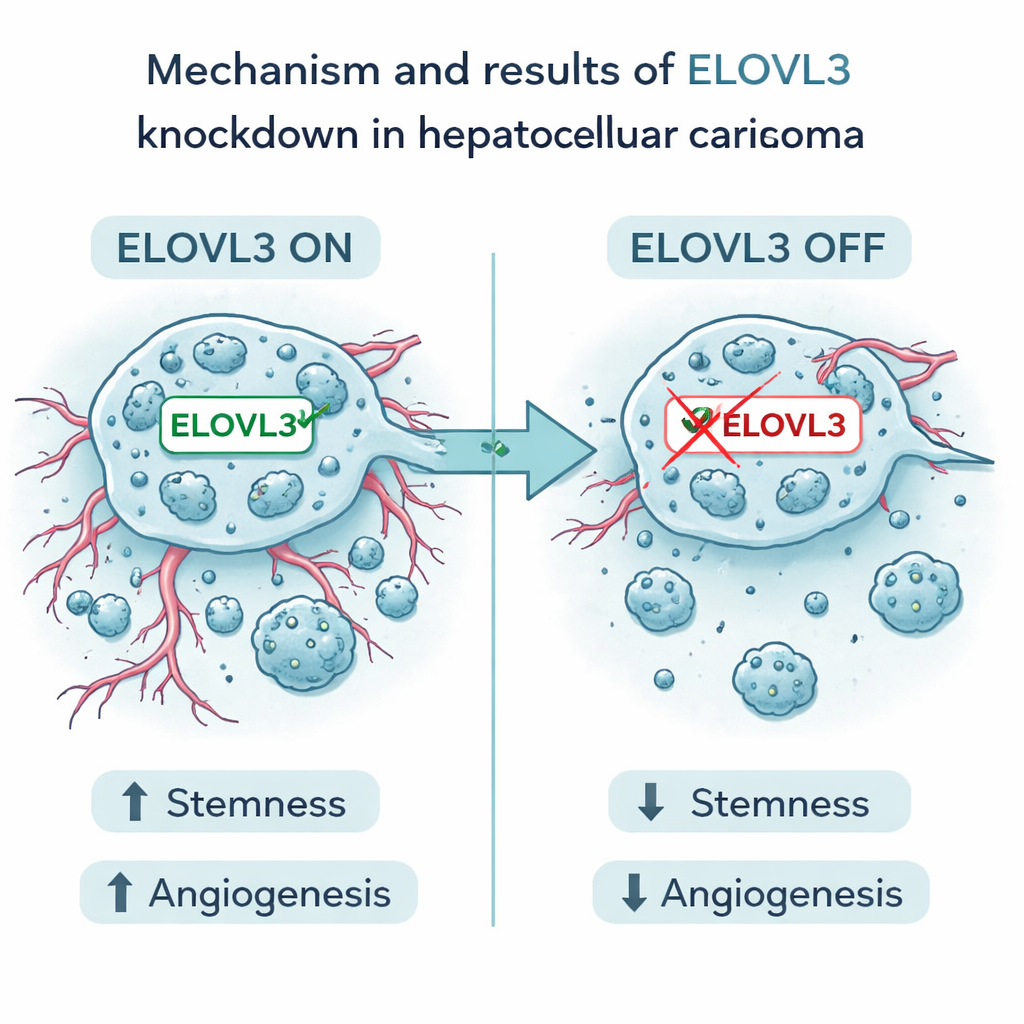
Focalizando un objetivo prometedor
Entre los nueve genes, uno denominado ELOVL3 destacó. Niveles altos de este gen se asociaron con peor supervivencia. En experimentos de laboratorio, los autores redujeron la expresión de ELOVL3 en células humanas de carcinoma hepatocelular. Esto hizo que las células fueran menos capaces de formar agregados con rasgos de stemness y disminuyó los marcadores conocidos de plasticidad. También redujo la producción y liberación de dos factores proangiogénicos importantes, VEGFA y FGF2. Las células cancerosas proliferaron, migraron e invadieron menos, y en modelos murinos, los tumores con menor ELOVL3 eran más pequeños y mostraban menos rasgos de agresividad. Estos hallazgos apoyan la idea de que ELOVL3 favorece tanto el comportamiento tipo semilla de las células de cáncer hepático como su habilidad para construir vasos de apoyo.
Qué podría significar esto para la atención futura
En términos simples, este trabajo aporta dos mensajes principales. Primero, una puntuación sencilla de nueve genes derivada de muestras tumorales puede clasificar a los pacientes con cáncer de hígado en grupos de mayor y menor riesgo y aportar indicios sobre cómo podrían responder a tratamientos basados en el sistema inmune. Segundo, uno de los genes de esa puntuación, ELOVL3, parece situarse en la intersección entre la capacidad del cáncer para regenerarse y para generar nuevos vasos, lo que lo convierte en un objetivo farmacológico atractivo. Aunque el modelo y el objetivo requieren confirmación en ensayos clínicos prospectivos, abren la puerta a una atención del cáncer hepático más personalizada y a estrategias combinadas que bloqueen tanto las «células semilla» tumorales como su suministro sanguíneo.
Cita: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Palabras clave: carcinoma hepatocelular, células madre cancerosas, angiogénesis, firma genética pronóstica, ELOVL3