Clear Sky Science · es
Variabilidad de genes de referencia según la edad y el sexo en ratones 5XFAD destaca desafíos de normalización en modelos de Alzheimer
Por qué este estudio en ratones importa para la investigación del Alzheimer
Cuando los científicos buscan señales tempranas o efectos de tratamiento en la enfermedad de Alzheimer, a menudo miden cuán activados o silenciados están distintos genes en el cerebro. Pero para saber si un gen ha cambiado realmente, primero necesitan una “regla” estable para comparar: genes de referencia que se suponen constantes. Este artículo demuestra que, en un modelo de ratón de progresión rápida de la enfermedad de Alzheimer, esos genes supuestamente estables no lo son tanto como muchos investigadores asumen, sobre todo según la edad, la región cerebral y entre machos y hembras.
Cómo leen los científicos la actividad genética del cerebro
La investigación cerebral moderna suele apoyarse en una técnica llamada RT-qPCR, que cuantifica cuánto del mensajero de un gen determinado está presente en una muestra de tejido. Como las muestras nunca contienen exactamente la misma cantidad total de material, los científicos normalizan sus mediciones con uno o varios genes de referencia, frecuentemente llamados genes “constitutivos”, que se esperan constantes entre condiciones. En la práctica, sin embargo, enfermedades como el Alzheimer alteran de forma drástica los tipos celulares, el metabolismo y la inflamación en el cerebro, lo que puede desplazar silenciosamente los niveles de estos genes de referencia. Si la referencia se desplaza, cualquier medida basada en ella puede resultar engañosa, exagerando u ocultando cambios biológicos reales.
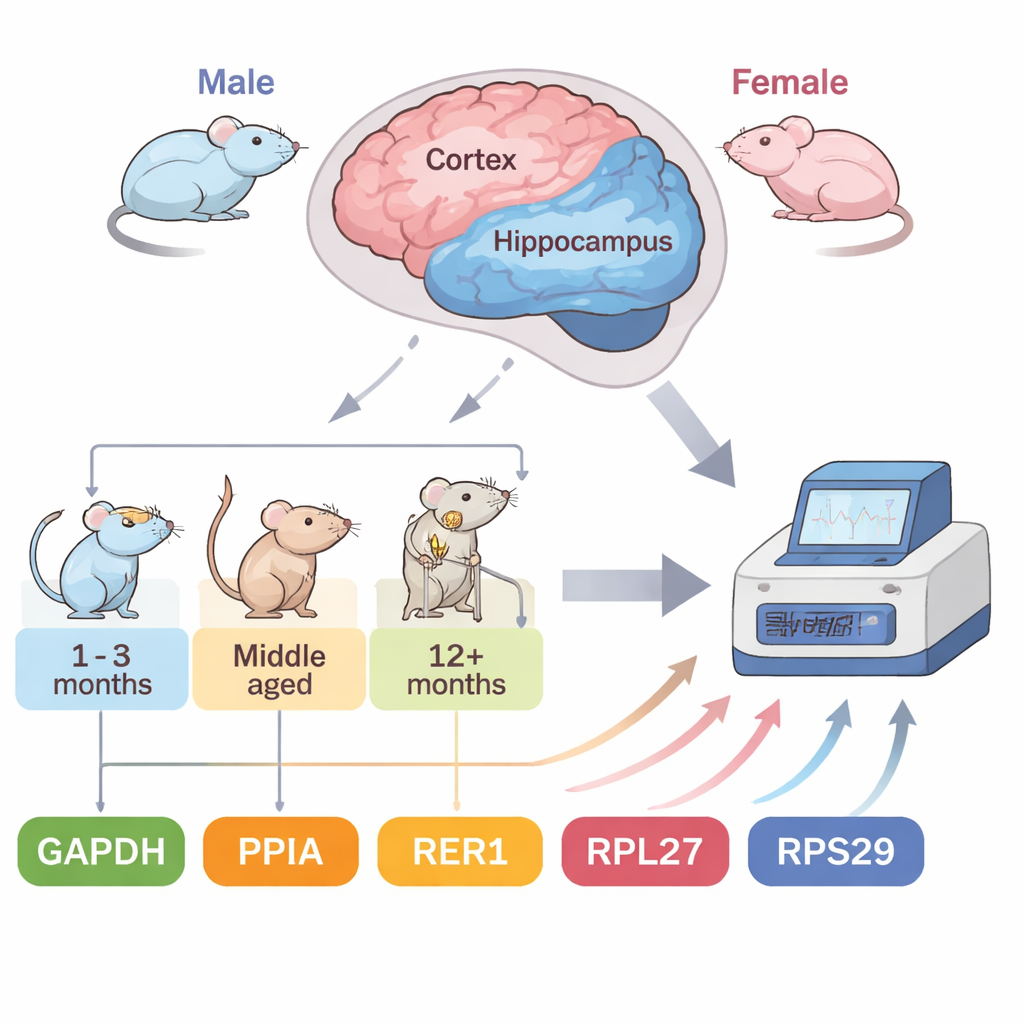
Un modelo de ratón acelerado del Alzheimer
El equipo se centró en ratones 5XFAD, un modelo ampliamente usado que porta cinco mutaciones humanas asociadas a la enfermedad de Alzheimer familiar. Estos animales desarrollan placas amiloides —acúmulos proteicos que son una característica de la enfermedad— de forma notablemente temprana: alrededor de los dos meses de edad, con una gran acumulación a los cuatro o cinco meses. Esta cronología acelerada permite a los investigadores seguir cambios relacionados con la enfermedad en meses en lugar de años. Los autores examinaron dos regiones cerebrales vulnerables, la corteza y el hipocampo, en machos y hembras en cuatro etapas: temprana (2 meses), en desarrollo (4 meses) y más avanzadas (7 y 10 meses). Evaluaron cinco genes de referencia comunes y emplearon cuatro herramientas estadísticas independientes para clasificar la estabilidad de cada uno bajo estas condiciones cambiantes.
Los genes de referencia no valen para todo
Los resultados muestran que ningún gen se mantuvo perfectamente estable en todos los contextos. En su lugar, la estabilidad dependió de la región cerebral de la muestra, del sexo del ratón y del avance de la enfermedad. Algunos genes, como Gapdh —un clásico en muchos estudios—, funcionaron relativamente bien en varios contextos, especialmente en la corteza a edades tempranas, pero mostraron mayor variabilidad en etapas posteriores o en ciertas muestras de hipocampo. Otros candidatos, como Rps29, Ppia, Rpl27 y Rer1, surgieron como mejores compañeros en combinaciones específicas, y estos “mejores pares” cambiaron con la edad y el sexo. En general, la corteza tendió a mostrar más variabilidad que el hipocampo, y las etapas más avanzadas de la enfermedad, particularmente en machos, alteraron la supuesta estabilidad de varios genes de referencia.
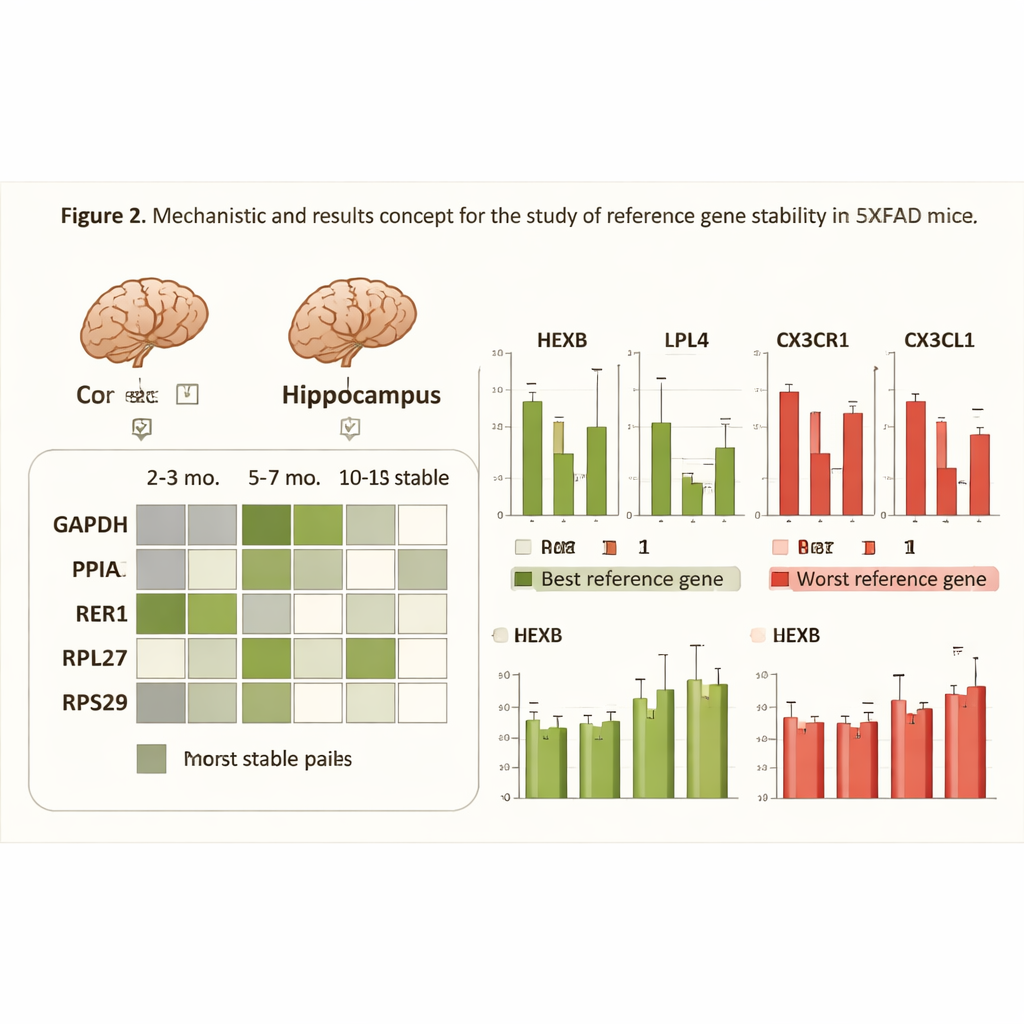
Qué ocurre cuando la regla se dobla
Para demostrar por qué importa elegir cuidadosamente los genes de referencia, los investigadores analizaron cuatro genes cerebrales implicados en inflamación, metabolismo y señalización inmune —procesos profundamente relacionados con la enfermedad de Alzheimer. Compararon cómo variaban los cambios aparentes en estos genes diana al normalizar con el par de referencia más estable, con el gen único menos estable o con los cinco genes juntos. Cuando se usaron genes de referencia pobres, los datos se volvieron más ruidosos y algunos cambios biológicamente relevantes parecieron más débiles o incluso no significativos estadísticamente. En contraste, usar el par mejor emparejado para cada condición redujo la dispersión en las mediciones y reforzó la detección de diferencias reales entre ratones sanos y enfermos, especialmente en etapas avanzadas de la patología.
Señales más claras para una enfermedad compleja
Para el público general, la conclusión es sencilla: incluso las reglas básicas utilizadas en estudios génicos pueden deformarse bajo la presión de una enfermedad cerebral que cambia rápidamente como el Alzheimer. Este trabajo ofrece una guía práctica para elegir mejores genes de referencia en un modelo de ratón importante y subraya que los investigadores deben validar sus “reglas” para cada región cerebral, edad y sexo que estudien. Al hacerlo, los científicos pueden obtener lecturas más claras y fiables de qué genes cambian realmente durante la degeneración similar al Alzheimer —un paso esencial para comprender los mecanismos de la enfermedad y evaluar posibles tratamientos.
Cita: Daini, E., Antonioni, K., Piemontese, M. et al. Reference gene variability across age and sex in 5XFAD mice highlights normalization challenges in Alzheimer’s models. Sci Rep 16, 7302 (2026). https://doi.org/10.1038/s41598-026-38346-5
Palabras clave: Enfermedad de Alzheimer, expresión génica, ratones 5XFAD, genes de referencia, RT-qPCR