Clear Sky Science · es
DGCR8 regula múltiples procesos de la reparación por escisión de nucleótidos acoplada a la transcripción
Cómo la luz solar habla con nuestros genes
Cada vez que nos exponemos al sol, los rayos ultravioletas (UV) invisibles impactan la piel y dañan el ADN de nuestras células. La mayor parte del tiempo, las células reparan discretamente ese daño antes de que cause problemas. Este estudio descubre un actor sorprendente en ese sistema de protección: una proteína llamada DGCR8, conocida hasta ahora por su papel en la biogénesis de microARNs. Los investigadores muestran que DGCR8 puede cambiar de función tras la exposición a UV, coordinando varios pasos de una vía clave de reparación del ADN que ayuda a prevenir el cáncer y otras enfermedades.
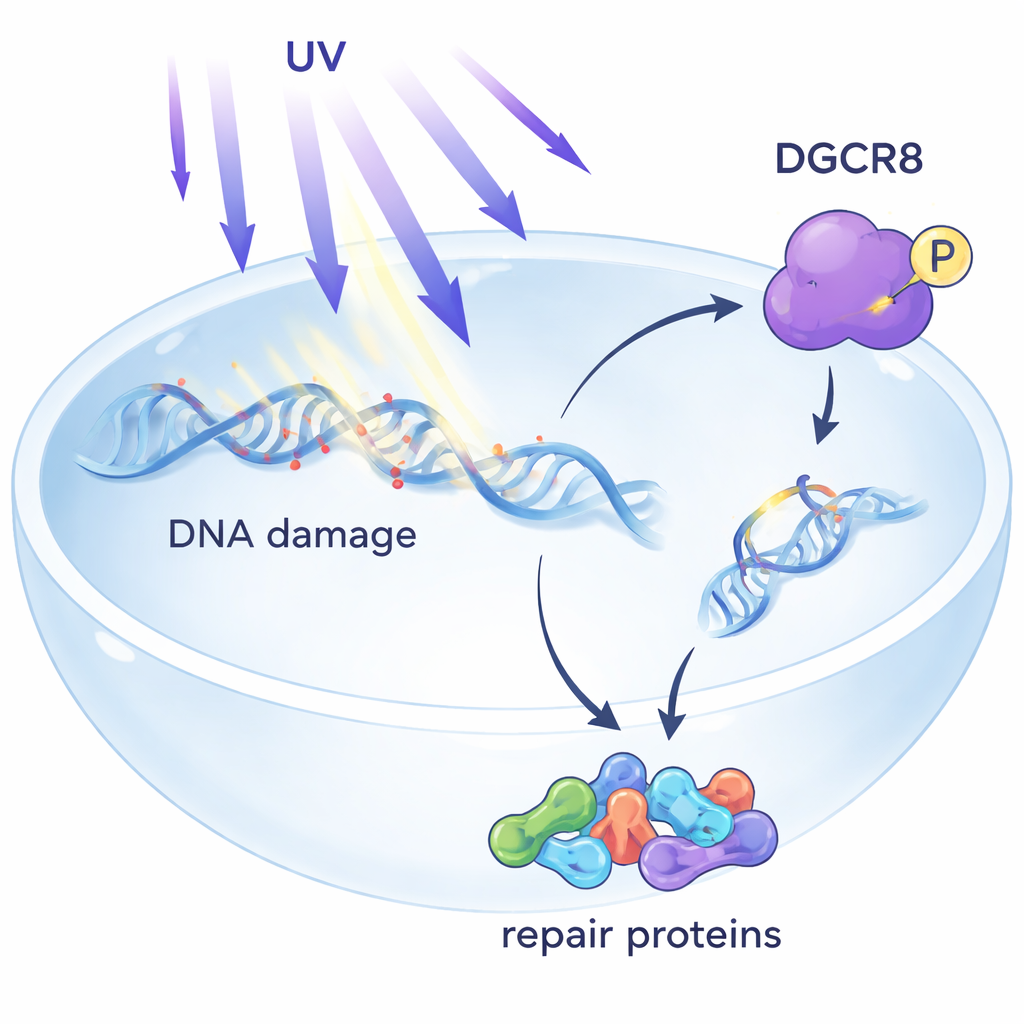
Un guardián oculto dentro de la reparación del ADN
La luz UV crea pequeñas lesiones en el ADN que pueden bloquear las máquinas moleculares que leen los genes. Una de las defensas principales del organismo es la reparación por escisión de nucleótidos acoplada a la transcripción, o TC-NER, que se centra en el daño que detiene a los enzimas lectores de genes. Hasta ahora, DGCR8 se conocía principalmente por procesar microARNs, moléculas cortas de ARN que ajustan la actividad génica. Estudios previos insinuaban que DGCR8 también protegía a las células frente a la radiación UV, pero se desconocía cómo lo hacía. Este artículo muestra que, tras la exposición a UV, DGCR8 se asocia físicamente con factores centrales de TC-NER, actuando como organizador que reúne los componentes de reparación justo allí donde la lectura génica está bloqueada.
Un interruptor molecular de encendido/apagado para DGCR8
La clave del nuevo papel de DGCR8 es una única marca química en uno de sus bloques constructores, el aminoácido serina en la posición 153. Cuando este sitio se fosforila—es decir, se añade un grupo fosfato—DGCR8 adquiere la capacidad de unirse a actores centrales de TC-NER, incluyendo la ARN polimerasa II (la enzima lectora de genes) y factores de reparación llamados CSB, CSA y UVSSA. Células diseñadas con una versión de DGCR8 que no puede fosforilarse en este sitio (el mutante S153A) mostraron interacciones débiles o perdidas entre estas proteínas de reparación, y el ensamblaje normal del complejo de reparación desencadenado por UV falló. Una versión “fosfomimética” que se comporta como si siempre estuviera fosforilada tuvo el efecto opuesto, reforzando interacciones clave incluso sin UV. Estos resultados indican que la fosforilación en Ser153 actúa como un interruptor que cambia a DGCR8 de su función habitual en el procesamiento de ARN a un coordinador de la reparación del ADN.
Desenredando nudos peligrosos ADN-ARN
Más allá de reunir proteínas de reparación, DGCR8 también ayuda a gestionar estructuras llamadas R-loops—tramos cortos donde el ARN recién sintetizado se vuelve a emparejar con el ADN del que procede, formando un híbrido ADN-ARN. En pequeñas cantidades, los R-loops pueden ser útiles, pero cuando se acumulan tras la exposición a UV pueden detener la replicación del ADN y desestabilizar los cromosomas. Usando anticuerpos especializados y sondas fluorescentes, los autores encontraron que las células sin DGCR8, o que portaban la forma no fosforilable S153A, acumulan muchos más R-loops tras la irradiación con UV. Se observó DGCR8 fosforilado en estas estructuras híbridas, especialmente donde se solapan con lesiones inducidas por UV, lo que sugiere que ayuda a prevenir o eliminar R-loops dañinos precisamente en genes activos bajo estrés.
Controlando la copia del ADN
Cuando el daño del ADN o los R-loops interfieren con la copia del genoma, las células normalmente desaceleran la replicación mediante un circuito de seguridad conocido como el punto de control ATR–CHK1. Experimentos de seguimiento de fibras mostraron que las células con DGCR8 normal ralentizaron las pistas de replicación tras la exposición a UV, reflejando un punto de control activado. En marcado contraste, las células sin DGCR8 o que llevaban la mutación S153A continuaron replicando a una velocidad casi normal, a pesar de haber acumulado daño en el ADN y R-loops. Pruebas adicionales revelaron que, aunque ATR en sí se activó, su socio clave CHK1 se activó pobremente en estas células mutantes. Esto indica que la DGCR8 fosforilada ayuda a transmitir la señal de estrés desde el ADN dañado y los R-loops hacia CHK1, permitiendo a la célula pausar y estabilizar la replicación.
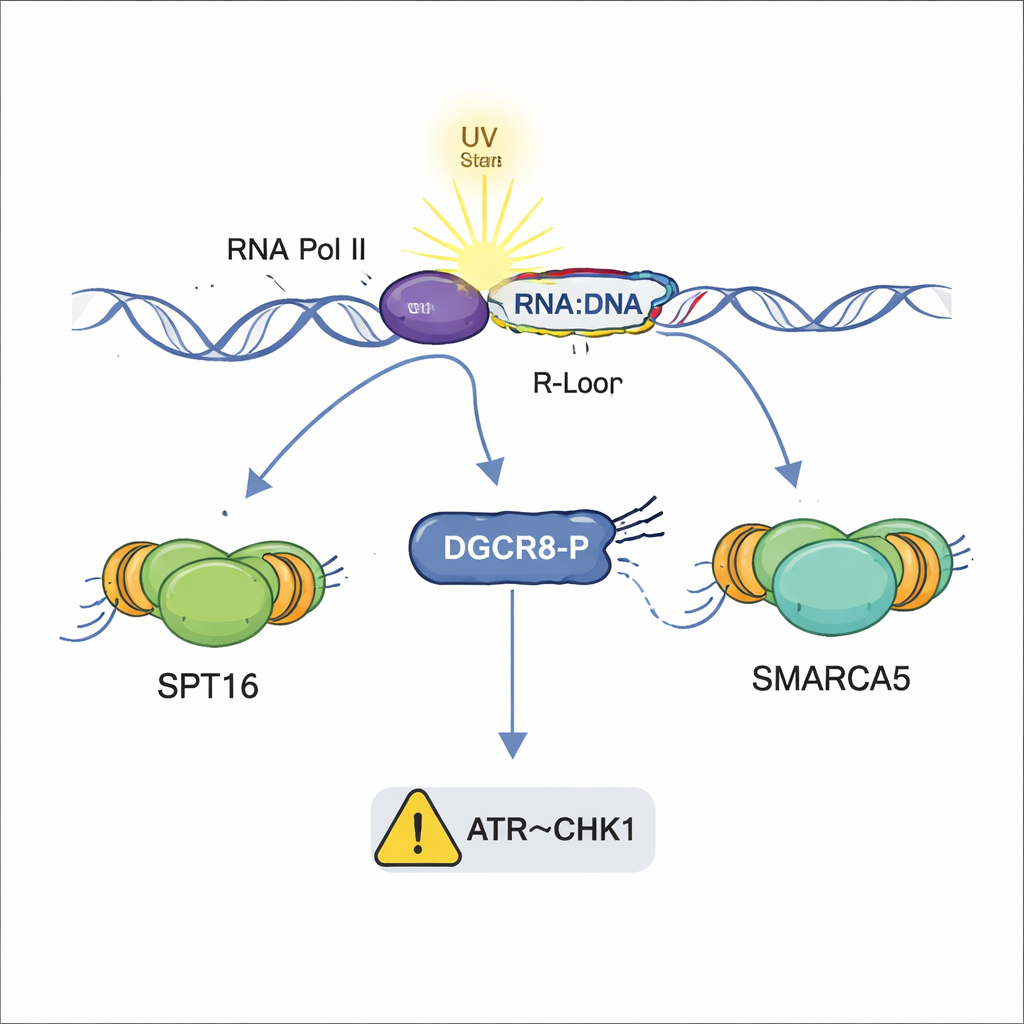
Por qué esto importa para la salud y la enfermedad
En conjunto, los hallazgos revelan a DGCR8 como un guardián polivalente que coordina varias capas de la respuesta al daño por UV: ensamblar el equipo de reparación TC-NER, reclutar remodeladores de cromatina que abren el ADN, restringir híbridos ADN-ARN dañinos y ayudar a activar la desaceleración de la replicación mediante la vía ATR–CHK1. De forma crucial, estas acciones son independientes del papel tradicional de DGCR8 en la biogénesis de microARNs y dependen de la fosforilación de un único sitio. Dado que fallos en la reparación del ADN y en el control de R-loops se asocian con cáncer y enfermedades neurológicas, y se han detectado mutaciones de DGCR8 en algunos tumores, comprender este interruptor molecular podría abrir nuevas vías para diagnosticar o tratar afecciones impulsadas por el daño por UV y la inestabilidad genómica.
Cita: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Palabras clave: Daño por UV en el ADN, DGCR8, Reparación del ADN, R-loops, Estabilidad del genoma