Clear Sky Science · es
PARP-1 conecta la señalización β-catenina/TCF4 con la transición epitelio‑mesénquima en la endometriosis
Por qué esta investigación importa para la salud de las mujeres
La endometriosis es una afección dolorosa en la que tejido similar al revestimiento del útero crece en lugares inadecuados, como los ovarios. Estos parches desplazados pueden invadir estructuras cercanas, causar cicatrices y contribuir a la infertilidad; sin embargo, los tratamientos actuales suelen ser imperfectos y los síntomas con frecuencia reaparecen. Este estudio explora un “interruptor” molecular llamado PARP‑1 y plantea si ayuda a que las lesiones de endometriosis se vuelvan más invasivas —y si fármacos existentes que bloquean PARP‑1 podrían atenuar suavemente ese interruptor.
Una mirada más cercana al comportamiento invasivo de las lesiones
Aunque la endometriosis se clasifica como una enfermedad benigna, el tejido ectópico (desplazado) a menudo se comporta de manera sorprendentemente agresiva: migra, se implanta y persiste de forma similar a un cáncer de crecimiento lento. Un proceso clave detrás de este comportamiento es la transición epitelio‑mesénquima, o TEM (EMT en inglés), en la que las células ordenadas que forman láminas aflojan sus conexiones y adoptan una identidad más móvil y fibrótica. Los autores examinaron tejido de mujeres con y sin endometriosis y encontraron que las lesiones endometrióticas ováricas mostraban un claro patrón similar a la TEM: la proteína “pegamento” E‑cadherina estaba reducida, mientras que marcadores de células más móviles, como N‑cadherina y vimentina, aumentaban. Al mismo tiempo, los niveles de PARP‑1 y de componentes de una vía de control del crecimiento conocida como Wnt/β‑catenina eran más altos en estas lesiones, lo que sugiere que todos estos cambios ocurren de forma conjunta.
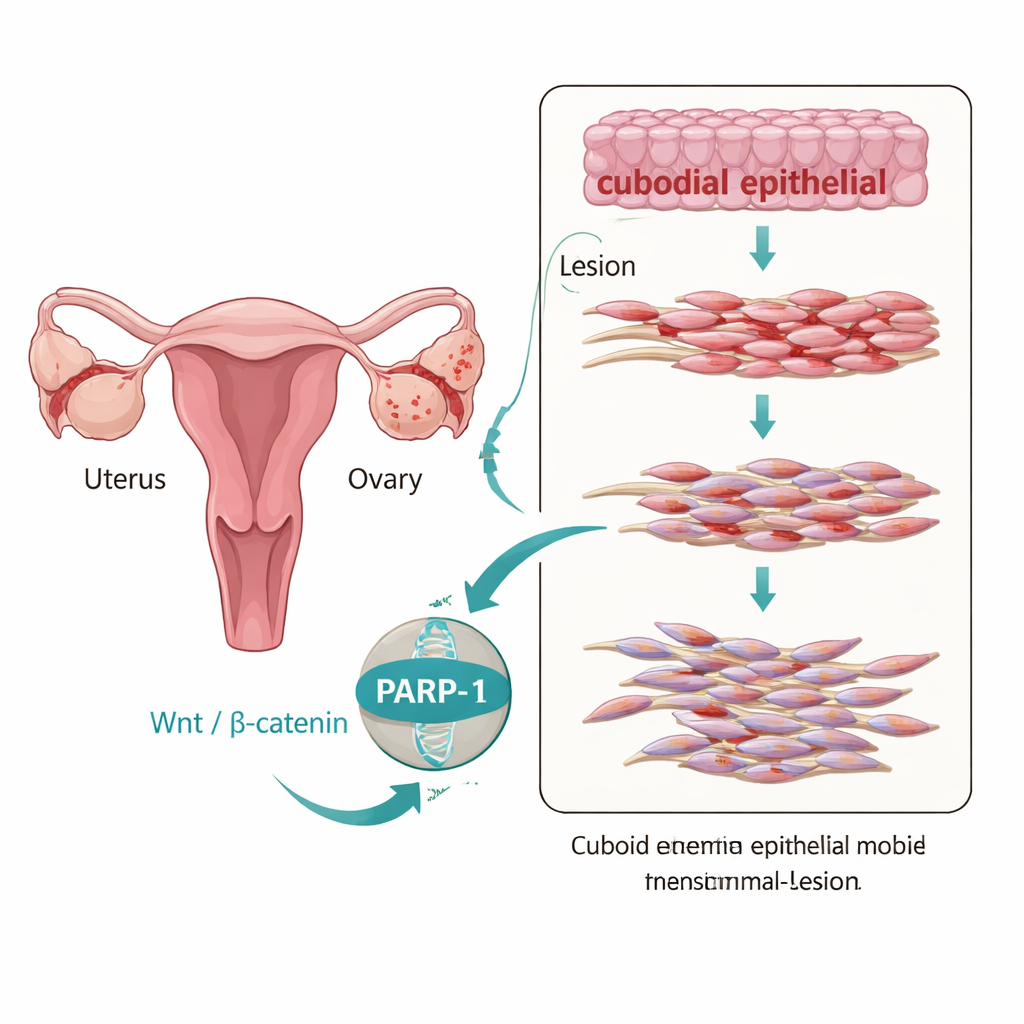
El puente molecular entre señales y cambio celular
Para averiguar si PARP‑1 está simplemente presente o si impulsa activamente estos cambios, los investigadores usaron una línea celular epitelial endometriótica inmortalizada llamada 12Z. Cuando aumentaron artificialmente los niveles de PARP‑1 en estas células, los marcadores de TEM cambiaron hacia un perfil más invasivo y las células se volvieron más móviles y viables en pruebas de laboratorio que imitan la cicatrización y la invasión tisular. Cuando redujeron PARP‑1 usando moléculas de ARN dirigidas, el patrón se invirtió: la E‑cadherina aumentó, los marcadores mesenquimales disminuyeron y las células se movieron y proliferaron menos. De forma importante, PARP‑1 se asoció físicamente con β‑catenina y TCF4, dos factores clave que traducen las señales Wnt en actividad génica, lo que apunta a PARP‑1 como un puente que ayuda a vincular señales externas con el programa génico de la TEM dentro del núcleo.
Atenuando el interruptor con un fármaco oncológico
Dado que los medicamentos que bloquean la actividad de PARP ya se usan en oncología, el equipo preguntó si uno de estos fármacos, olaparib, podría suavizar los rasgos similares a la TEM y reducir el crecimiento de lesiones en un modelo murino de endometriosis. Ratones implantados con pequeños fragmentos de tejido uterino desarrollaron lesiones ectópicas en el abdomen, reproduciendo aspectos de la enfermedad humana. Cuando fueron tratados con olaparib durante dos semanas, estos animales presentaron un volumen total de lesión claramente menor y úteros más ligeros con lesiones adheridas en comparación con los controles no tratados. El tejido de los ratones tratados también mostró un patrón de marcadores más “epitelial”: mayor E‑cadherina y menor N‑cadherina, vimentina, β‑catenina y TCF4, lo que indica que la inhibición de PARP había alejado a las células del estado invasivo similar a la TEM.
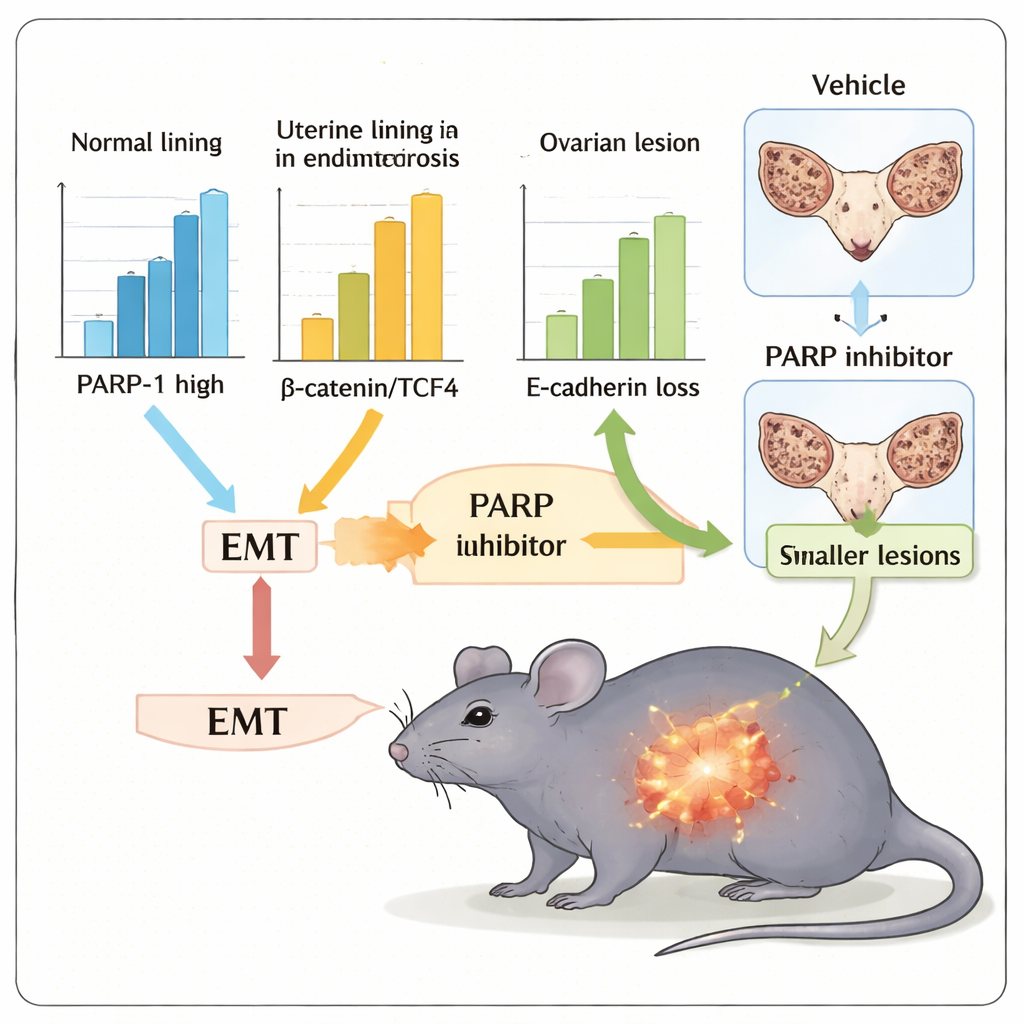
Qué podría significar esto para la atención futura
En conjunto, los hallazgos procedentes de muestras de pacientes, experimentos en cultivo celular y el modelo murino respaldan una idea unificadora: PARP‑1 actúa como un nodo farmacológicamente direccionable que conecta la señalización Wnt/β‑catenina con el comportamiento tipo TEM en la endometriosis. Más que ser el único interruptor maestro, PARP‑1 parece ser un conector clave en una red más amplia de inflamación, estrés oxidativo y señales hormonales que determinan cómo crecen e invaden las lesiones. Dado que ya existen inhibidores de PARP, este trabajo plantea la posibilidad de reutilizarlos o adaptarlos —tal vez en combinación con otros fármacos dirigidos a vías o al sistema inmune— para reducir la carga de lesiones, las adherencias y posiblemente el impacto sobre la fertilidad. Serán necesarios estudios mayores y a más largo plazo, pero esta investigación abre un camino concreto hacia terapias más dirigidas y basadas en mecanismos para una condición que afecta a millones de mujeres en todo el mundo.
Cita: Zhang, L., Li, X., Kong, L. et al. PARP-1 couples β-catenin/TCF4 signaling to epithelial–mesenchymal transition in endometriosis. Sci Rep 16, 6940 (2026). https://doi.org/10.1038/s41598-026-38335-8
Palabras clave: endometriosis, PARP-1, transición epitelio‑mesénquima, Wnt/β-catenina, terapia con inhibidores de PARP