Clear Sky Science · es
Un novedoso método con cámara de flujo acoplada a IA que cuantifica la fragilidad osmótica de los eritrocitos
Por qué importa la fragilidad de los glóbulos rojos
Cada segundo, millones de tus glóbulos rojos se comprimen para pasar por vasos tan finos como un cabello mientras transportan oxígeno. La facilidad con la que estas células se rompen bajo estrés —su “fragilidad”— puede revelar anemia, problemas en el almacenamiento de sangre y complicaciones de infecciones graves como la sepsis. Este estudio presenta un dispositivo moderno asistido por IA acoplado a un microscopio que mide la rapidez con la que los glóbulos rojos se desintegran en soluciones salinas, con el objetivo de hacer esta prueba importante más rápida, más precisa y más fácil de realizar tanto en laboratorios de investigación como, en el futuro, en hospitales.
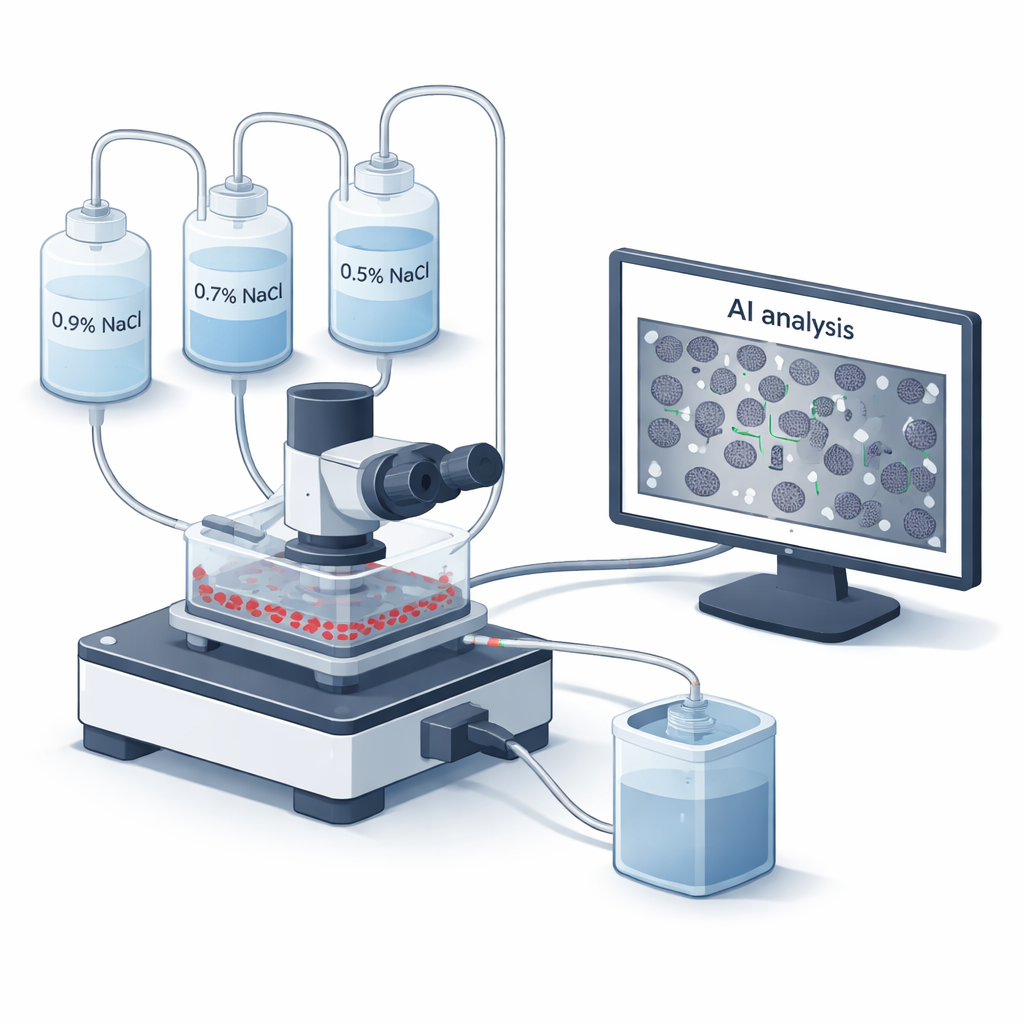
Una nueva forma de observar las células sanguíneas bajo estrés
Los médicos han utilizado pruebas de fragilidad osmótica desde la década de 1940 para evaluar la resistencia de las membranas de los glóbulos rojos. Tradicionalmente, la sangre se mezcla con una serie de soluciones salinas y una máquina mide cuánto hemoglobina se filtra cuando las células estallan. Aunque fiable, este método clásico es lento, manual y no revela cómo lucen las células individuales al fallar. El equipo de este trabajo construyó un nuevo sistema de cámara de flujo microfluídica, llamado BioExP, que extiende los glóbulos rojos en una monocapa delgada sobre una lámina de vidrio tratada. Diferentes soluciones salinas se bombean a través de esta capa mientras un microscopio y una cámara registran lo que ocurre en tiempo real, y el software incorporado usa inteligencia artificial para contar cuántas células permanecen intactas en cada concentración de sal.
Poner a prueba la IA y el control de flujo
Para evaluar si BioExP era fiable, los investigadores lo compararon directamente con el ensayo clásico de espectrofotometría usando sangre de cuatro donantes sanos. Se centraron en un número clave llamado MCF₅₀: la concentración de sal en la que la mitad de los glóbulos rojos han estallado. Primero tuvieron que ajustar su sistema nuevo encontrando el mejor “tiempo de saciación”: cuánto tiempo exponer las células a una solución de baja sal para que las más vulnerables hayan lisado sin exagerar. Al seguir cuántas células desaparecían a 0,4% de sal durante 15 minutos, encontraron que casi el 80% de la hemólisis ocurrió en los primeros tres minutos. Esta ventana de tres minutos se convirtió en su tiempo estándar de exposición, equilibrando la rapidez con mediciones fiables.
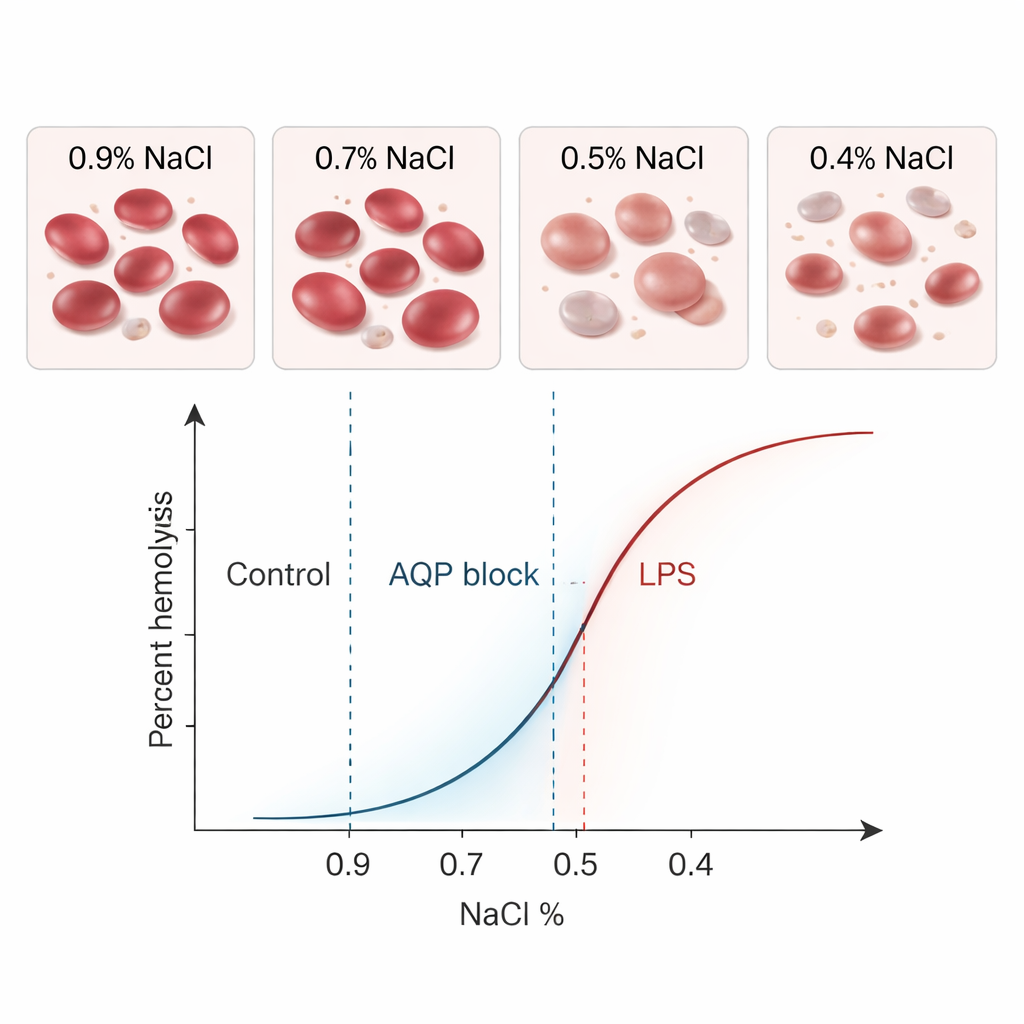
Concordancia con la prueba clásica y sondeando la biología real
Cuando analizaron las mismas muestras sanas con ambos métodos, BioExP y la prueba clásica ofrecieron valores promedio de MCF₅₀ casi idénticos —0,41% de sal— con variabilidad similar. Los análisis estadísticos no mostraron una diferencia significativa entre los métodos, y la mayoría de los pares de resultados cayeron dentro de estrechos límites de concordancia. En otras palabras, el nuevo dispositivo estaba, efectivamente, “hablando el mismo idioma” que el ensayo establecido. Sin embargo, la verdadera fuerza de BioExP radica en su capacidad para evaluar cómo diversas condiciones modifican la fragilidad celular. Los investigadores eligieron dos moduladores con interés biológico: cloruro de mercurio, que bloquea proteínas canales de agua llamadas acuaporinas en la membrana celular, y lipopolisacárido bacteriano (LPS), una toxina asociada con la sepsis.
Cómo las toxinas y los canales de agua cambian la resistencia celular
Bloquear las acuaporinas hizo que los glóbulos rojos fueran más difíciles de romper: el MCF₅₀ se desplazó hacia concentraciones de sal más bajas, lo que significa que las células toleraron una mayor dilución antes de romperse. Tanto BioExP como el método clásico detectaron claramente este desplazamiento hacia la izquierda. El LPS produjo el efecto opuesto. Cuando las células se incubaron con una dosis alta de LPS en ausencia de plasma, se volvieron más frágiles, estallando a concentraciones de sal más altas. Al microscopio, muchas células cambiaron de forma, volviéndose más esféricas o espinosas, signos visuales de que sus membranas se habían alterado. De nuevo, ambos métodos registraron un desplazamiento fuerte y estadísticamente significativo hacia la derecha en las curvas de fragilidad. En todas estas pruebas, el nuevo sistema de cámara de flujo siguió de forma consistente las mismas tendencias biológicas que el ensayo antiguo, aunque con valores absolutos ligeramente menores que fueron pequeños y sistemáticos.
Qué significa esto para pacientes y laboratorios
La plataforma BioExP reduce el tiempo del ensayo de varias horas a menos de una hora, necesita solo volúmenes diminutos de sangre (potencialmente una punción en el dedo) y automatiza el conteo y el ajuste de curvas con IA en lugar de depender de múltiples pasos manuales. Al capturar imágenes de las mismas células a lo largo del tiempo, puede relacionar la apariencia celular con la facilidad con que estallan, y probar muchos niveles de sal o condiciones farmacológicas en una sola corrida. El estudio demuestra que este enfoque moderno puede igualar la exactitud de la prueba clásica de fragilidad osmótica mientras añade velocidad, flexibilidad y un rico detalle visual. Si se valida más en grupos de donantes más grandes y diversos, tales sistemas podrían convertirse en herramientas valiosas para diagnosticar anemias hemolíticas, monitorizar sangre almacenada en bancos y explorar cómo las infecciones o nuevos fármacos debilitan o protegen a nuestros glóbulos rojos.
Cita: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
Palabras clave: glóbulos rojos, fragilidad osmótica, microfluidos, sepsis, inteligencia artificial