Clear Sky Science · es
Expresión espaciotemporal de apéndices de endosporas e información por criomicroscopía electrónica sobre el anclaje de S-ENA mediado por Ena1C en Bacillus paranthracis
Por qué importan las esporas bacterianas resistentes
Las bacterias del grupo Bacillus cereus pueden convertirse en esporas resistentes que soportan el calor, los productos químicos y los agentes de limpieza. Estas esporas a menudo se adhieren a equipos de procesado de alimentos y a otras superficies, donde pueden causar intoxicaciones alimentarias o contaminar productos durante largos periodos. Este estudio examina las diminutas fibras semejantes a pelos en estas esporas, llamadas apéndices de endosporas, y revela cuándo se forman y cómo una proteína clave, Ena1C, las fija en la superficie de la espora. Comprender este proceso podría ayudar a la industria a diseñar estrategias de limpieza más eficaces y también podría inspirar nuevas formas de diseñar esporas útiles para la agricultura o la biotecnología.
Pelitos rígidos en bacterias en reposo
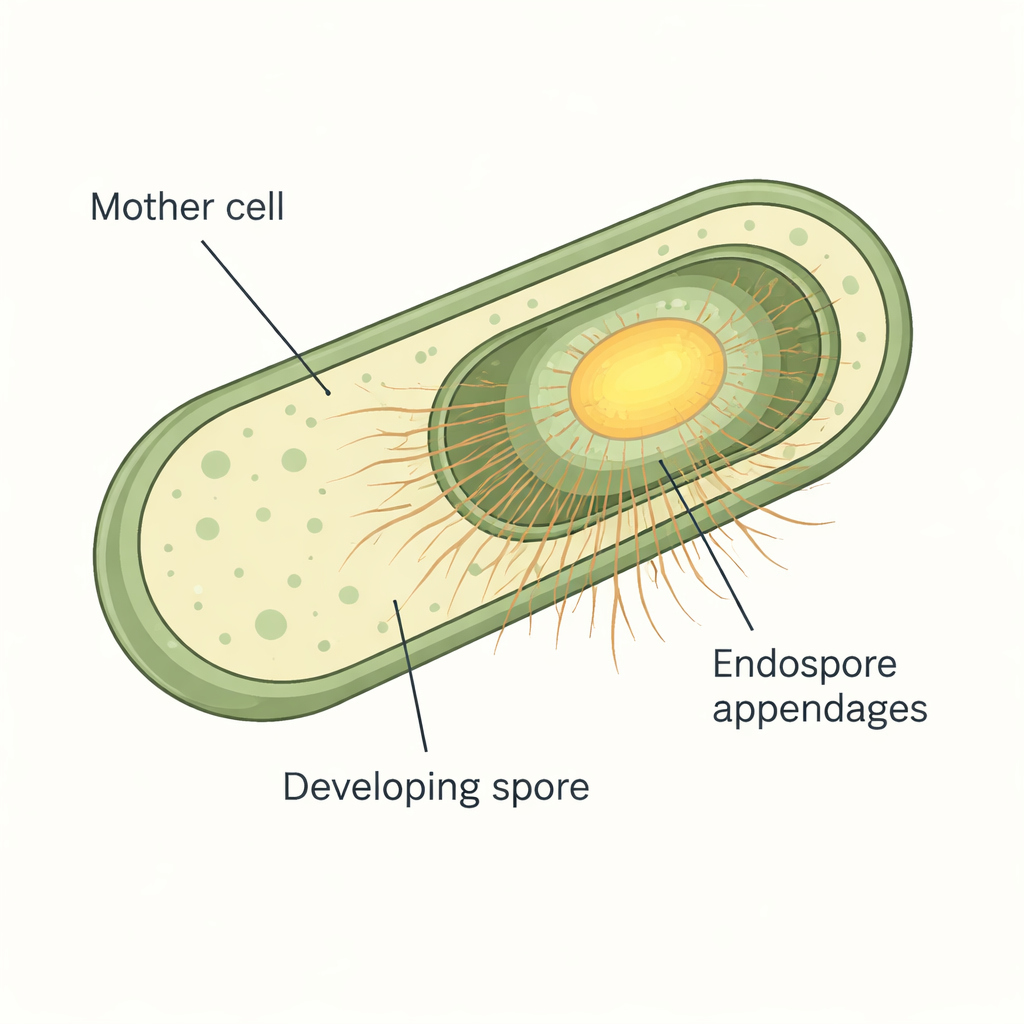
Al microscopio, las esporas de muchos miembros del grupo Bacillus cereus están cubiertas por finas fibras que recuerdan a cerdas o pili. Estos apéndices de endosporas son extremadamente resistentes y aguantan tanto enzimas como agentes químicos agresivos, lo que ha dificultado su estudio. Trabajos previos con criomicroscopía electrónica de alta resolución habían revelado que Bacillus paranthracis fabrica dos tipos principales de fibras: S-ENAs gruesas y escalonadas que constituyen alrededor del 90% de los filamentos, y L-ENAs más delgadas y en forma de escalera que representan el resto. Análisis genéticos ya habían vinculado genes ena específicos con cada tipo de fibra, pero seguían sin responder cuándo y dónde aparecen estas proteínas durante la formación de la espora, ni cómo se anclaban realmente las S-ENAs a la espora.
Vigilar cómo se activan las fibras en tiempo real
Para seguir estos elementos constructivos mientras se formaban las esporas, los investigadores fusionaron las proteínas ENA con etiquetas fluorescentes brillantes, lo que les permitió rastrear cada proteína en células vivas por microscopía de lapso temporal. Cultivaron Bacillus paranthracis sobre almohadillas de agar especialmente preparadas bajo el microscopio y capturaron imágenes cada 10 a 12 minutos mientras las células avanzaban en la esporulación. El equipo observó que ninguna de las proteínas ENA se fabricaba mientras las células crecían con normalidad. En su lugar, la producción comenzaba solo después de que las esporas en desarrollo se volvían "fase-brillantes", un signo visual de que el núcleo de la espora y sus capas protectoras habían madurado. La fluorescencia de las ENA aumentó bruscamente al final de la esporulación y se concentró alrededor de la espora, especialmente en la interfaz entre la célula madre y la espora en formación, lo que muestra que estas fibras son verdaderas decoraciones específicas de la espora añadidas hacia el final del proceso.
Dos tipos de fibras con calendarios diferentes
El equipo también comparó el momento de producción de S-ENA y L-ENA rastreando dos proteínas a la vez en las mismas células. Cuando las subunidades de S-ENA (Ena1A o Ena1C) etiquetadas en verde se expresaban conjuntamente con la subunidad de L-ENA Ena3A etiquetada en rojo, la señal verde aparecía de forma consistente aproximadamente una hora antes que la roja. Este calendario escalonado coincide con lo que se sabe sobre la arquitectura de la espora: las S-ENAs emergen de la capa de la cutícula de la espora, que se forma antes, mientras que las L-ENAs se anclan al exosporio, una envoltura externa añadida más tarde. Los hallazgos sugieren que la célula usa interruptores genéticos de etapa tardía para activar los genes ena en un orden estricto, de modo que cada tipo de fibra se entregue a la capa de espora correcta en el momento oportuno.
Un "muelle" molecular que mantiene las fibras en su sitio
Uno de los actores más enigmáticos fue Ena1C, una proteína necesaria para que las fibras S-ENA aparezcan en las esporas, pero que no forma parte del tallo de la fibra. Al examinar esporas de bacterias sin el gen ena1C, los investigadores encontraron que las fibras S-ENA seguían ensamblándose pero flotaban libres en el líquido circundante en lugar de estar unidas a las esporas. Cuando Ena1C se sobreproducía, las esporas llevaban muchas más S-ENAs, pero cada fibra era más corta, como si un conjunto limitado de bloques de construcción se repartiera entre más puntos de unión. Esto apuntó a Ena1C como un anclaje dedicado que sujeta las fibras S-ENA a la cutícula de la espora, controlando tanto cuántas fibras se fijan como cuánto pueden crecer.
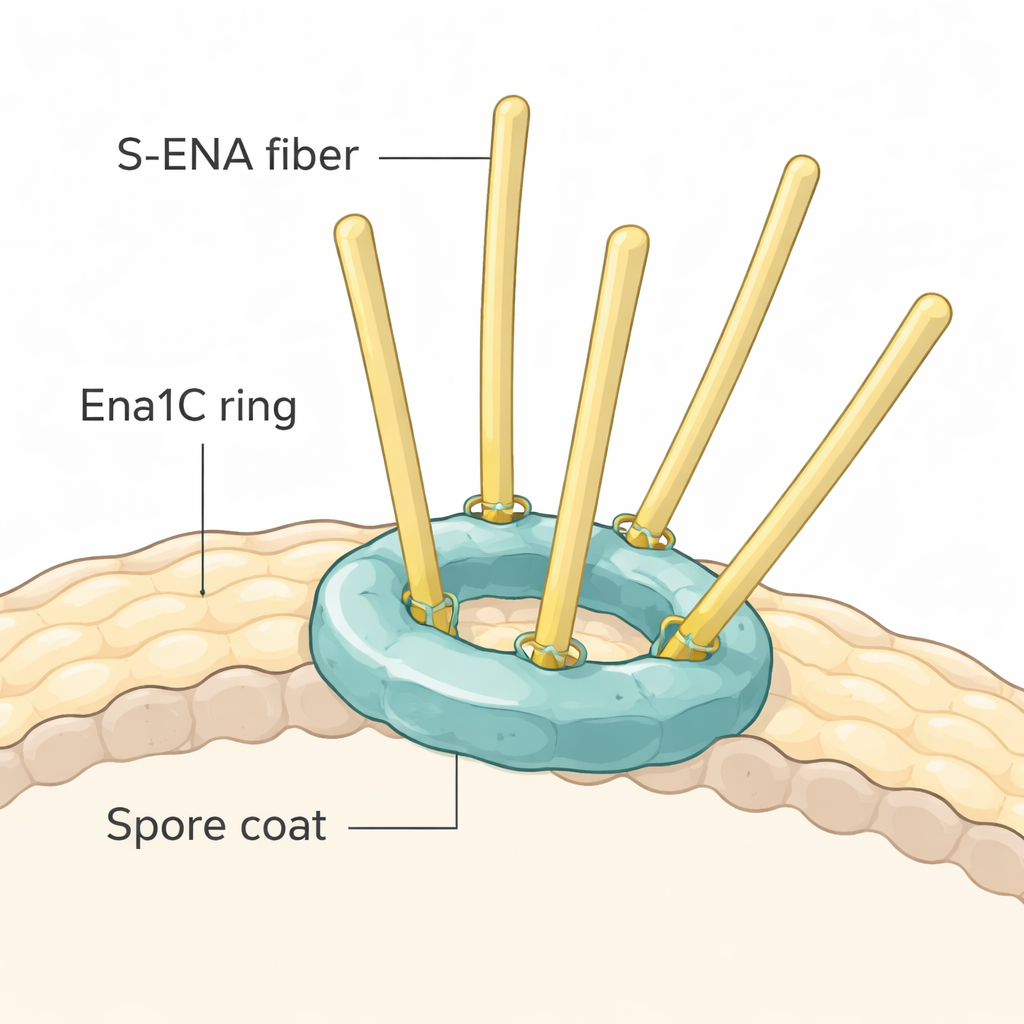
Anclajes en forma de anillo revelados por criomicroscopía
Para ver cómo Ena1C podría sujetar las fibras, el equipo purificó la proteína y la imagenó con criomicroscopía electrónica de alta resolución. Descubrieron que Ena1C no forma filamentos largos. En su lugar, nueve copias de la proteína se ensamblan para crear un anillo resistente con una apertura central, reforzado por múltiples enlaces disulfuro—vínculos químicos fuertes entre aminoácidos que contienen azufre. Modelado por ordenador y comparaciones estructurales con proteínas conocidas de fibras indican que los tallos de S-ENA probablemente encajan en el embudo cargado positivamente en el centro de este anillo, donde residuos de cisteína clave en Ena1C pueden formar enlaces disulfuro con sitios coincidentes en las subunidades de la fibra. De este modo, cada anillo de Ena1C parece servir como un muelle molecular que abrocha una o pocas fibras S-ENA a la capa exterior de la espora.
Qué significa esto para controlar esporas difíciles
En conjunto, el estudio muestra que los pelitos de las esporas en Bacillus paranthracis se producen solo después de que la espora está madura, con las fibras S-ENA construidas y ancladas a la cutícula antes de que las L-ENAs se añadan al exosporio. También identifica a Ena1C como un anclaje en forma de anillo que enlaza covalentemente las fibras S-ENA a la superficie de la espora. Para el público general, el mensaje clave es que la forma en que las esporas se adhieren a las superficies no es accidental: es el resultado de un proyecto de construcción cuidadosamente cronometrado que añade un Velcro robusto basado en fibras al exterior de la espora. Al dirigirse a este sistema de anclaje—ya sea interrumpiendo Ena1C o alterando la formación de ENA—las estrategias futuras podrían debilitar la adhesión de las esporas, haciendo la limpieza industrial más eficaz, o, por el contrario, permitir a los ingenieros diseñar esporas que se adhieran deliberadamente a cultivos o materiales con fines beneficiosos.
Cita: Zegeye, E.D., Sleutel, M., Jonsmoen, U.L. et al. Spatiotemporal expression of endospore appendages and cryo-EM insights into Ena1C-mediated S-ENA anchoring in Bacillus paranthracis. Sci Rep 16, 7122 (2026). https://doi.org/10.1038/s41598-026-38321-0
Palabras clave: esporas bacterianas, adhesión superficial, crio-microscopía electrónica, ensamblaje de proteínas, seguridad alimentaria