Clear Sky Science · es
Las redes neuronales de grafos heterogéneos revelan mecanismos moleculares de la deficiencia de folato en la insuficiencia placentaria mediante integración multiómica
Por qué esto importa para madres y bebés
El folato es mejor conocido como la vitamina de los comprimidos prenatales que ayuda a prevenir malformaciones congénitas, pero su papel en un embarazo saludable va mucho más allá. Este estudio examina cómo la falta de folato puede dañar silenciosamente la placenta, el órgano que nutre y protege al feto en crecimiento. Combinando biología de vanguardia con inteligencia artificial avanzada, los investigadores muestran cómo cambios sutiles en genes, proteínas y pequeñas moléculas actúan conjuntamente para privar a la placenta de lo que necesita, y exploran cómo este conocimiento podría algún día ayudar a los médicos a detectar embarazos de alto riesgo de forma más temprana.
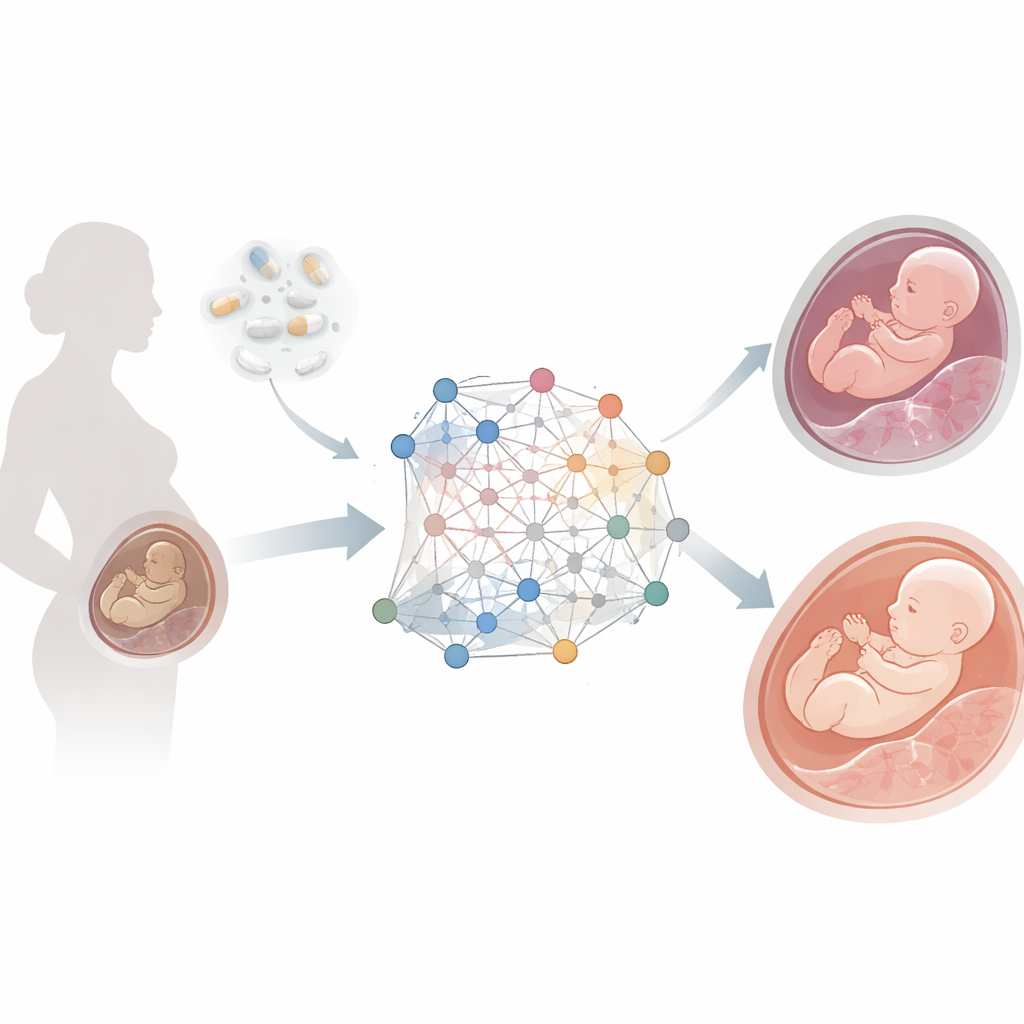
Cuando la placenta no da abasto
La insuficiencia placentaria ocurre cuando la placenta no puede suministrar suficiente oxígeno y nutrientes al feto, lo que provoca complicaciones como crecimiento fetal deficiente, preeclampsia y parto prematuro. Afecta aproximadamente entre el cinco y el diez por ciento de los embarazos en el mundo. El folato está en el centro de muchos procesos celulares: construir ADN, controlar qué genes se activan o desactivan y mantener vasos sanguíneos sanos. Cuando los niveles de folato son demasiado bajos, estos sistemas pueden fallar, pero ha sido difícil rastrear la cadena precisa de eventos dentro del tejido placentario. Los estudios tradicionales suelen examinar un solo tipo de datos biológicos a la vez, como genes o metabolitos, perdiendo la visión global de cómo interactúan estas capas.
Leer la placenta con muchas lentes
Para afrontar esta complejidad, el equipo recogió muestras placentarias en el momento del parto de 156 embarazos con insuficiencia placentaria relacionada con el folato y 142 controles sanos. De cada muestra midieron cuatro tipos diferentes de información molecular: cambios en el ADN, actividad génica, niveles de proteínas y pequeños metabolitos. En lugar de tratar estas mediciones como listas largas y separadas, las vincularon en un gran mapa biológico que contenía 6.704 moléculas y más de 16.000 interacciones conocidas. Genes, proteínas y metabolitos se representaron como distintos tipos de nodos conectados por aristas que reflejaban cómo se unen, regulan o transforman entre sí en células reales.
Enseñar a una red inteligente a detectar problemas
Los investigadores entrenaron entonces un modelo de inteligencia artificial especializado llamado red neuronal de grafos heterogénea sobre este mapa molecular. A diferencia de los algoritmos convencionales que ven cada medición de forma aislada, este modelo “escucha” cómo se propagan las señales a lo largo de toda la red. Asigna pesos de atención para resaltar las moléculas y conexiones más informativas a la hora de distinguir placentas enfermas de las sanas. En un conjunto de prueba retenido, el modelo clasificó correctamente el 94,7% de las placentas y alcanzó un área bajo la curva ROC casi perfecta de 0,978, superando con claridad a los métodos tradicionales de aprendizaje automático y a cualquier análisis que utilizara un único tipo de dato. Esto demuestra que la señal de la enfermedad no reside solo en marcadores individuales, sino en patrones compartidos a través de múltiples capas biológicas.
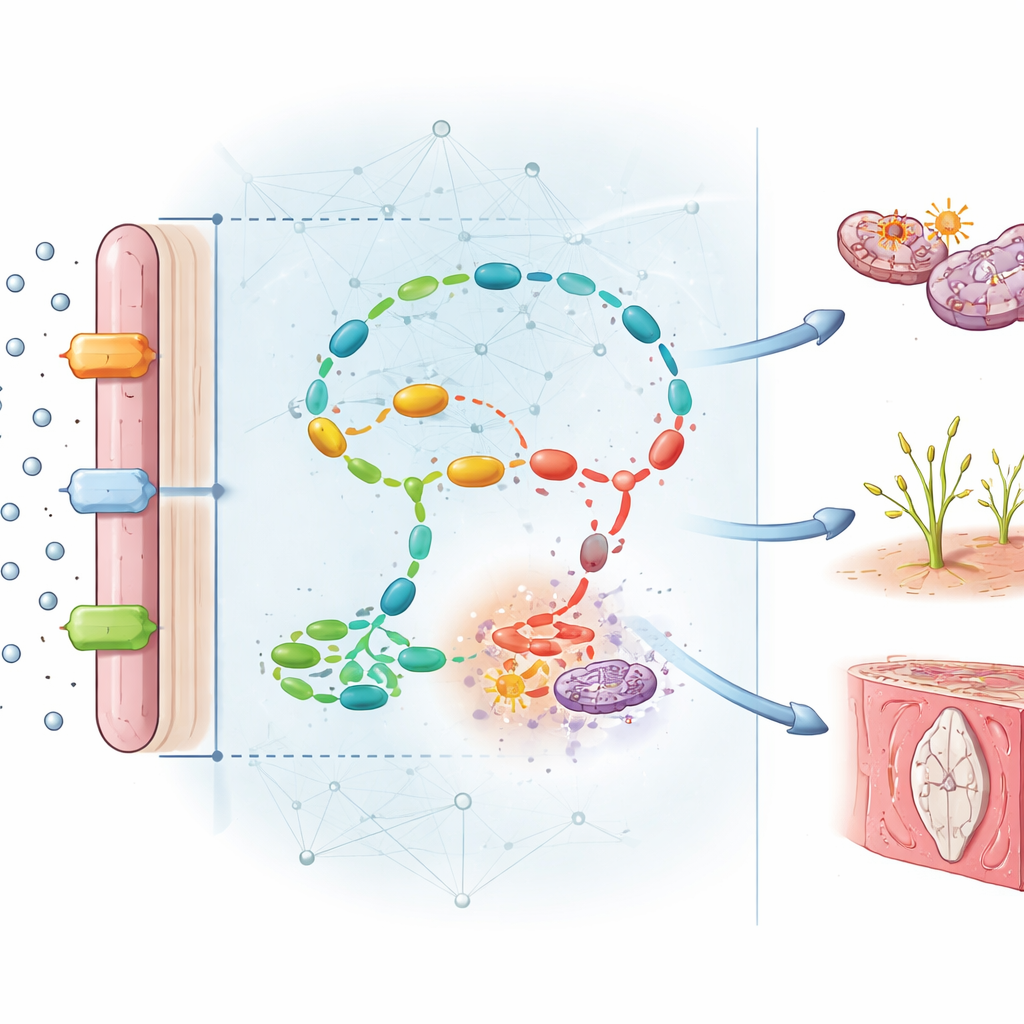
Descubrir las cadenas ocultas de daño
Más allá de la predicción, el diseño del modelo permitió a los autores ver qué moléculas pesaban más en sus decisiones. Varias destacaron. Componentes clave del manejo del folato, como la enzima MTHFR y el transportador de folato FOLR1, estaban fuertemente reducidos en placentas enfermas, mientras que la homocisteína, un subproducto tóxico, se acumuló más de seis veces. A partir de la red surgieron siete módulos funcionales principales que vinculan la alteración de la química del folato con la reducción de la metilación del ADN, el aumento del estrés oxidativo, el crecimiento defectuoso de vasos sanguíneos, la inflamación y la muerte celular excesiva. En otras palabras, la deficiencia de folato no daña la placenta de una sola manera; desencadena una red de fallos conectados que en conjunto limitan el flujo sanguíneo y la entrega de nutrientes al feto.
Qué podría significar esto para la atención futura
Por ahora, este trabajo es sobre todo un microscopio potente más que una prueba clínica. Como todas las muestras se tomaron en el momento del parto, el modelo aún no puede usarse para predecir el riesgo durante el embarazo, cuando la intervención sería más importante. Aun así, las firmas moleculares que revela, especialmente los cambios combinados en el transporte de folato, la acumulación de homocisteína y las vías dañadas de crecimiento vascular, ofrecen una hoja de ruta para buscar marcadores en sangre que puedan reflejar lo que ocurre en la placenta. Con estudios futuros que sigan a las madres a lo largo del tiempo y comparen su sangre con el tejido placentario, este enfoque podría ayudar a desarrollar herramientas de cribado tempranas y no invasivas y estrategias nutricionales o médicas más personalizadas para proteger los embarazos vulnerables.
Cita: Xie, X., Li, Z., Xiao, Q. et al. Heterogeneous graph neural networks reveal molecular mechanisms of folate deficiency in placental insufficiency through multiomics integration. Sci Rep 16, 8417 (2026). https://doi.org/10.1038/s41598-026-38288-y
Palabras clave: insuficiencia placentaria, deficiencia de folato, redes neuronales de grafos, multiómica, complicaciones del embarazo