Clear Sky Science · es
La inhibición de PERK atenúa la muerte celular multiprogramada mediante la activación de Nrf2/HO-1 en la retinopatía diabética con proteómica integrada y validación funcional en HRECs
Por qué proteger la visión en la diabetes importa
Para millones de personas con diabetes, una de las complicaciones más temidas es la pérdida progresiva de la visión conocida como retinopatía diabética. Este daño al tejido fotosensible en la parte posterior del ojo suele comenzar de forma silenciosa, mucho antes de que aparezcan los síntomas. El estudio detrás de este artículo investiga qué es lo que realmente mata a las diminutas células de los vasos sanguíneos que mantienen la retina sana, y prueba una nueva forma de protegerlas. Al comprender y calmar las «respuestas de estrés» celulares desencadenadas por la azúcar elevada en sangre, los investigadores esperan ralentizar o incluso prevenir la ceguera en personas con diabetes.
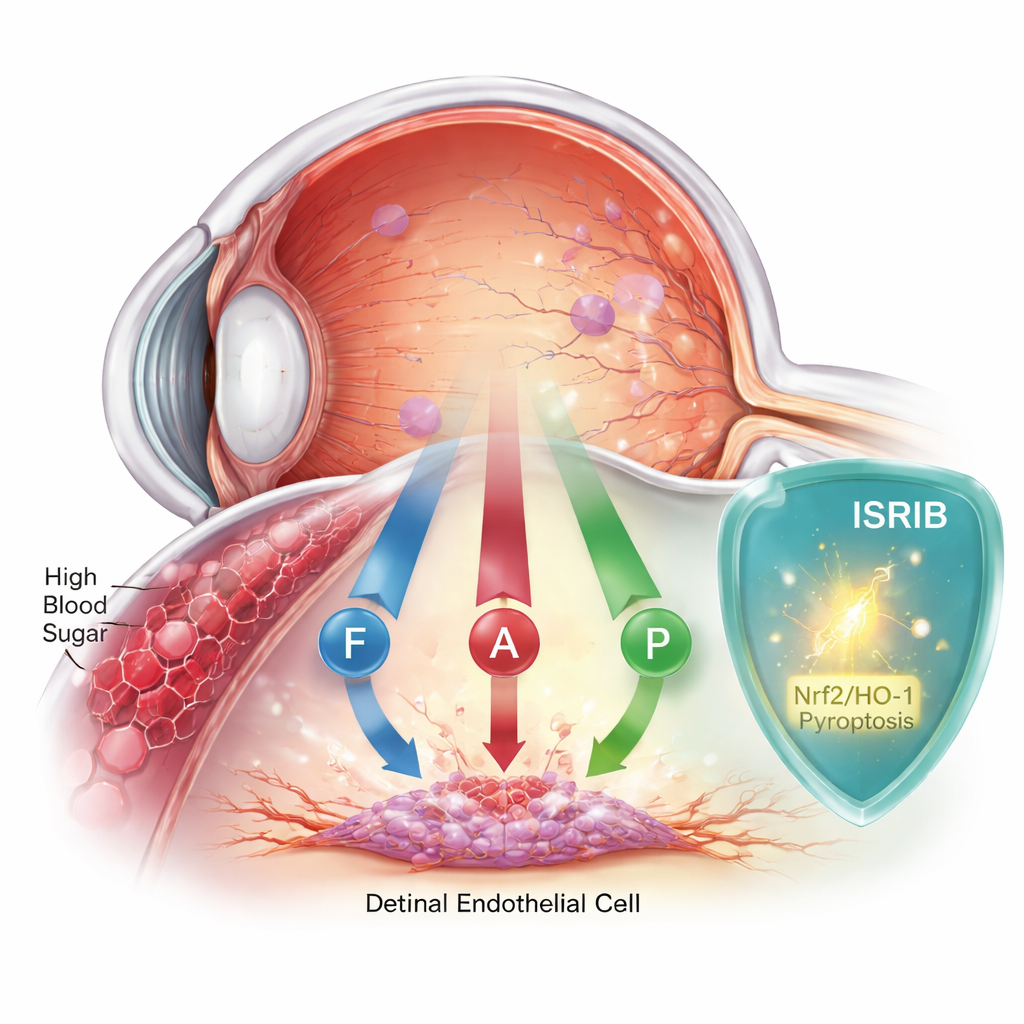
Cuando la glucosa daña el ojo en silencio
La retinopatía diabética comienza cuando la glucosa alta daña el delicado revestimiento interno de los vasos sanguíneos retinianos. Estas células forman una barrera que mantiene la retina nutrida y protegida. Durante años, los científicos pensaron que una única forma de muerte celular, llamada apoptosis, era la principal culpable. Pero la evidencia acumulada sugiere que la historia es más compleja. Este equipo se centró en células endoteliales retinianas humanas cultivadas en el laboratorio y las expuso a niveles de azúcar similares a los observados en diabetes mal controlada, y luego observó cómo respondían las células a lo largo de dos días.
Tres formas en que las células pueden morir a la vez
Usando una potente técnica de medición de proteínas llamada proteómica, los investigadores encontraron que los niveles altos de glucosa alteraban cientos de proteínas, especialmente las implicadas en respuestas al estrés, el metabolismo y el manejo del hierro. Pruebas posteriores mostraron que las células no morían de una sola manera, sino de tres: la clásica muerte programada (apoptosis), una forma inflamatoria y «ardiente» (piroptosis) y una forma más reciente impulsada por el hierro llamada ferroptosis. Marcadores de daño oxidativo, sobrecarga de hierro y agotamiento de antioxidantes aumentaron, mientras que las enzimas protectoras disminuyeron. En conjunto, estos cambios dibujaron el retrato de células desbordadas por el estrés, la inflamación y la acumulación tóxica de moléculas reactivas.
Un interruptor de estrés en el centro del problema
El equipo se centró entonces en un sensor clave de estrés dentro de las células llamado PERK, que se encuentra en la membrana del retículo endoplásmico, una estructura que ayuda a plegar y procesar proteínas. Bajo condiciones de glucosa alta, PERK se volvió hiperactivo, actuando como una alarma de emergencia atascada que sigue sonando. Esto pareció alimentar los tres programas de muerte. Al mismo tiempo, un sistema de defensa natural que normalmente ayuda a las células a hacer frente al daño oxidativo —la vía antioxidante Nrf2/HO-1— se debilitó. En términos sencillos, las señales de peligro se intensificaron mientras que los extintores internos se apagaron.
Bajar el estrés, aumentar la protección
Para ver si podían romper este ciclo destructivo, los investigadores trataron las células expuestas a alta glucosa con ISRIB, una pequeña molécula que atenúa eficazmente la señalización de estrés de PERK. Los resultados fueron llamativos. ISRIB mejoró la supervivencia celular, redujo los marcadores de daño impulsado por el hierro y el estrés oxidativo, y disminuyó las señales químicas tanto de apoptosis como de piroptosis. Al mismo tiempo, potenció la vía de defensa Nrf2/HO-1, ayudando a las células a restaurar su capacidad antioxidante. Un fármaco separado que bloquea específicamente la ferroptosis también fue beneficioso, pero ISRIB destacó porque calmó las tres vías de muerte a la vez en lugar de solo una.
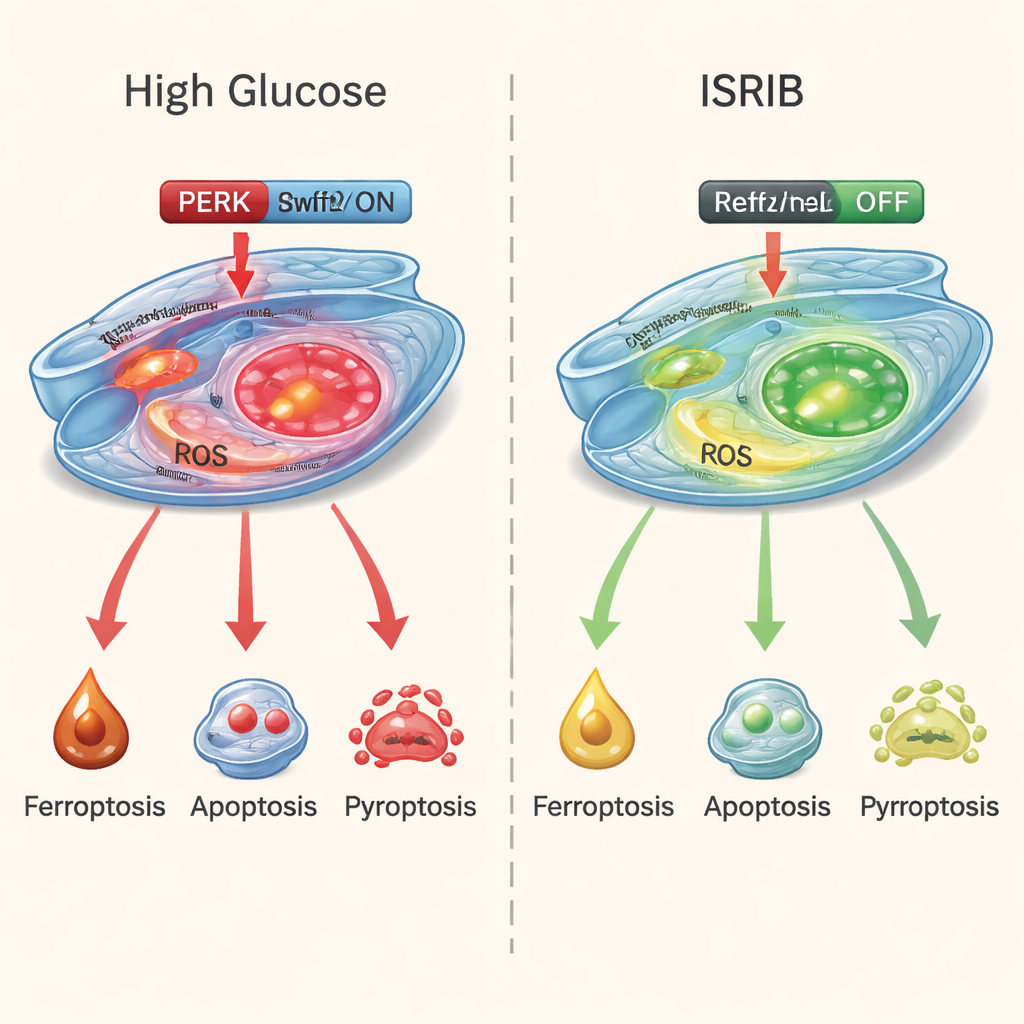
Qué podría significar esto para las personas con diabetes
Este trabajo sugiere que el daño temprano en la retinopatía diabética no lo provoca un único «actor malo», sino la convergencia de varios programas de muerte que se refuerzan entre sí y son impulsados por el estrés celular crónico. Al bajar el interruptor de estrés PERK y reactivar los sistemas protectores propios de la célula, fármacos como ISRIB podrían ofrecer una forma más unificada de mantener con vida los vasos sanguíneos retinianos. Aunque estos experimentos se realizaron en células, no aún en pacientes, apuntan hacia tratamientos futuros que apunten a las respuestas de estrés dentro del ojo, y que potencialmente podrían añadir una nueva capa de protección junto al control glucémico y las inyecciones oculares actuales para ayudar a preservar la visión en la diabetes.
Cita: Xie, L., Zhang, X., Tian, M. et al. PERK inhibition attenuates multi-program cell death through Nrf2/HO-1 activation in diabetic retinopathy with integrated proteomics and functional validation in HRECs. Sci Rep 16, 7225 (2026). https://doi.org/10.1038/s41598-026-38213-3
Palabras clave: retinopatía diabética, muerte celular retiniana, estrés oxidativo, vía PERK, Nrf2 HO-1