Clear Sky Science · es
La inhibición de la vía SHH y el co‑cultivo con astrocitos inducen respuestas distintas en glioblastoma y en células madre cancerosas
Por qué los tumores cerebrales son tan difíciles de tratar
El glioblastoma es uno de los cánceres cerebrales más letales y, aun con cirugía, radiación y quimioterapia, solo una pequeña fracción de pacientes sobrevive más de cinco años. Una razón es que estos tumores no están formados por un único tipo de célula. Incluyen un pequeño grupo de células especialmente persistentes, las “células madre” cancerosas, que pueden sobrevivir al tratamiento y ayudar a que el tumor vuelva a crecer. Este estudio plantea una pregunta clave: ¿cómo responden estos diferentes tipos celulares cuando se bloquea una señal que impulsa el crecimiento, y cómo cambia esa respuesta la presencia de células normales de soporte cerebral llamadas astrocitos?
Una mirada más cercana a las células más resistentes del tumor
Los investigadores trabajaron con dos tipos principales de células de un modelo común de glioblastoma: las células del tumor en masa y una pequeña subpoblación marcada por una proteína llamada CD133, que se comporta como células madre cancerosas. Estas células con rasgos de madre se dividían menos, eran más pequeñas y redondeadas, y formaban racimos más compactos que las células de la masa tumoral. El equipo también cultivó las células tumorales junto con astrocitos, las células en forma de estrella que ayudan a mantener el tejido cerebral sano. Este cultivo mixto imita mejor el entorno real del tumor, donde las células cancerosas mantienen una comunicación constante con sus vecinas. 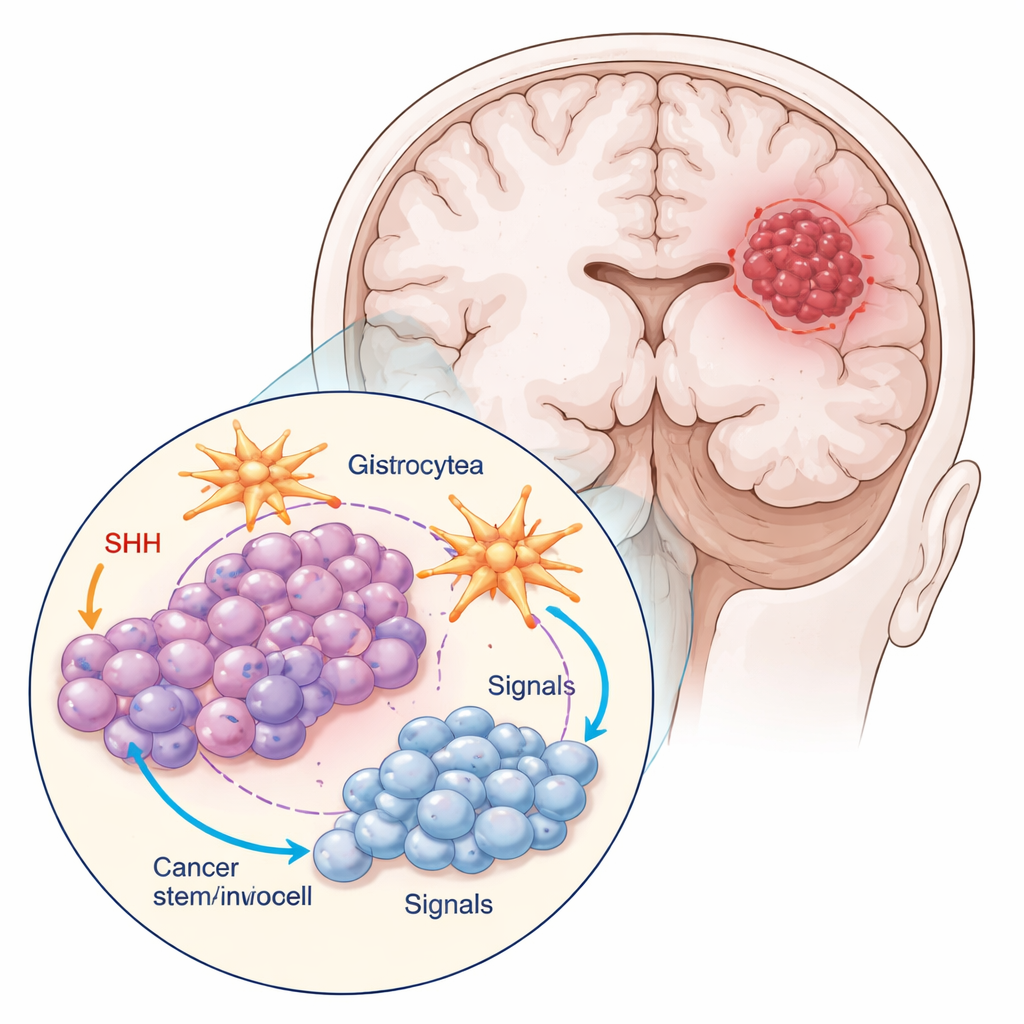
Bloquear una señal del desarrollo que los tumores reutilizan
Muchos glioblastomas, y en particular sus células con rasgos de madre, secuestran una vía de comunicación molecular llamada Sonic Hedgehog (SHH), normalmente activa durante el desarrollo cerebral. El equipo empleó ciclopamina, un compuesto que bloquea un componente clave de SHH, para ver cómo responden tanto las células de la masa tumoral como las células madre cancerosas. Midieron la actividad de genes y proteínas relacionados con SHH, la velocidad a la que las células avanzaban por el ciclo celular y con qué frecuencia sufrían muerte celular programada (apoptosis). La ciclopamina modificó la señalización SHH de manera que dependía mucho del tipo celular y de si había astrocitos presentes. Las células madre cancerosas producían más señal SHH cuando se cultivaban solas, pero esta secreción cayó cuando se cultivaban con astrocitos y se exponían al fármaco, lo que sugiere que las células cerebrales circundantes pueden atenuar el “auto‑sostén” químico del tumor.
Cómo el vecindario altera crecimiento y muerte
Más allá de SHH en sí, el equipo siguió otras redes génicas que regulan si las células continúan dividiéndose, se detienen o comienzan a especializarse. En cultivos simples solo con tumor, el bloqueo de SHH empujó a las células de la masa tumoral hacia una detención en la fase tardía de la división (G2/M), mientras que las células con rasgos de madre tendían a acumularse antes, en la fase de reposo o entrada (G0/G1). Al añadir astrocitos, estos patrones cambiaron: las células madre cancerosas, que habían sido más quiescentes, se desplazaron hacia un arresto en G2/M, lo que implica un conjunto diferente de “frenos” aplicado en el entorno mixto. Los investigadores también observaron que señales vinculadas al destino celular y la morfogénesis—como las vías WNT, BMP y TGF‑β—se regulaban de forma distinta en las células de la masa y en las células con rasgos de madre cuando había astrocitos presentes, lo que significa que el microambiente puede inclinar a las células hacia un comportamiento más mantenedor de la condición de madre o hacia un estado más diferenciado y menos agresivo.
Provocar la muerte celular en las células más resistentes
El estudio examinó además con qué facilidad las células entraban en apoptosis. Lecturas genéticas y una prueba de detección de daño en el ADN (ensayo TUNEL) mostraron que la ciclopamina favorecía una vía “externa” de muerte celular, impulsada por una proteína llamada CASP8, en particular en la población de células madre cancerosas. Curiosamente, en células tumorales cultivadas solas, la muerte celular global a veces disminuía tras el bloqueo de SHH, lo que sugiere que esas células podían activar estrategias de supervivencia alternativas. Por el contrario, cuando las células con rasgos de madre se co‑cultivaron con astrocitos, la ciclopamina aumentó marcadores de apoptosis, indicando que las células cerebrales circundantes pueden hacer que estas células, por lo demás resistentes, sean más vulnerables una vez bloqueada la señalización SHH. 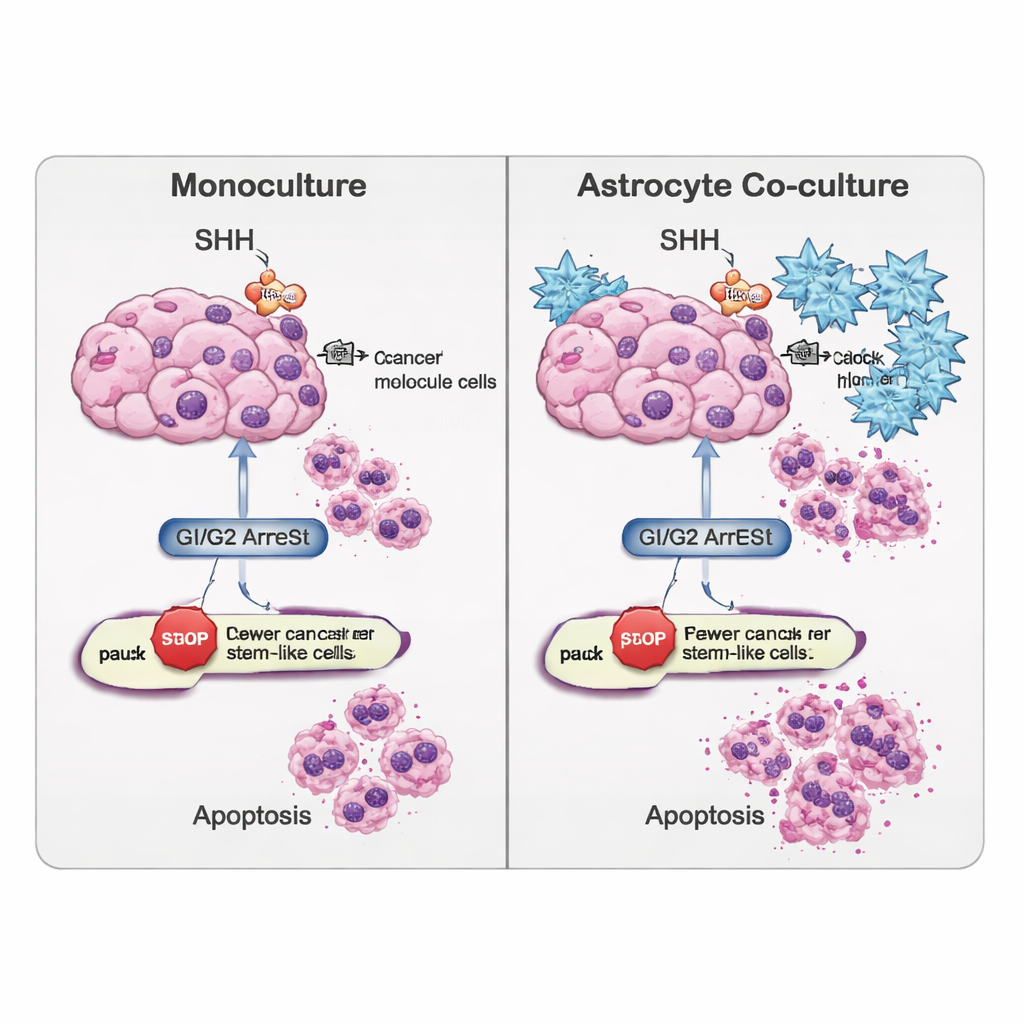
Qué implica esto para futuros tratamientos del cáncer cerebral
Para un público no especialista, el mensaje clave es que dirigir una sola señal de crecimiento en glioblastoma no es suficiente si se ignora el vecindario del tumor. Este trabajo muestra que los astrocitos—las células normales que comparten espacio con el tumor—pueden cambiar profundamente cómo responden tanto las células de la masa tumoral como las células madre cancerosas al bloqueo de la vía SHH. Las células madre cancerosas, en particular, se volvieron más propensas al arresto del ciclo celular y a una forma de muerte celular cuando había astrocitos presentes. Los autores concluyen que los fármacos dirigidos a SHH y vías relacionadas tienen más probabilidades de funcionar si se prueban y, eventualmente, se usan de formas que reflejen el entorno real del cerebro, posiblemente en combinación con otros tratamientos que ataquen las rutas de supervivencia alternativas del tumor. En resumen, comprender y explotar la “conversación” entre las células tumorales y sus vecinas puede abrir estrategias más precisas y duraderas contra este cáncer tan implacable.
Cita: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Palabras clave: glioblastoma, células madre cancerosas, vía Sonic Hedgehog, microambiente tumoral, astrocitos