Clear Sky Science · es
Identificación y validación de una nueva firma génica relacionada con la ferroptosis asociada con la degeneración retiniana hereditaria en ratones Rd10
Por qué importa que las células del ojo mueran para todos nosotros
La retinitis pigmentosa es un grupo de enfermedades oculares hereditarias que arrebatan gradualmente la vista, a menudo comenzando con ceguera nocturna y culminando en una pérdida completa de la visión. No existe cura, y las terapias génicas disponibles solo pueden ayudar a una pequeña fracción de los pacientes. Este estudio explora un enfoque distinto: una forma especial de muerte celular llamada ferroptosis, impulsada por el hierro y el daño oxidativo, para descubrir nuevos genes diana que podrían, en el futuro, proteger a las células sensibles a la luz en la retina —independientemente de la mutación con la que haya nacido una persona.
Una mirada más cercana a una enfermedad que causa ceguera
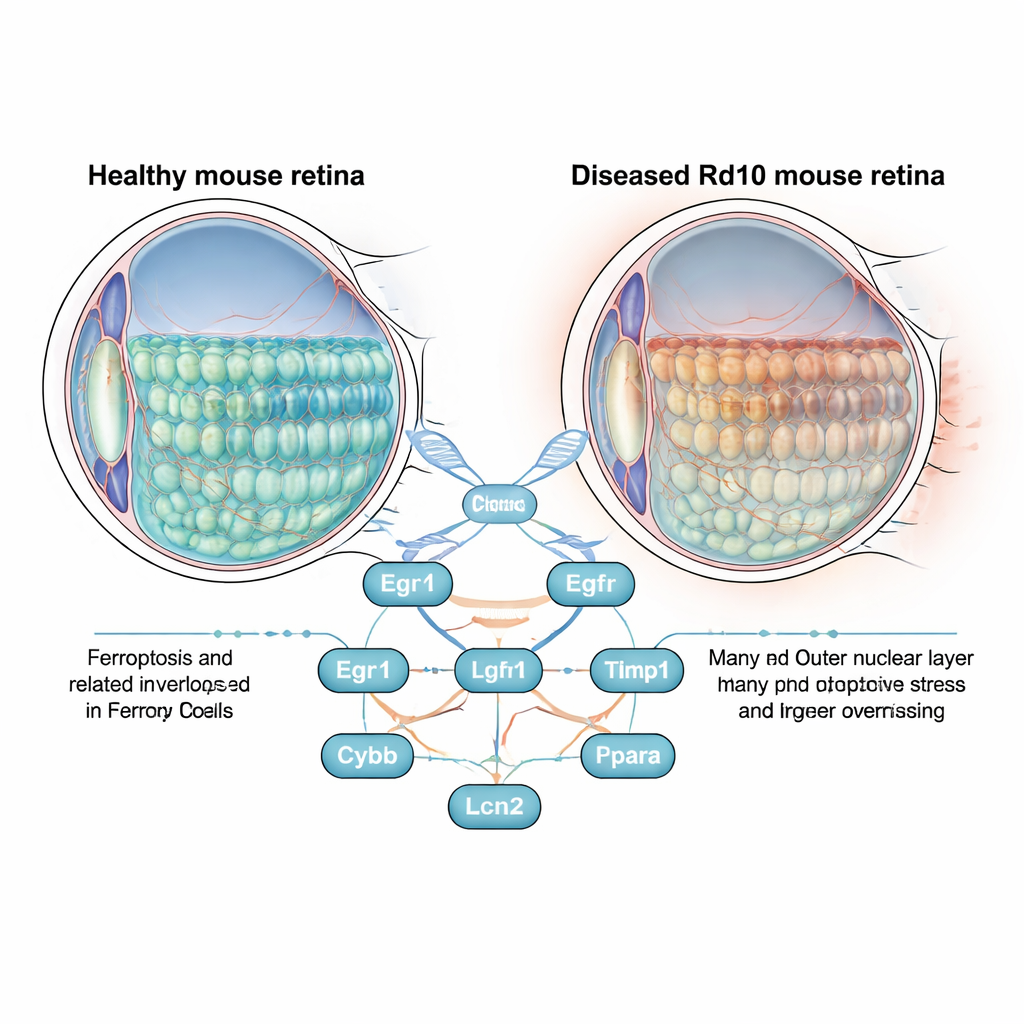
La retina es una capa delgada de tejido en la parte posterior del ojo que alberga los fotorreceptores en bastón y cono, las células que convierten la luz en señales eléctricas. En la retinitis pigmentosa, estas células mueren lentamente, privando primero de la visión nocturna y periférica y, más tarde, de la visión central. Los científicos suelen estudiar este proceso en ratones Rd10, que portan una mutación que imita estrechamente la enfermedad humana. En lugar de centrarse únicamente en el gen defectuoso, los autores plantearon una pregunta más amplia: a medida que la retina degenera, ¿qué genes vinculados a la ferroptosis se activan o desactivan, y podrían estar impulsando la pérdida celular?
Encontrar los genes clave en un mar de datos
El equipo analizó grandes conjuntos públicos de datos de expresión génica de retinas de ratones sanos y Rd10, tomando esencialmente una “instantánea” global de qué genes estaban más o menos activos. Encontraron más de 2.000 genes que cambiaron, y luego los cruzaron con una lista curada de genes relacionados con la ferroptosis. Esto redujo el campo a 37 candidatos ligados a la muerte celular oxidativa impulsada por el hierro. Los análisis computacionales mostraron que estos genes se agrupaban en procesos como la respuesta al estrés oxidativo, la regulación de la muerte neuronal y las vías del metabolismo de los lípidos, marcas de la ferroptosis y respuestas al estrés conocidas en nervios en degeneración.
Ocho genes que destacan
Para identificar a los actores más influyentes, los investigadores construyeron una red de interacción de proteínas y aplicaron varios algoritmos de clasificación. Surgieron ocho genes “centro”: Egr1, Cd44, Egfr, Tlr4, Timp1, Cybb, Lcn2 y Ppara. Siete de ellos mostraron mayor actividad en las retinas enfermas, mientras que Ppara mostró una actividad reducida. El grupo confirmó estos patrones en un conjunto de datos independiente y luego examinó más de cerca dónde aparecían los genes principales en el ojo. Mediante tinción fluorescente y secuenciación de ARN a una sola célula, demostraron que Egr1 aumenta de forma marcada en fotorreceptores en bastón y cono, mientras que Cd44 se eleva de manera pronunciada en las células de Müller, las células gliales de soporte que atraviesan la retina. Esto sugiere que los fotorreceptores estresados y sus células de soporte podrían cooperar —quizá de forma perjudicial— a través de vías vinculadas a la ferroptosis.
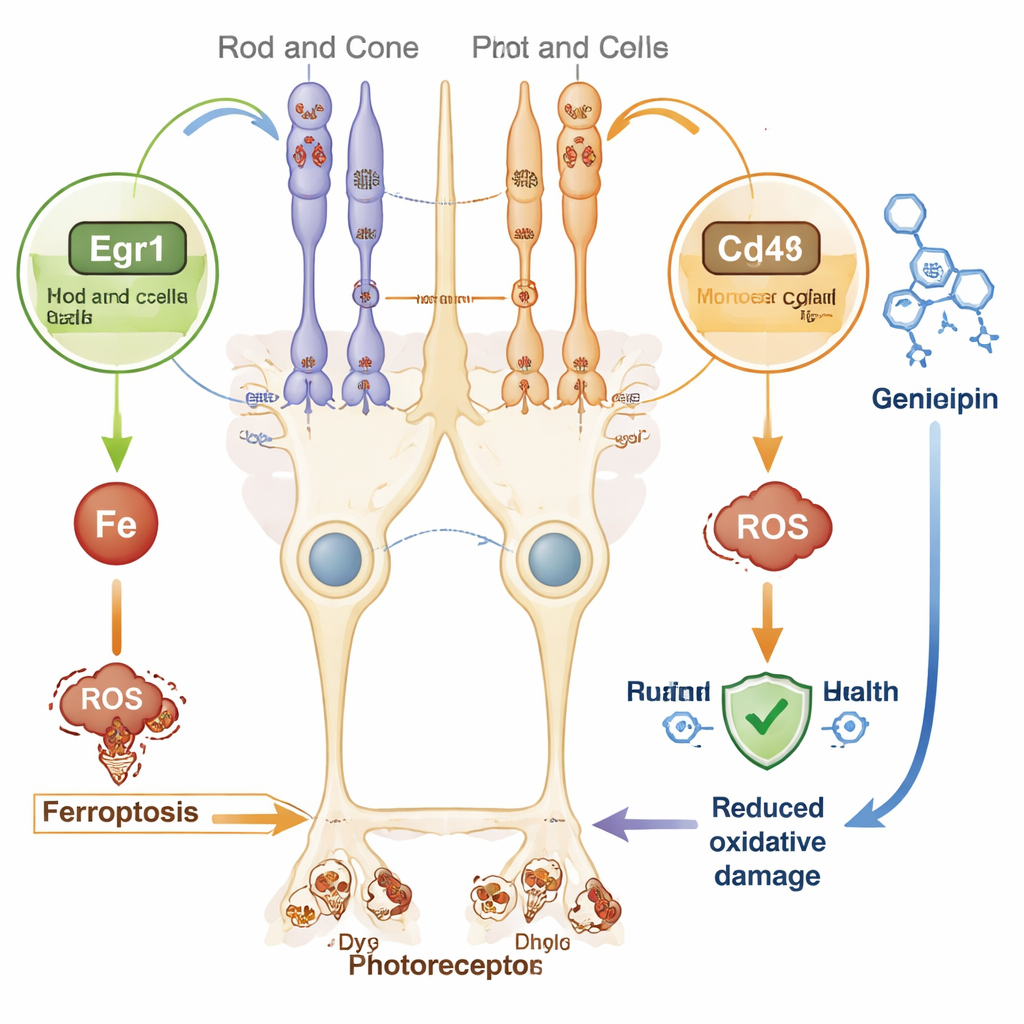
Qué significa esto para tratamientos futuros
Dado que la terapia génica adaptada a cada gen defectuoso es compleja y costosa, las estrategias de acción amplia resultan atractivas. La firma génica recién identificada sugiere varias de estas vías. Por ejemplo, Egr1 es un interruptor de respuesta rápida al estrés oxidativo que puede promover la ferroptosis en otros órganos. Cd44, una molécula de superficie en las células de Müller, ha demostrado en distintos tejidos agravar la sobrecarga de hierro y la muerte celular. Al mismo tiempo, la disminución de Ppara, un regulador del metabolismo lipídico y del uso de energía, puede dejar a las células retinianas más vulnerables al daño. Al dirigirse a estas vías de estrés compartidas, podría ser posible ralentizar la degeneración retiniana en muchas formas genéticas de retinitis pigmentosa.
Fármacos que podrían ayudar a proteger la vista
Utilizando una base de datos de interacción fármaco‑gen, los autores buscaron compuestos que pudieran influir en Egr1 o Cd44. Surgieron varios fármacos existentes, incluido el compuesto natural genipina, que ha mostrado efectos protectores en modelos de enfermedad de Parkinson, degeneración nerviosa y retinopatía diabética al reducir el estrés oxidativo y la inflamación. Si bien ninguno de estos fármacos candidatos ha sido aún probado en este modelo concreto de ratón con retinitis pigmentosa, proporcionan puntos de partida prometedores para futuros estudios de laboratorio y en animales orientados a proteger a los fotorreceptores frente a la ferroptosis.
Conclusión para no especialistas
Este trabajo muestra que la muerte celular oxidativa impulsada por el hierro está estrechamente entrelazada con los cambios en la actividad génica observados en un modelo clásico de ceguera hereditaria. Al destacar ocho genes clave, y en particular el gene sensible al estrés Egr1 en fotorreceptores y Cd44 en células de Müller, el estudio traza un nuevo territorio para posibles terapias que no dependen de corregir un único gen mutado. Si experimentos futuros confirman que calmar la ferroptosis mediante estos objetivos puede mantener vivas a las células retinianas, podría abrir la puerta a tratamientos que beneficien a un amplio abanico de pacientes con pérdida progresiva de visión.
Cita: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
Palabras clave: retinitis pigmentosa, ferroptosis, fotoreceptores, degeneración retinal, Egr1 Cd44