Clear Sky Science · es
Metabolómica integrada y secuenciación 16S rRNA revelan el mecanismo de las flavonas totales de Abelmoschus manihot (L.) Medic contra la fibrosis hepática
Poder floral para un hígado cicatrizado
La cicatrización del hígado, o fibrosis, es un peligro silencioso que puede conducir lentamente a cirrosis e insuficiencia hepática. La medicina moderna aún carece de fármacos seguros y ampliamente eficaces para detener o revertir este proceso. Este estudio explora si compuestos naturales de las flores amarillo brillante de Abelmoschus manihot —una planta medicinal tradicional china ya empleada para enfermedades renales— pueden proteger el hígado frente a daños tóxicos crónicos, y cómo podrían hacerlo actuando tanto sobre la química corporal como sobre los microbios de nuestro intestino.
Un problema hepático global en aumento
Cientos de millones de personas en todo el mundo conviven con enfermedad hepática crónica causada por virus, alcohol, acumulación de grasa o toxinas. Cuando el hígado se lesiona una y otra vez, responde depositando tejido cicatricial, como una herida que nunca termina de curar. Con el tiempo, esta fibrosis puede endurecer el órgano, bloquear el flujo sanguíneo y progresar a cirrosis, una causa principal de muertes relacionadas con el hígado. Dado que muchos desencadenantes pueden impulsar este daño simultáneamente, los investigadores muestran especial interés en mezclas vegetales que actúen sobre varios objetivos a la vez, en lugar de fármacos de molécula única que solo afectan una vía.
Probando un remedio tradicional en ratones
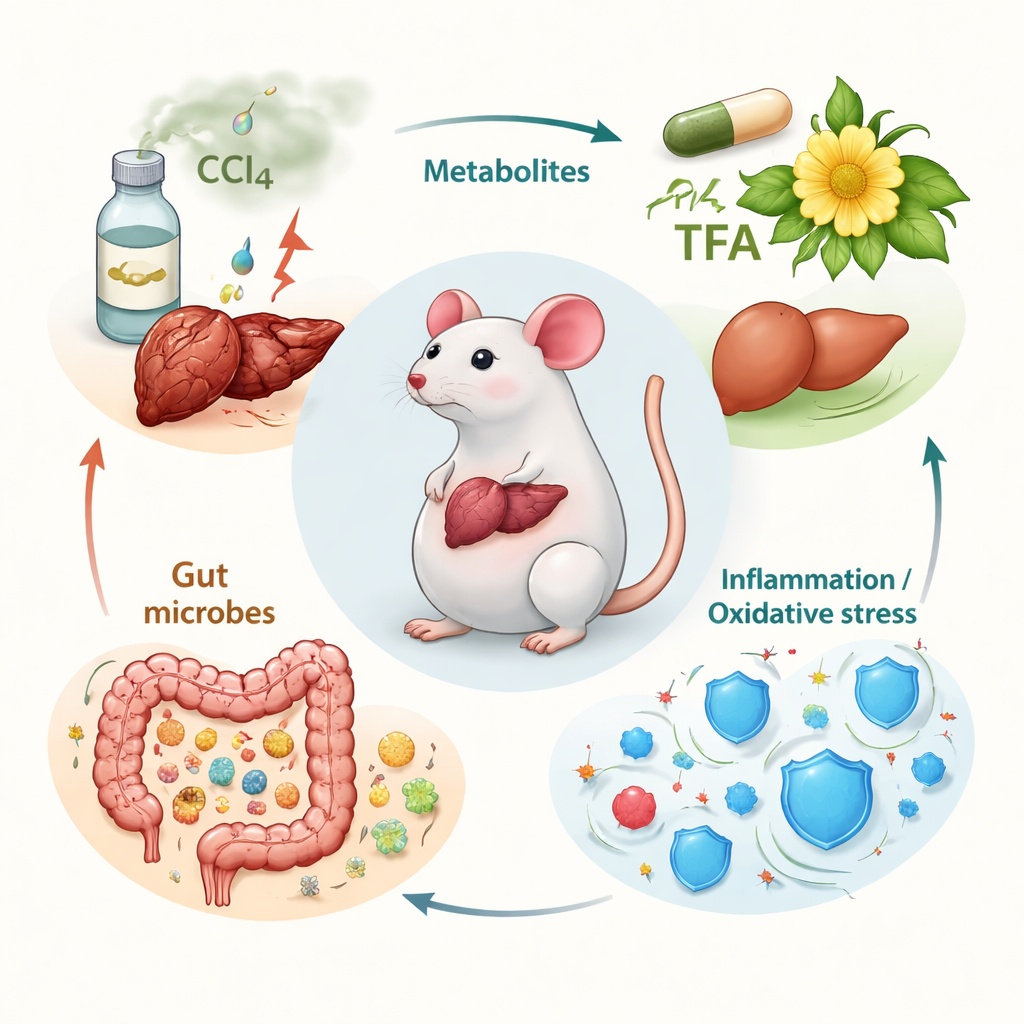
El equipo se centró en las “flavonas totales” de Abelmoschus manihot (TFA), una mezcla concentrada de siete compuestos vegetales relacionados que previamente se ha demostrado que son antiinflamatorios y antioxidantes. Utilizaron un modelo murino bien establecido en el que la exposición repetida al químico industrial tetracloruro de carbono (CCl4) provoca lesión hepática crónica y cicatrización similar a la fibrosis humana. Los ratones machos se dividieron en grupos: controles sanos, ratones “modelo” dañados con CCl4, un grupo con fármaco estándar y tres grupos con distintas dosis de TFA. Tras semanas de exposición a CCl4, los investigadores administraron TFA por vía oral y luego examinaron su sangre, tejido hepático y contenido intestinal.
Análisis sanguíneos más limpios y tejido hepático más sano
TFA mostró efectos protectores claros. Los niveles sanguíneos de las enzimas hepáticas ALT y AST —indicadores clínicos de daño celular hepático— aumentaron drásticamente en ratones expuestos a CCl4, pero se redujeron aproximadamente a la mitad en los animales tratados con TFA. El examen microscópico confirmó la misma tendencia: los hígados fibrosos no tratados mostraron arquitectura distorsionada, células muertas, depósitos intensos de colágeno y enjambres de células inflamatorias. Los hígados tratados con TFA presentaron menos “seudolóbulos” cicatriciales, menor tinción de colágeno y signos reducidos de muerte celular. También mejoraron marcadores de estrés oxidativo: las defensas antioxidantes (SOD y GSH‑Px) aumentaron, mientras que los subproductos dañinos (MDA) descendieron. Mensajeros inflamatorios clave, incluidos TNF‑α, IL‑6 y TGF‑β1, también disminuyeron, junto con marcadores químicos de fibrosis como la hidroxiprolina, el colágeno IV y el ácido hialurónico.
Reequilibrando la química corporal y los microbios intestinales
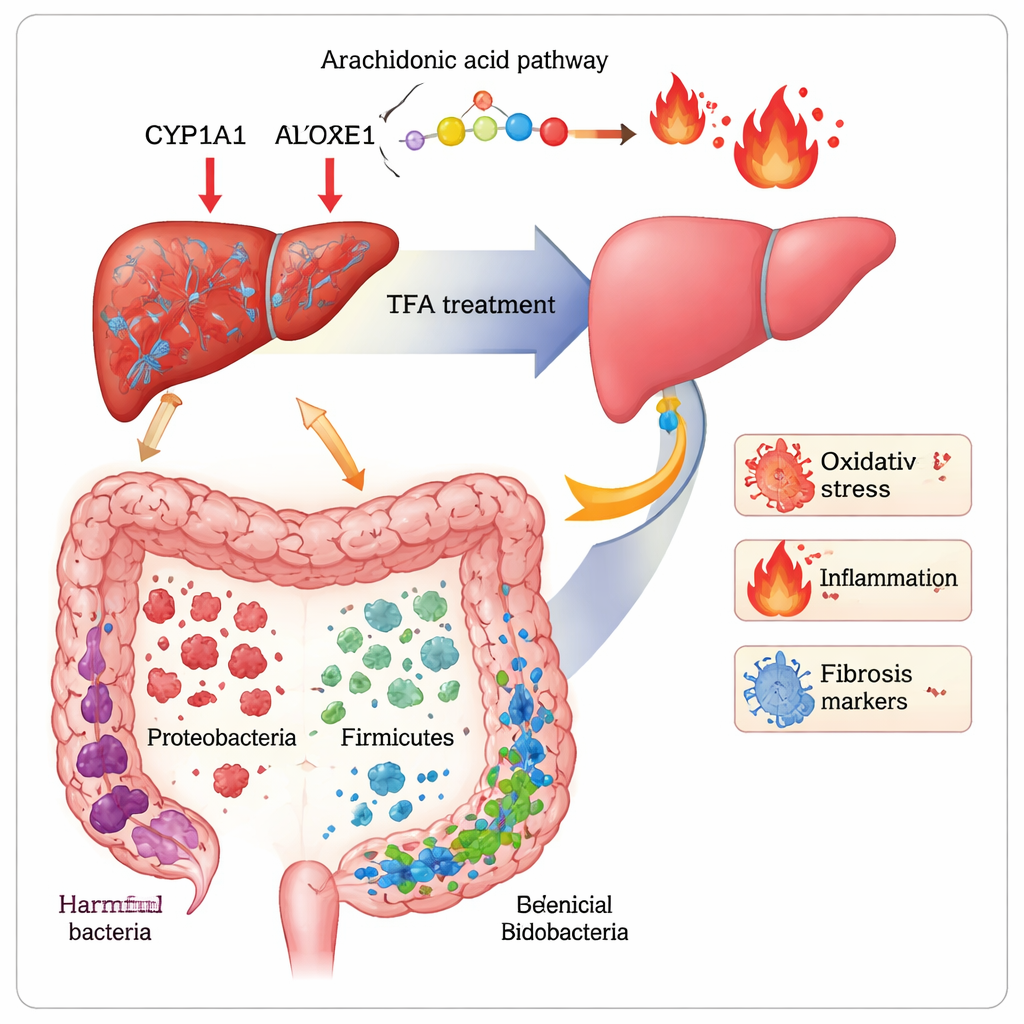
Para descubrir cómo TFA produce estos beneficios, los investigadores combinaron dos herramientas potentes: metabolómica, que perfila cientos de pequeñas moléculas en la sangre, y secuenciación 16S rRNA, que mapea los tipos de bacterias en el intestino. En los ratones con fibrosis, docenas de metabolitos implicados en el manejo de grasas y la degradación de aminoácidos estaban alterados. TFA restableció en parte el equilibrio en vías relacionadas con las membranas celulares (glicerofosfolípidos), el aminoácido relacionado con el estado de ánimo triptófano y un ácido graso llamado ácido araquidónico que alimenta señales inflamatorias. Los niveles de dos productos del ácido araquidónico, 20‑HETE y 16(R)‑HETE —ambos ligados al estrés oxidativo y la fibrosis— se acercaron a la normalidad. En el hígado, TFA redujo la abundancia de tres enzimas (CYP1A1, CYP2E1, ALOX15) que contribuyen a generar estas moléculas dañinas. Al mismo tiempo, el CCl4 alteró la microbiota intestinal, reduciendo grupos beneficiosos como Firmicutes, Lactobacillus y Bifidobacterium y permitiendo que prosperen potencialmente Proteobacteria perjudiciales. TFA revirtió gran parte de este cambio, aumentando la diversidad y restaurando bacterias “amigables” asociadas a mejor función de la barrera intestinal y menor inflamación.
Una estrategia multitarget en la autopista intestino–hígado
Al vincular cambios bacterianos con químicos sanguíneos y marcadores de enfermedad, el estudio sugiere que TFA actúa a lo largo del “eje intestino–hígado”: la transitada autopista de señales, nutrientes y toxinas que viajan del intestino al hígado. Las bacterias y sus productos nocivos parecen acompañar niveles más altos de inflamación y cicatrización, mientras que los microbios beneficiosos se correlacionan con perfiles metabólicos más saludables y menos fibrosis. TFA parece empujar todo este sistema de vuelta hacia el equilibrio: fortalece las defensas antioxidantes, calma las vías inflamatorias alimentadas por el ácido araquidónico, remodela la comunidad microbiana intestinal y, en última instancia, atenúa la respuesta de cicatrización en el hígado.
Qué podría significar esto para tratamientos futuros
Para el público general, el mensaje clave es que un extracto floral usado durante largo tiempo en la medicina tradicional mostró una promesa real en una prueba moderna y rigurosa de cicatrización hepática crónica. En ratones, TFA hizo más que proteger las células hepáticas: redujo la química tóxica y los microbios dañinos al mismo tiempo. Aunque estos resultados aún no prueban beneficio en humanos, y se obtuvieron solo en animales machos usando un tipo de lesión hepática, ponen de relieve una posible terapia multitarget que trabaja con las redes del organismo en lugar de contra una única molécula. Con más estudios, estas flavonas de origen vegetal podrían algún día formar parte de una caja de herramientas más amplia para ralentizar o incluso revertir la fibrosis hepática.
Cita: Li, D., Ge, H., Zhang, Y. et al. Integrated metabolomics and 16S rRNA sequencing reveal the mechanism of total flavones of Abelmoschus manihot (L.) Medic against liver fibrosis. Sci Rep 16, 7342 (2026). https://doi.org/10.1038/s41598-026-38192-5
Palabras clave: fibrosis hepática, microbiota intestinal, metabolómica, flavonoides, medicina tradicional china