Clear Sky Science · es
INHBA: un gen relacionado con la mitocondria y el pan‑muerte celular asociado al pronóstico y la inmunidad del CSOC
Por qué esto importa en el cáncer de boca
El carcinoma escamoso oral, una forma común de cáncer de boca, puede privar a las personas de capacidades básicas como hablar, comer e incluso sonreír con comodidad. A pesar de la cirugía, la radiación y la quimioterapia, muchos pacientes siguen afrontando recidivas y una supervivencia a largo plazo deficiente. Este estudio ofrece una mirada nueva al cáncer de boca centrada en cómo un único gen, llamado INHBA, contribuye a moldear la muerte celular, el vecindario de células de soporte del tumor y el éxito o fracaso de tratamientos modernos como la inmunoterapia.
Una mirada más detallada a un cáncer de boca letal
La mayoría de los tumores de cabeza y cuello comienzan en el revestimiento de la boca, y más del 90% de ellos son carcinoma escamoso oral (CSOC). A nivel mundial, los casos y las muertes por CSOC aumentan y se espera que crezcan alrededor de un 40% para 2040. La atención estándar se basa en cirugía más radiación y quimioterapia, pero muchos tumores resisten el tratamiento y reaparecen. Las inmunoterapias más recientes, que buscan activar las defensas del propio cuerpo, benefician solo a una fracción de los pacientes. Para avanzar más allá del ensayo y error en el tratamiento, los investigadores necesitan entender qué genes impulsan el CSOC y cómo interactúan con el sistema inmune.
Muerte celular, centrales energéticas y una nueva categoría de genes
Nuestras células están programadas para morir por varios mecanismos cuidadosamente regulados, incluidos procesos con nombres como apoptosis, autofagia, ferroptosis y otros. En el cáncer, estos programas de muerte suelen reconfigurarse para que las células tumorales sobrevivan cuando no deberían. El equipo detrás de este estudio se centró en un amplio grupo que llaman genes de “pan‑muerte celular”: genes que se sitúan en el cruce de distintas vías de muerte —y afinó aún más su búsqueda hacia los vinculados a las mitocondrias, las pequeñas centrales energéticas de la célula. Al combinar grandes bases de datos públicas de cáncer con un catálogo especializado de genes mitocondriales, definieron un conjunto de “genes de pan‑muerte asociados a mitocondrias” y buscaron cuáles estaban más fuertemente vinculados al comportamiento del CSOC y al resultado de los pacientes.
Encontrando INHBA entre muchos sospechosos
Usando estadística avanzada y nueve algoritmos de aprendizaje automático diferentes, los investigadores filtraron miles de genes e identificaron 19 genes mitocondriales de pan‑muerte con fuertes lazos con el pronóstico en CSOC. Entre ellos, INHBA destacó. Su actividad fue consistentemente mayor en muestras tumorales que en tejido oral normal y se asoció con una peor supervivencia tanto en CSOC como en el conjunto más amplio de tumores de cabeza y cuello. Al dividir los tumores en grupos de INHBA alto y bajo, los de niveles más altos mostraron señales biológicas más agresivas, incluidas vías relacionadas con la invasión tisular, la angiogénesis y el estrés mitocondrial. Pruebas de laboratorio en muestras de pacientes confirmaron que los niveles de ARNm de INHBA estaban realmente elevados en tumores del mundo real.
El papel escondido de las células de soporte alrededor del tumor
Para entender dónde actúa INHBA con más intensidad, el equipo recurrió a la secuenciación de ARN de célula única y la transcriptómica espacial, tecnologías que mapean la actividad génica en células individuales y a través de cortes de tejido. Encontraron que INHBA no es producido principalmente por las células cancerosas en sí, sino por fibroblastos asociados al cáncer: células de soporte que remodelan el tejido y configuran el entorno inmunitario. Un subtipo particular, llamado fibroblastos miofibroblásticos (myCAF), mostró niveles especialmente altos de INHBA. Mapas detallados de comunicación sugirieron que los fibroblastos ricos en INHBA dialogan intensamente con células inmunes y tumorales, ayudando a crear un nicho inmunosupresor y parecido a una cicatriz alrededor del cáncer. Este microambiente parece favorecer el crecimiento tumoral y puede atenuar algunas formas de inmunoterapia.
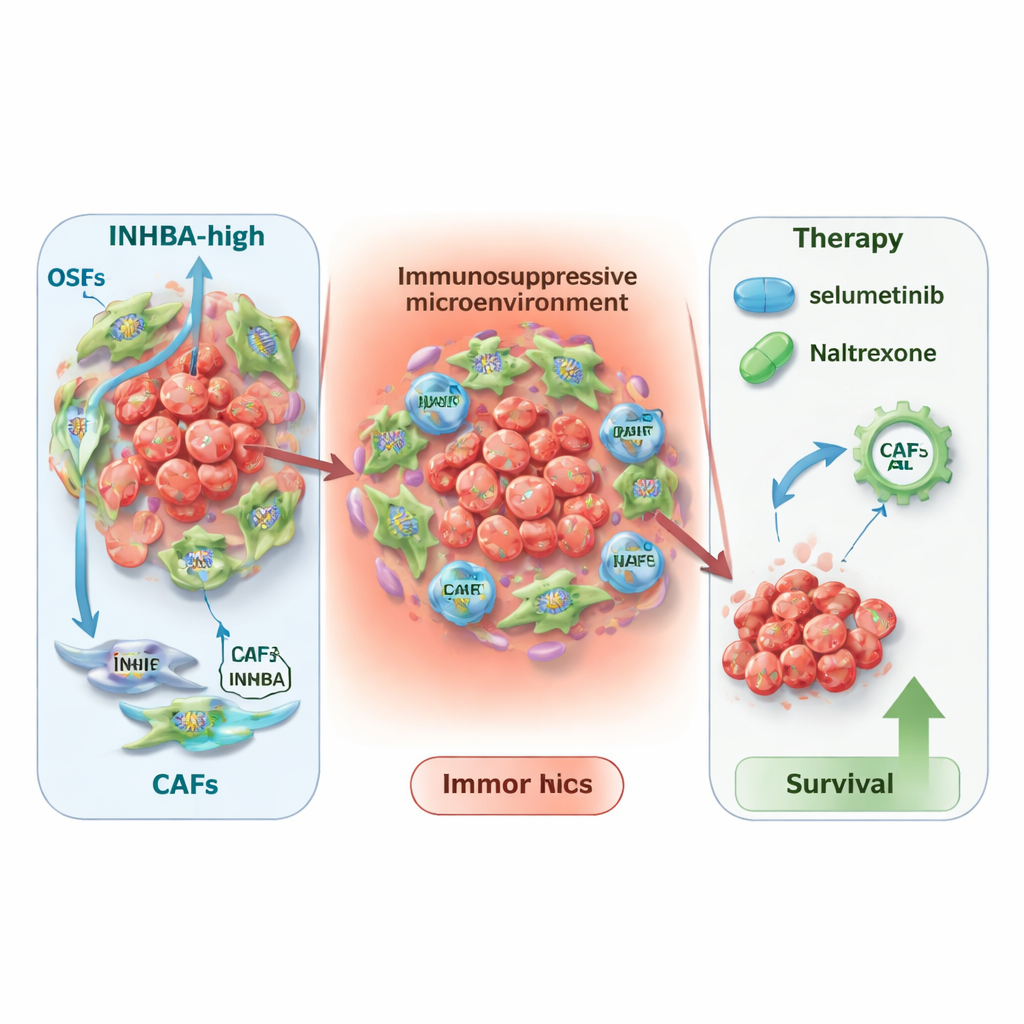
Nuevos ángulos de tratamiento e impacto más amplio
Sabiendo que INHBA marca un vecindario tumoral más peligroso, los investigadores exploraron cómo esto podría orientar la terapia. En pacientes que recibieron inmunoterapia, niveles bajos de INHBA se asociaron con mejores resultados con fármacos comunes que apuntan a PD‑L1 o CTLA4, mientras que niveles altos de INHBA parecían predecir mayor beneficio de enfoques con células CAR‑T. Al explorar dos grandes bases de datos de respuesta a fármacos, también señalaron dos medicamentos existentes —selumetinib y naltrexona— como especialmente prometedores en tumores con INHBA alto. Modelos computacionales mostraron que ambos fármacos podrían unirse fuertemente a la proteína INHBA, sugiriendo un efecto directo. Finalmente, un análisis pancáncer reveló que INHBA está elevado y vinculado a mala supervivencia en muchos otros tipos tumorales, lo que sugiere que su importancia va más allá del cáncer de boca.
Qué significa esto para los pacientes
En términos sencillos, este estudio identifica a INHBA como un gen “interruptor maestro” que ayuda a que los tumores orales letales crezcan, se diseminen y evadan el sistema inmune, actuando en gran medida a través de células de soporte especializadas más que solo por las células cancerosas. Medir INHBA en los tumores podría ayudar a los médicos a identificar a pacientes de alto riesgo, predecir quién se beneficiará de distintos tipos de inmunoterapia y elegir fármacos dirigidos que puedan funcionar mejor en este contexto. Dado que INHBA desempeña un papel dañino similar en varios otros cánceres, las terapias dirigidas a este gen y a sus socios fibroblásticos podrían finalmente beneficiar a una amplia gama de pacientes, acercando la atención a tratamientos precisos y personalizados.
Cita: Zhang, X., Sun, M., Qiu, T. et al. INHBA: a mitochondrial-related pan-cell death gene associated with the prognosis and immunity of OSCC. Sci Rep 16, 7642 (2026). https://doi.org/10.1038/s41598-026-38131-4
Palabras clave: carcinoma escamoso oral, INHBA, microambiente tumoral, fibroblastos asociados al cáncer, inmunoterapia