Clear Sky Science · es
Nanopartículas de albúmina sérica bovina mejoran la estabilidad de bacteriófagos y su actividad antimicrobiana frente a Pseudomonas aeruginosa
Por qué importa proteger a los virus beneficiosos
A medida que aumenta la resistencia a los antibióticos, los médicos agotan las opciones para tratar infecciones peligrosas. Un culpable persistente es Pseudomonas aeruginosa, una bacteria que a menudo infecta los pulmones de personas con defensas debilitadas y que puede resistir muchos fármacos. Este estudio explora una estrategia creativa: usar virus beneficiosos que atacan bacterias, llamados bacteriófagos, y protegerlos dentro de pequeñas esferas proteicas hechas a partir de una proteína sanguínea común, la albúmina sérica bovina (BSA). El objetivo es mantener estos virus estables y activos el tiempo suficiente para combatir mejor las difíciles infecciones pulmonares.
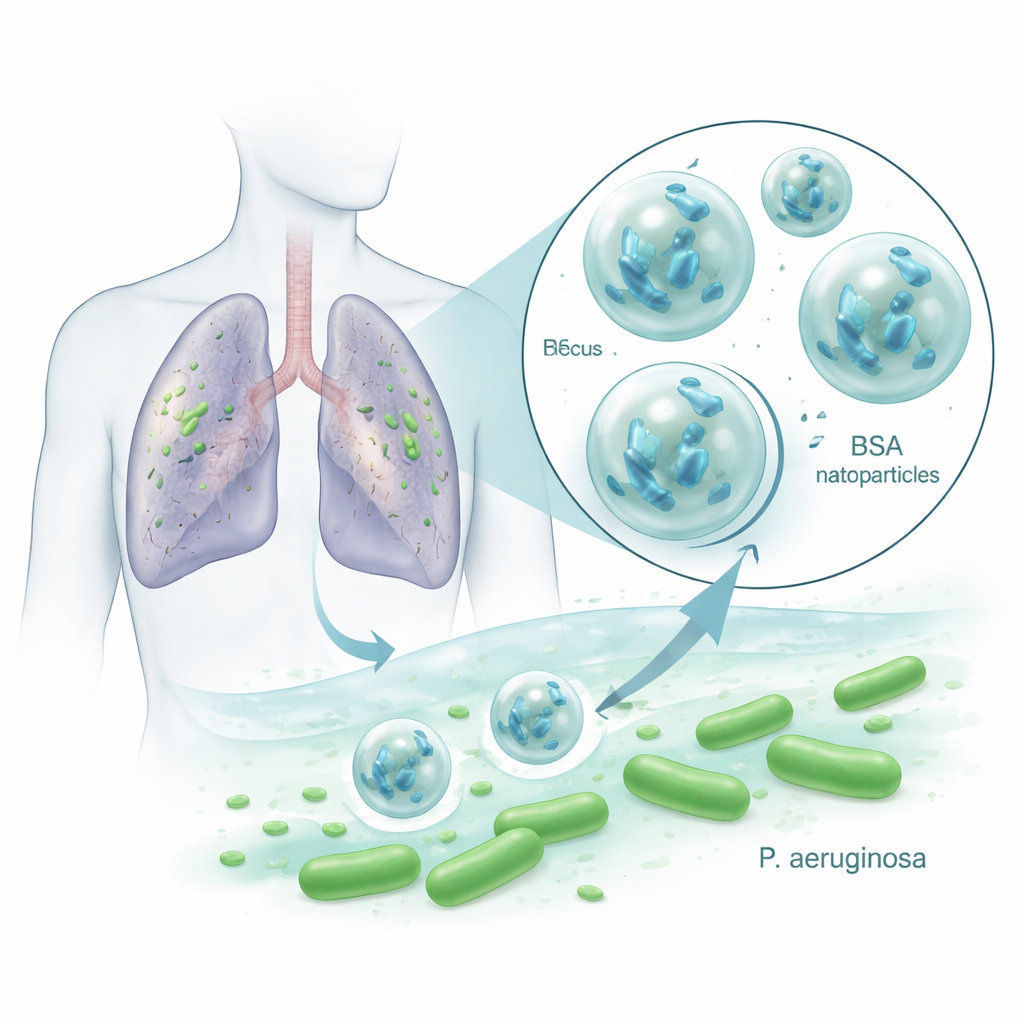
Pequeños aliados contra gérmenes pulmonares persistentes
Pseudomonas aeruginosa es famosa en hospitales porque resiste múltiples antibióticos y forma biofilms viscosos que la protegen del tratamiento. Los bacteriófagos, o fagos, son virus que infectan y hacen estallar bacterias específicas mientras dejan en gran medida intactas las células humanas y los microbios beneficiosos. Pueden multiplicarse dondequiera que su hospedador bacteriano esté presente, lo que los convierte en un complemento o alternativa atractiva a los antibióticos. Pero los fagos son frágiles: el calor, la acidez, las enzimas y el sistema inmunitario pueden inactivarlos rápidamente, lo que ha limitado su éxito en pacientes reales. Los investigadores se preguntaron si empaquetar un fago que mata Pseudomonas llamado VAC1 dentro de nanopartículas de BSA podría protegerlo y hacer los tratamientos más eficaces.
Construyendo una cubierta proteica protectora
El equipo primero tuvo que diseñar una partícula que no dañara al fago. Probaron disolventes comunes usados para formar nanopartículas de BSA y encontraron que etanol y metanol destruyeron a VAC1, mientras que la acetona no lo hizo, por lo que usaron acetona en su proceso. Mezclaron el fago con una solución de BSA y luego añadieron cuidadosamente acetona para hacer que la proteína se agregara en esferas a escala nanométrica, estabilizándolas con un agente entrecruzante químico. Estas partículas cargadas con fago, llamadas NPPha, tuvieron un diámetro medio de alrededor de 220 nanómetros —mucho más pequeñas que una célula humana— y atraparon más del 95% del fago en su interior. Imágenes por microscopía electrónica mostraron partículas de BSA de forma irregular que contenían regiones más densas que probablemente correspondían al fago, y las pruebas confirmaron que virus activos se liberaban de forma lenta durante al menos dos días a temperatura corporal sin perder infectividad.
Mayor poder bactericida en el laboratorio
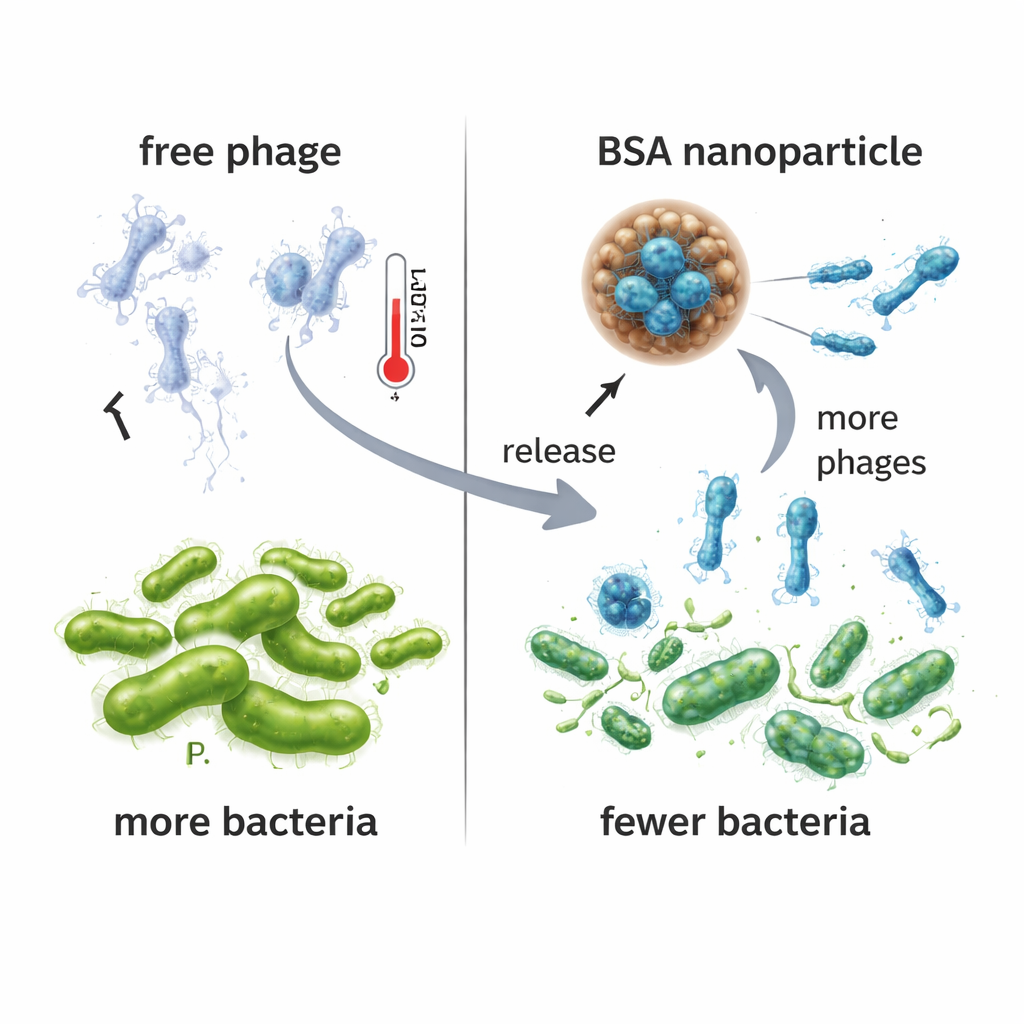
Los investigadores compararon luego qué tan bien VAC1 libre y NPPha controlaban Pseudomonas en cultivo líquido. Cuando las bacterias se expusieron a NPPha, su crecimiento se suprimió mucho más que con el mismo fago administrado solo o con nanopartículas vacías. En 24 horas, los cultivos tratados con NPPha produjeron aproximadamente cien mil veces más partículas de fago nuevas que los cultivos tratados con VAC1 libre, lo que sugiere que la liberación sostenida desde las nanopartículas generó una batalla virus-bacteria más prolongada. Es importante que las nanopartículas de BSA —tanto cargadas con fago como vacías— no dañaran células humanas derivadas del hígado en pruebas de toxicidad, lo que respalda su seguridad potencial como vehículo de entrega. Experimentos de estabilidad a 37 °C mostraron que el fago libre perdió rápidamente actividad en dos días, mientras que el fago dentro de NPPha permaneció infectivo hasta cinco días.
Probando el enfoque en ratones infectados
Para ver si estos beneficios se traducían en animales vivos, el equipo usó un modelo murino de infección pulmonar aguda por Pseudomonas. Los ratones fueron infectados por la nariz y, una hora después, tratados con NPPha, VAC1 libre, nanopartículas vacías o una solución salina. En este modelo muy severo, todos los animales, independientemente del tratamiento, murieron en 12 horas, por lo que la supervivencia no mejoró. Sin embargo, al examinar los pulmones, encontraron que los ratones tratados con NPPha tenían menos bacterias y era más probable que aún presentaran fagos detectables que los tratados con VAC1 libre. Cortes de tejido de pulmones tratados con NPPha mostraron menos daño estructural, paredes más finas entre los alvéolos y menor acumulación de células inflamatorias en comparación con otros grupos infectados, lo que indica que la infección se vio algo atenuada aunque no lo suficiente para salvar a los animales en estas condiciones tan duras.
Qué significa esto para futuros tratamientos de infecciones
Para no especialistas, el mensaje clave es que empaquetar bacteriófagos dentro de pequeñas burbujas proteicas puede mantenerlos vivos y potentes por más tiempo, ayudándoles a atacar mejor bacterias de difícil tratamiento como Pseudomonas aeruginosa. En placas de cultivo y en pulmones de ratón, las nanopartículas de BSA aumentaron el número de fagos, redujeron el crecimiento bacteriano y atenuaron el daño pulmonar, aunque aún no previnieron la muerte en un modelo de infección muy agresivo. El trabajo sugiere que las nanopartículas de albúmina ofrecen una vía simple, de bajo coste y aparentemente segura para estabilizar fagos terapéuticos. Con una dosificación y un momento más refinados, y quizá su uso en infecciones menos extremas o más crónicas, los fagos nanoempaquetados podrían convertirse en una herramienta valiosa junto a los antibióticos en la lucha contra bacterias multirresistentes.
Cita: Cunha, G.A.d., Marangoni, G.S., Durante, M.F.R. et al. Bovine serum albumin nanoparticles improve bacteriophage stability and antimicrobial activity against Pseudomonas aeruginosa. Sci Rep 16, 7146 (2026). https://doi.org/10.1038/s41598-026-38106-5
Palabras clave: terapia con fagos, nanopartículas, Pseudomonas aeruginosa, resistencia a los antibióticos, infección pulmonar