Clear Sky Science · es
Obinutuzumab induce la desestabilización lisosomal mediante la inhibición dependiente de esfingomielina de TRPML2
Por qué importa esta historia sobre anticuerpos
Para muchas personas con linfomas de células B, los medicamentos basados en anticuerpos han convertido un diagnóstico que antes era casi siempre mortal en una enfermedad tratable. Sin embargo, no todos los anticuerpos son iguales: algunos destruyen las células tumorales con más potencia y fiabilidad que otros. Este trabajo explora por qué un fármaco de este tipo, obinutuzumab, es mejor para matar directamente las células del linfoma que su predecesor rituximab, investigando a fondo un culpable inesperado en el interior de la célula: los propios centros de reciclaje celular, llamados lisosomas, y un delicado equilibrio de lípidos y canales iónicos en sus membranas.
Del objetivo en la superficie al autodescenso interno
Tanto rituximab como obinutuzumab reconocen el mismo blanco en las células B, una proteína llamada CD20. Pero los autores muestran que obinutuzumab se internaliza en la célula de forma mucho más rápida y eficiente. Una vez ligado a CD20 en la superficie de la célula tumoral, los complejos anticuerpo‑receptor son atraídos hacia el interior mediante un proceso endocítico y entregados a compartimentos ácidos, incluidos los lisosomas. Allí, obinutuzumab provoca la permeabilización de la membrana lisosomal: la membrana lisosomal, normalmente resistente, se vuelve permeable, permitiendo que enzimas digestivas como las catepsinas se filtren en la célula e inicien rutas de muerte celular. Cambios en el equilibrio de sales y agua de estos compartimentos, que hacen que los lisosomas se hinchen, amplifican considerablemente este efecto letal.
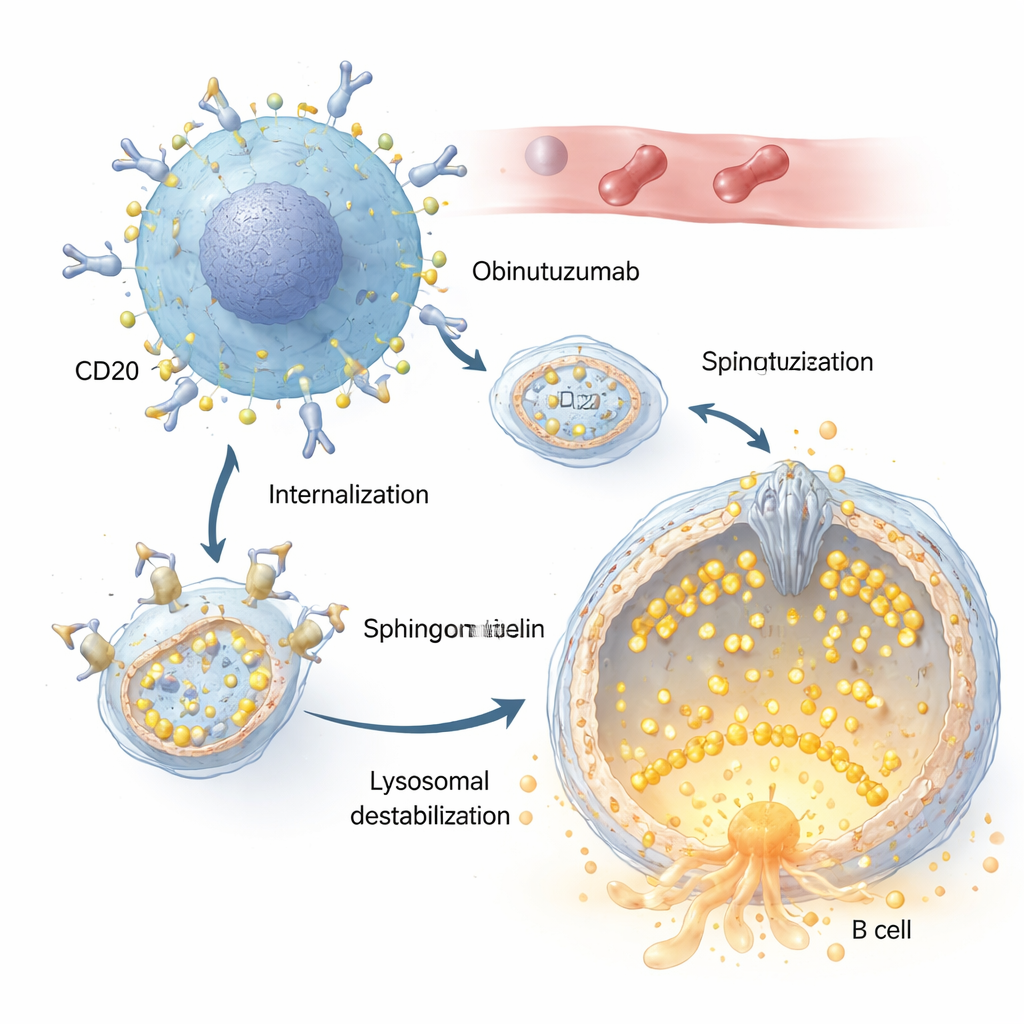
El papel de un pequeño canal guardián
En el centro de esta historia está TRPML2, un canal de calcio integrado en la membrana lisosomal. En condiciones normales, TRPML2 ayuda a los lisosomas a afrontar el estrés mecánico y osmótico liberando calcio, lo que favorece la reparación de la membrana, el tráfico y el control del volumen. Utilizando una combinación de colorantes fluorescentes para calcio y versiones de TRPML2 diseñadas para detectar calcio, los investigadores muestran que obinutuzumab cierra rápidamente este canal: a los pocos minutos del tratamiento, un fármaco que normalmente abre canales TRPML ya no provoca un estallido de calcio. Enfoques genéticos que reducen los niveles de TRPML2, o inhibidores de pequeñas moléculas que bloquean la actividad de TRPML, aumentan la vulnerabilidad de las células de linfoma frente a obinutuzumab, provocando más filtraciones lisosomales y mayores tasas de muerte celular directa.
Cómo los lípidos de la membrana inclinan la balanza
El estudio plantea entonces qué conecta la captación del anticuerpo con el cierre del canal. La atención se dirige a la esfingomielina, un lípido abundante en las membranas celulares que se sabe que interfiere con los canales TRPML. Mediante una sonda fluorescente que se une a la esfingomielina, los autores encuentran que las vesículas que contienen obinutuzumab son ricas en esfingomielina una vez que alcanzan compartimentos ácidos, mucho más que las vesículas que contienen rituximab. Cuando las células se tratan con esfingomielinasa, una enzima que elimina esfingomielina, la actividad liberadora de calcio de TRPML2 se restablece incluso en presencia de obinutuzumab. En estas condiciones, los lisosomas son menos propensos a filtrar y mueren menos células, lo que sugiere con fuerza que la acumulación de esfingomielina inactiva TRPML2 y prepara a los lisosomas para romperse.
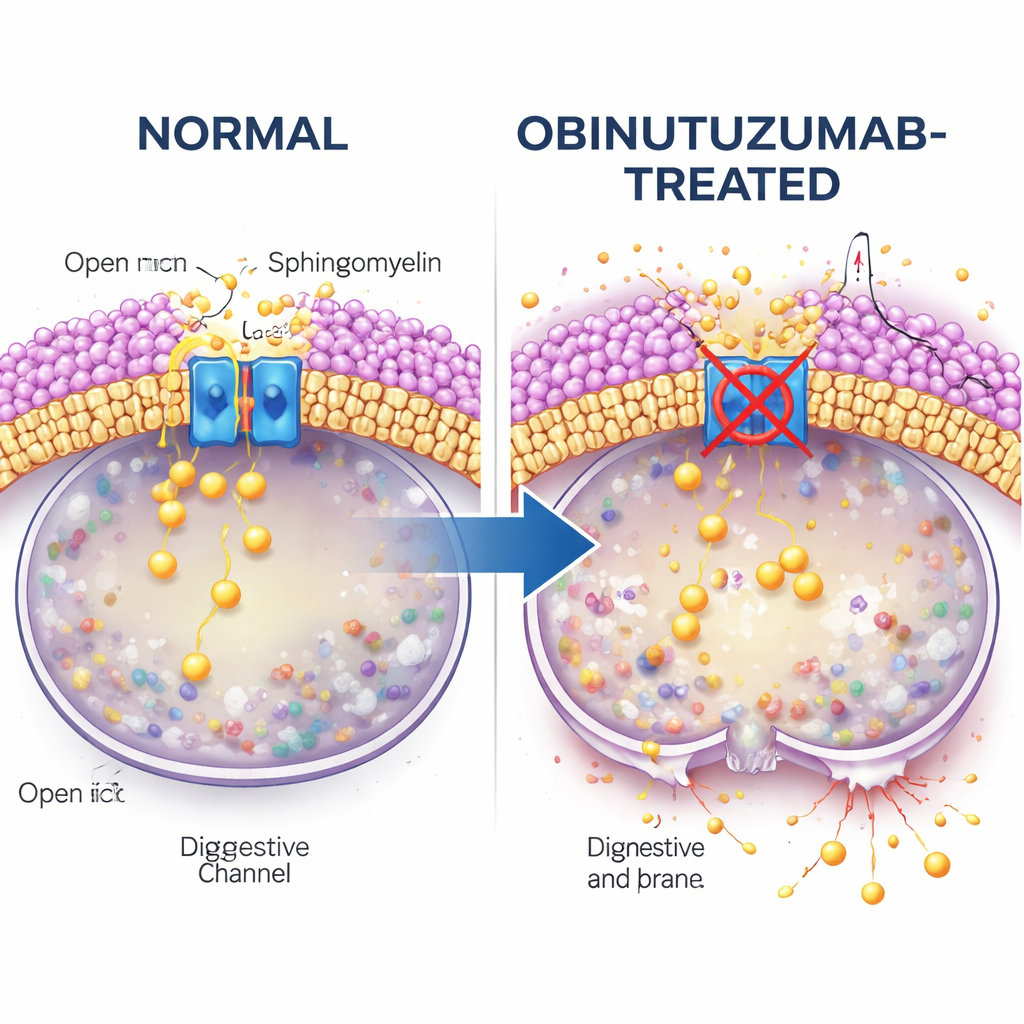
Rutas de tráfico y controles de colesterol
La vía que recorre obinutuzumab hacia el interior de la célula también importa. La microscopía electrónica y el marcado de anticuerpos sensible al pH revelan que obinutuzumab abandona la superficie celular y entra en vesículas intracelulares más rápido que rituximab. Cuando los investigadores interfieren con rutas de captación específicas, encuentran que bloquear una forma de endocitosis dependiente de colesterol (con un compuesto llamado filipina) impide que obinutuzumab apague TRPML2, y reduce parcialmente el daño lisosomal y la muerte celular. Otros inhibidores de endocitosis no muestran este efecto protector. Esto apunta a una vía especializada, rica en colesterol y esfingomielina, que entrega obinutuzumab a los lisosomas de una manera que configura la inhibición de TRPML2 y la posterior desestabilización de la membrana.
Qué significa esto para futuros tratamientos contra el cáncer
En términos sencillos, este trabajo muestra que obinutuzumab mata los linfomas de células B con tanta eficiencia porque lleva a sus lisosomas a un estado frágil. Al dirigir los complejos anticuerpo‑CD20 a compartimentos ricos en esfingomielina, el fármaco apaga indirectamente un canal protector de calcio, TRPML2. Una vez que esa protección desaparece, los lisosomas tienen más probabilidades de estallar bajo estrés, vertiendo enzimas corrosivas que desmantelan la célula tumoral desde dentro. Comprender este eje lípido‑canal iónico no solo explica por qué obinutuzumab supera a rituximab; también sugiere nuevas estrategias para potenciar las terapias con anticuerpos —por ejemplo, combinándolas con fármacos que alteren esfingolípidos o aumenten la actividad de TRPML2 para afinar cómo y cuándo los lisosomas de las células tumorales se autodestruyen.
Cita: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Palabras clave: obinutuzumab, linfoma de células B, lisosoma, esfingomielina, TRPML2