Clear Sky Science · es
Mejora de la cicatrización con nanofibras electrohiladas de PLA/PVA cargadas de roflumilast y L-arginina: fabricación, optimización y evaluación in vivo
Por qué importan los vendajes que aceleran la cicatrización
Cualquiera que haya sufrido un corte profundo, una incisión quirúrgica o una llaga crónica sabe que esperar a que la piel cierre puede ser lento, doloroso y arriesgado. Los médicos buscan apósitos que hagan más que cubrir la herida: quieren vendajes que modulen activamente la inflamación, alimenten el tejido en formación y mantengan la zona húmeda pero estable. Este estudio explora un nuevo tipo de vendaje “inteligente” hecho de fibras ultrafinas que transportan dos medicamentos distintos a la vez, diseñado para ayudar a la piel a cerrarse más rápido y con una reparación de mejor calidad.
Una malla de fibras microscópicas que imita el soporte de la piel
Los investigadores construyeron su vendaje a partir de una lámina aireada de nanofibras: filamentos miles de veces más finos que un cabello humano. Estas fibras forman una malla transpirable que se asemeja a la estructura de soporte natural de la piel, ofreciendo a las células un andamiaje para adherirse mientras crecen. Para fabricar esta malla, el equipo usó una técnica llamada electrohilado: mezclas de polímero líquido se estiran en fibras largas y finas mediante un campo de alta tensión y se recogen como una hoja blanda. Una de las soluciones se basó en PLA, un plástico resistente y de degradación lenta ya empleado en dispositivos médicos. La otra fue PVA, un material hidrofílico que se hincha y ayuda a mantener las heridas húmedas. 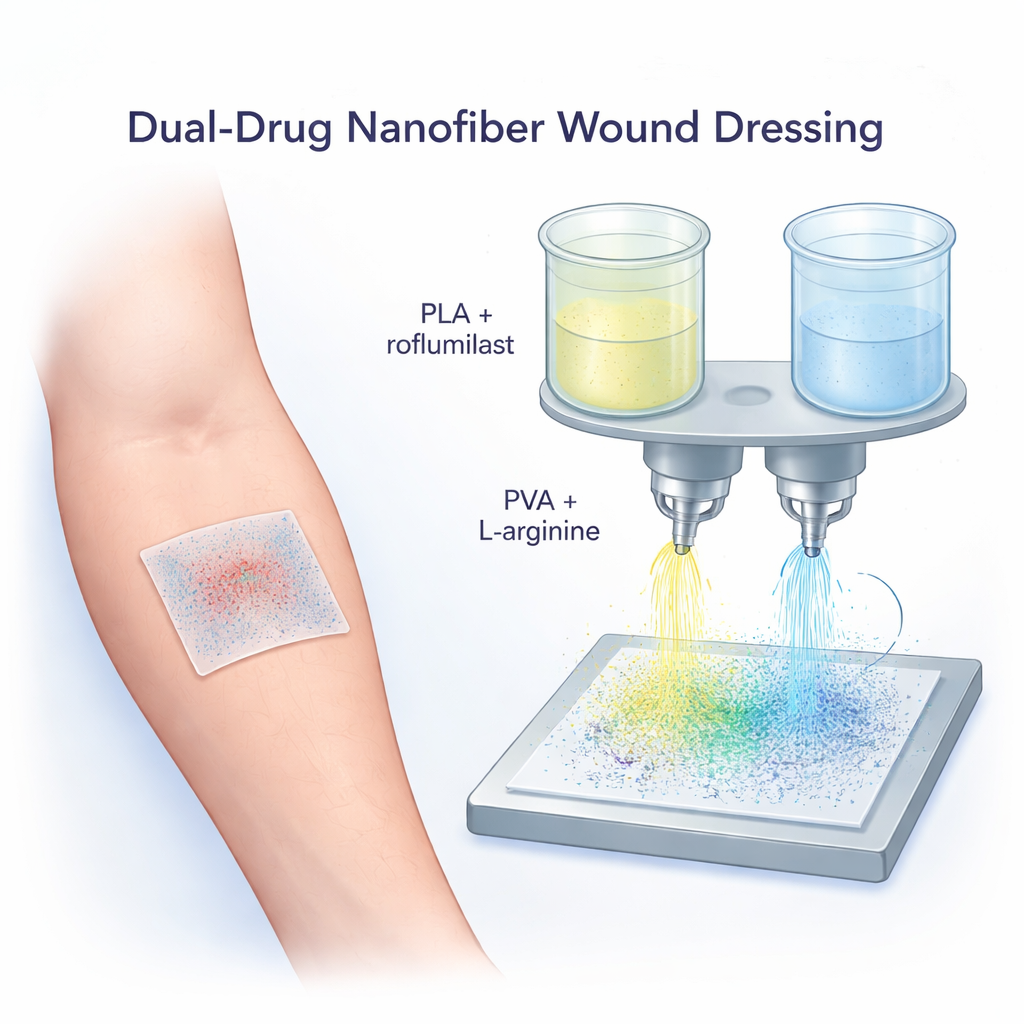
Combinar dos fármacos para un efecto de cicatrización en dos tiempos
Además del diseño de las fibras, el equipo cargó cada polímero con un fármaco diferente. Las fibras de PLA contenían roflumilast, un medicamento más conocido por tratar enfermedades pulmonares y psoriasis al reducir la inflamación en el organismo. Las fibras de PVA llevaban L-arginina, un aminoácido natural que el cuerpo utiliza para producir óxido nítrico, el cual aumenta el flujo sanguíneo, apoya a las células inmunitarias y ayuda a la formación de colágeno —todos pasos clave en la reparación cutánea. Al hilar ambas soluciones simultáneamente mediante dos boquillas, crearon una sola lámina donde los dos fármacos coexisten lado a lado en fibras separadas pero entretejidas, listas para liberarse de forma coordinada.
Evaluando la estructura y la gestión del agua del vendaje
Antes de probar en animales, los autores debían demostrar que los materiales eran seguros, estables y bien integrados. Con microscopios electrónicos observaron fibras lisas, sin perlas y de grosor uniforme, incluso después de la incorporación de los fármacos. Técnicas de identificación química confirmaron que ambos medicamentos estaban físicamente atrapados dentro de la matriz PLA/PVA sin formar compuestos indeseados. El análisis por rayos X mostró que, una vez dentro de las fibras, los fármacos pasaron de su forma cristalina habitual a un estado más desordenado u “amorfo”, que con frecuencia se disuelve más rápido y de forma más homogénea. El equipo también midió cómo las láminas absorbían agua. La versión con ambos fármacos se hinchó rápidamente —llegando a absorber más de seis veces su peso en seco inicialmente— y luego se estabilizó, lo que significa que puede absorber el exudado de la herida y mantener la humedad sin convertirse en un gel blando y frágil. 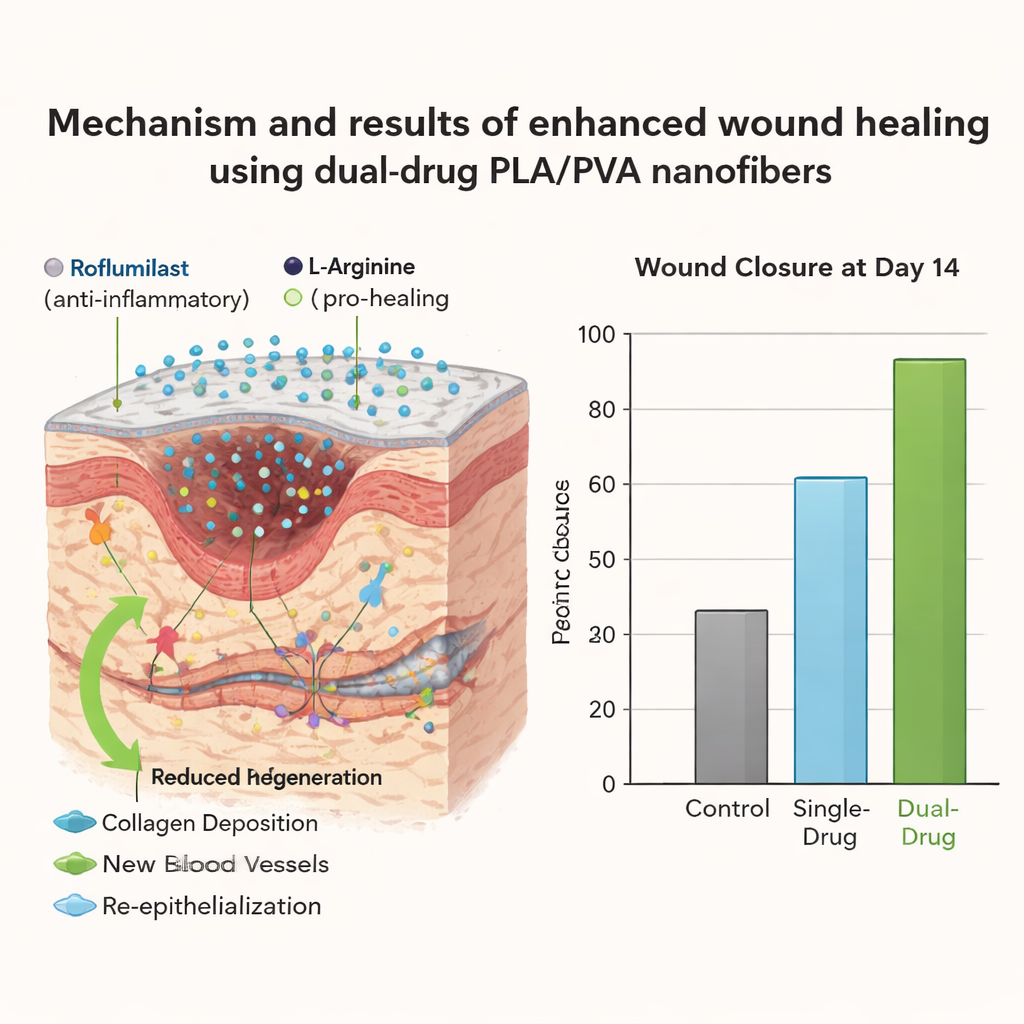
Probando el vendaje inteligente en heridas reales
Para comprobar si este diseño realmente mejora la cicatrización, los científicos trataron pequeñas heridas cutáneas circulares en ratas con diferentes versiones de las láminas de fibra: sin fármaco, solo roflumilast, solo L-arginina o ambos fármacos combinados. Otro grupo recibió únicamente gasa convencional. Durante dos semanas fotografiaron las heridas y midieron cuánto del área original abierta se había cerrado. Todas las láminas medicadas funcionaron mejor que la gasa sola, pero el vendaje con doble fármaco destacó claramente. Al día 14, las heridas cubiertas con las fibras combinadas de roflumilast y L-arginina estaban casi completamente cerradas, alcanzando aproximadamente un 99,8% de cicatrización, en comparación con un cierre mucho más lento en los grupos no tratados y en los de un solo fármaco.
Observando el interior de la piel para evaluar la calidad de la reparación
Cicatrizar no es solo cerrar un hueco: la calidad del tejido nuevo importa. Al examinar cortes finos de piel al microscopio, los grupos con gasa y algunos de los tratados con un solo fármaco aún mostraron “tejido de granulación”, un signo de reparación incompleta, aunque la superficie pareciera cerrada. En contraste, la piel tratada solo con roflumilast mostró tejido cicatricial más maduro, y el tratamiento con ambos fármacos obtuvo los mejores resultados. Estas muestras exhibieron tejido fibroso denso y organizado, regeneración completa de la capa externa de la piel, ausencia de tejido de granulación residual y solo una inflamación leve persistente, lo que sugiere una reparación más completa y robusta.
Qué podría significar esto para los vendajes del futuro
Para el público general, el mensaje es directo: al combinar un fármaco antiinflamatorio y un nutriente pro-cicatrización dentro de una malla de fibras cuidadosamente diseñada, este estudio creó un vendaje que ayudó a que las heridas en ratas se cerraran más rápido y de manera más completa que los apósitos estándar o las versiones con un solo fármaco. Aunque se necesitan más ensayos en humanos, el enfoque muestra cómo los vendajes de próxima generación podrían suministrar discretamente la mezcla adecuada de señales justo donde se necesitan, convirtiendo un simple recubrimiento en un socio activo de la cicatrización —y potencialmente mejorando la recuperación de pacientes con lesiones cutáneas de difícil curación.
Cita: Salim, S.A., Elbadry, A.M.M., Abdelazim, E.B. et al. Enhancing wound healing with synergistic dual-drug electrospun roflumilast and L-arginine loaded PLA/PVA nanofibers through fabrication, optimization, and in vivo assessment. Sci Rep 16, 7481 (2026). https://doi.org/10.1038/s41598-026-38086-6
Palabras clave: cicatrización de heridas, vendajes de nanofibras, liberación dual de fármacos, roflumilast, L-arginina