Clear Sky Science · es
Propiedades funcionales de las vesículas extracelulares derivadas de miotubos esqueléticos basadas en perfiles de microARN: un análisis comparativo con vesículas extracelulares derivadas de células madre mesenquimales
Mensajes musculares en paquetes diminutos
Nuestros músculos hacen mucho más que movernos: envían constantemente “mensajes de texto” moleculares a lo largo del organismo. Este estudio explora cómo se comparan las partículas diminutas liberadas por las células musculares con partículas similares procedentes de células madre ampliamente utilizadas en terapias futuras. Al decodificar las señales genéticas que transportan estas partículas, los autores plantean una pregunta práctica: ¿para qué tipos de enfermedades podrían ser más adecuadas las vesículas derivadas del músculo que las derivadas de células madre?
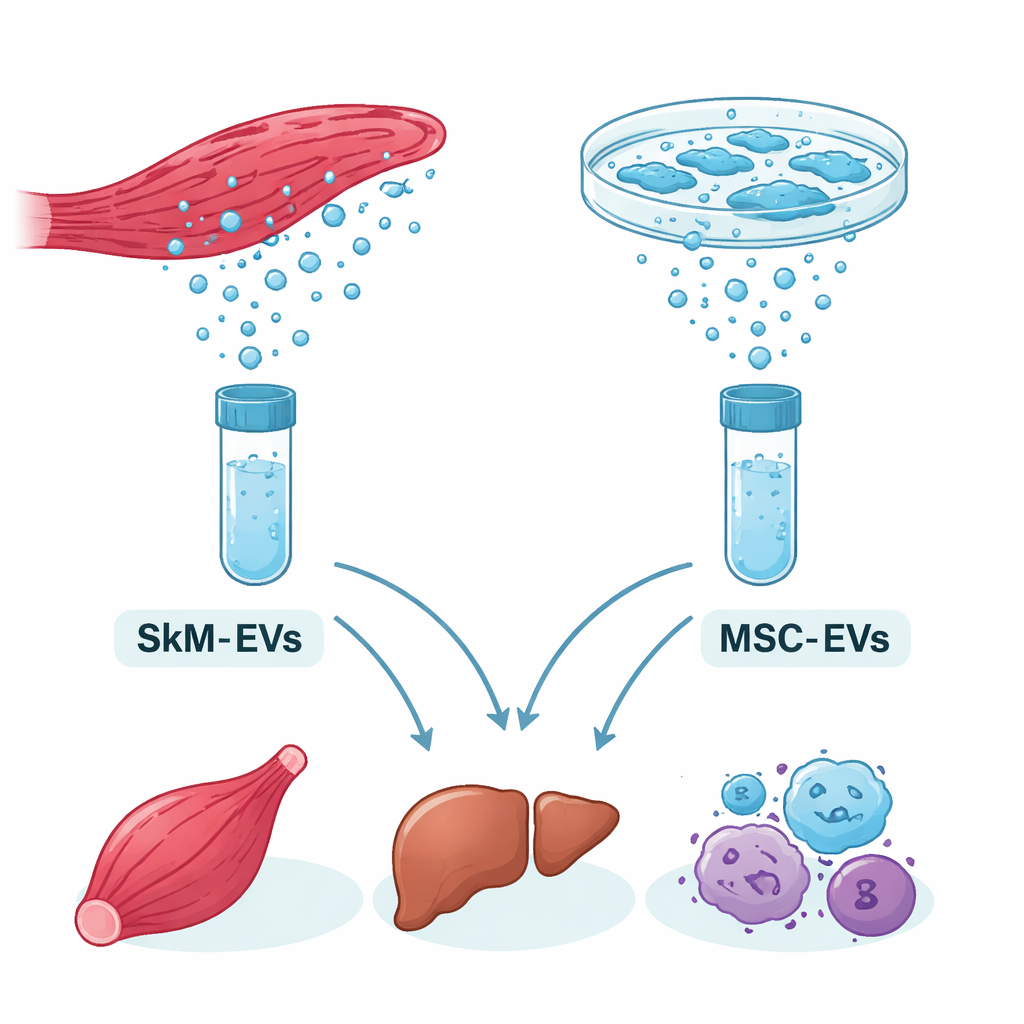
Pequeños mensajeros que viajan por el cuerpo
Todas las células liberan burbujas microscópicas llamadas vesículas extracelulares, o VE. Son paquetes de tamaño nanométrico envueltos en lípidos y cargados con moléculas. Un tipo clave de carga son los microARN: fragmentos cortos de ARN que ayudan a bajar o subir la expresión de genes, moldeando el comportamiento celular. El músculo esquelético, el tejido que genera movimiento, resulta ser el mayor órgano secretor del cuerpo y puede liberar grandes cantidades de VE, sobretodo cuando se estimula por vías no invasivas como el ultrasonido. Las células madre mesenquimales, en cambio, ya son un pilar en ensayos clínicos, y sus VE se prueban para reparación tisular y reducción de la inflamación.
Leer el código genético de la carga
En lugar de probar las VE directamente en animales o personas, los investigadores reanalizaron conjuntos de datos de secuenciación existentes que catalogan qué microARN están presentes en las VE de miotubos esqueléticos de ratón (fibras musculares cultivadas en laboratorio) y de células madre mesenquimales derivadas de médula ósea. Las VE musculares mostraron unos pocos microARN dominantes, como miR-206-3p y miR-378a-3p, que constituyeron más del 60 por ciento de su carga, mientras que las VE de células madre portaban una mezcla más equilibrada, incluido el amplio grupo let-7. Dado que cada microARN puede influir en muchos genes diana, y numerosos microARN pueden converger en la misma vía, el equipo desarrolló métodos computacionales para entender cómo perfiles completos —no moléculas aisladas— podrían remodelar programas celulares.
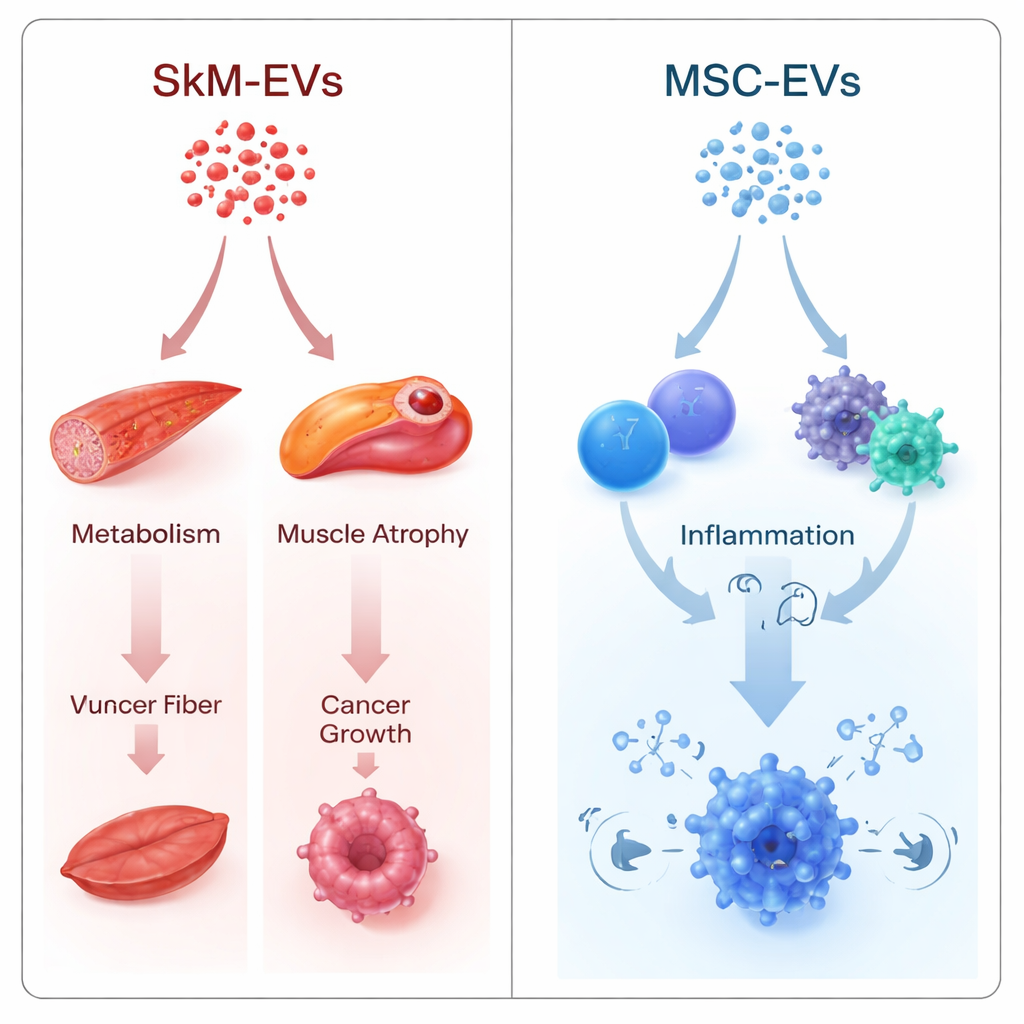
Vías relacionadas con músculo, metabolismo y cáncer
Los autores usaron dos estrategias complementarias. Una comparó directamente las VE musculares y las de células madre, preguntando en qué microARN diferían. La otra trató cada tipo de VE por separado, convirtiendo su perfil de microARN en una “puntuación de impacto” a nivel génico que estima la fuerza con la que la carga podría atenuar determinadas vías. A pesar de las diferencias matemáticas, ambos enfoques apuntaron en la misma dirección. Las VE derivadas del músculo mostraron una tendencia predicha a suprimir vías vinculadas a la pérdida muscular (señalización FoxO y TGF-β), al control de la glucemia y el equilibrio energético (FoxO, mTOR, AMPK) y a rutas de crecimiento tumoral (señalización ErbB y un grupo etiquetado como “microARN en el cáncer”). Muchos de los dianas más influyentes eran reguladores centrales de la gluconeogénesis hepática, impulsores clave de la atrofia muscular y genes nucleares promotores del cáncer.
Vesículas de células madre y el sistema inmunitario
Las VE de células madre contaron otra historia. Su carga de microARN se predijo que actúa con más fuerza sobre rutas relacionadas con el sistema inmunitario: señalización NF-κB, interacciones citocina–receptor, señalización de receptores B y T, y diferenciación de células Th17. Estas vías son centrales para cómo el organismo percibe infecciones, enciende y apaga la inflamación, y define la identidad de las células inmunitarias. Este sesgo concuerda con evidencia experimental creciente de que las VE de células madre pueden modular de forma amplia las respuestas inmunes y se están probando en condiciones donde calmar la inflamación es crucial, como enfermedades autoinmunes e inflamatorias.
De las predicciones informáticas a tratamientos futuros
En conjunto, el trabajo sugiere que las VE derivadas del músculo pueden estar naturalmente adecuadas para afecciones que implican pérdida muscular, metabolismo alterado o crecimiento celular descontrolado, mientras que las VE de células madre pueden encajar mejor en enfermedades impulsadas por respuestas inmunitarias desreguladas. Los resultados se obtienen íntegramente a partir de análisis computacionales de datos existentes y aún no demuestran beneficio en pacientes, ni contemplan otras cargas de las VE como proteínas o lípidos. Aun así, al convertir perfiles complejos de microARN en “huellas” a nivel de vías, este estudio ofrece una hoja de ruta para emparejar fuentes de VE con tipos de enfermedad y ayuda a priorizar qué combinaciones son más prometedoras para probar en el laboratorio y, eventualmente, en la clínica.
Cita: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
Palabras clave: vesículas extracelulares, músculo esquelético, microARN, células madre mesenquimales, vías de señalización celular