Clear Sky Science · es
Ingeniería de criogeles funcionalizados con polietilenimina y metales para una unión, actividad y durabilidad a largo plazo superiores de la catalasa
Por qué importa mantener las enzimas en su sitio
El peróxido de hidrógeno es un subproducto químico común en procesos que van desde el procesamiento de alimentos hasta tratamientos médicos, y las células vivas dependen de la enzima catalasa para descomponerlo en agua y oxígeno inofensivos. En la industria, sin embargo, la catalasa suele usarse en forma libre y disuelta, lo que hace que pierda rápidamente su eficacia, no se recupere fácilmente y deba reemplazarse con frecuencia. Este estudio explora una forma de “aparcar” la catalasa dentro de un material poroso tipo esponja para que se mantenga activa por más tiempo, pueda reutilizarse muchas veces y funcione de manera más eficiente, lo que podría reducir costos y hacer los procesos enzimáticos más limpios y sostenibles.

Construyendo una esponja inteligente
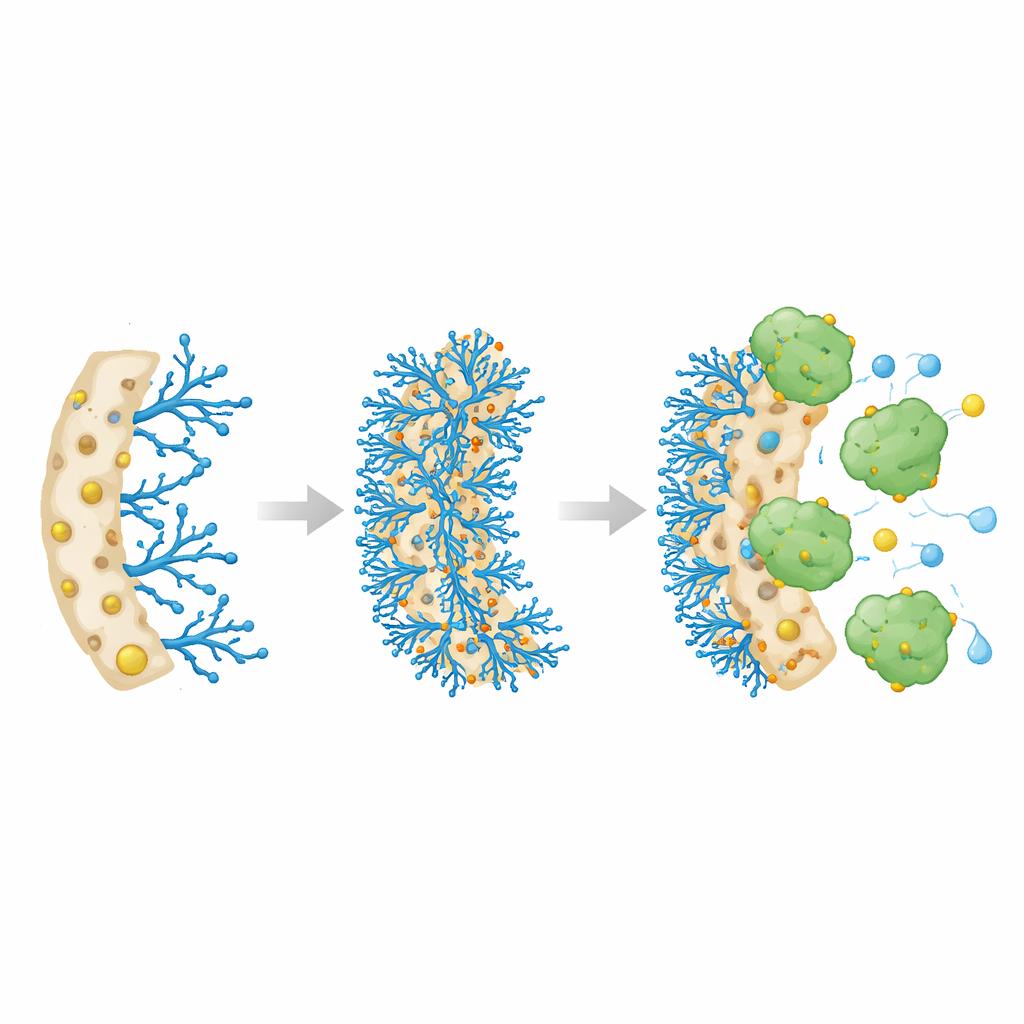
Los investigadores diseñaron una esponja polimérica especial, denominada criogel, formada por el proceso de congelación y descongelación de una mezcla líquida de modo que los cristales de hielo crean poros grandes e interconectados. Estos poros permiten que los líquidos fluyan libremente, como el agua a través de una lufa, mientras que la estructura sólida permanece resistente y elástica. El equipo usó un material base llamado Poly(HEMA-co-GMA) y, a continuación, injertó químicamente una molécula ramificada rica en grupos nitrogenados, polietilenimina (PEI). Finalmente, fijaron iones metálicos—cobre, níquel o cobalto—a esos sitios nitrogenados. La idea era que los iones metálicos actuaran como puntos de anclaje que atraen y mantienen fuertemente a las moléculas de catalasa sin bloquear el flujo de líquido a través de la esponja.
Ajustando el material para un mejor rendimiento
Para comprender cómo cada paso del diseño alteraba el material, el equipo usó varias técnicas de laboratorio para sondear su estructura, química y estabilidad. Demostraron que la adición de PEI y luego de metales no colapsó la red porosa, sino que en realidad aumentó la capacidad de la esponja para retener agua, lo cual es beneficioso para mantener las enzimas en condiciones favorables. Entre los tres metales, el cobre produjo el entorno más hidratado y mejor organizado. Imágenes de microscopía revelaron que el material original se parecía a gránulos compactos, mientras que las versiones tratadas con PEI y metales se abrieron en una red más limpia y continua de poros grandes. Mediciones del contenido metálico confirmaron que el cobre se unía con mayor fuerza y en cantidades superiores a las del níquel o el cobalto, lo que sugiere que proporcionaría los puntos de anclaje más efectivos para la catalasa.
Bloqueando la catalasa en su lugar
Cuando se introdujo la catalasa en las distintas esponjas portadoras de metales, las tres captaron la enzima rápidamente, pero la versión con cobre destacó. Cargó la mayor cantidad de catalasa—aproximadamente 392 miligramos por gramo de esponja seca—y alcanzó un nivel estable en unas ocho horas. Los investigadores examinaron entonces cómo funcionaba la enzima inmovilizada en comparación con la catalasa libre en solución. Aunque la velocidad máxima de reacción por gramo de enzima disminuyó algo, la catalasa inmovilizada mostró una atracción aparente mucho más fuerte por su sustrato, el peróxido de hidrógeno. En términos prácticos, esto significa que la enzima ligada realizó su función de manera más eficiente a niveles de sustrato más bajos, probablemente porque la esponja de cobre porosa y llena de agua concentró el sustrato cerca de la enzima y ayudó a mantener su conformación activa.
Una enzima que perdura
Una de las mayores ventajas de inmovilizar enzimas es la promesa de reutilización y larga vida útil. Aquí, la catalasa unida al criogel a base de cobre demostró ser mucho más duradera que su contraparte libre. Tras 15 ciclos de uso repetidos, la enzima inmovilizada aún conservaba alrededor de un tercio de su actividad inicial, mientras que la catalasa libre típicamente se descartaría tras un solo uso. En pruebas de almacenamiento a temperatura de refrigerador durante 70 días, la catalasa inmovilizada mantuvo más del 60% de su actividad, aproximadamente el doble que la enzima libre. La esponja también permitió que la enzima se desprendiera y recargara varias veces usando una simple solución salina, demostrando que el propio material puede reutilizarse sin una pérdida importante de capacidad.
Qué significa esto para el uso en el mundo real
Para un público no especialista, la conclusión principal es que los investigadores han construido una especie de “esponja enzimática” reutilizable que retiene la catalasa de forma firme pero delicada, ayudando a que funcione mejor con menores concentraciones químicas y dure mucho más tanto en uso como en almacenamiento. Al combinar un criogel altamente poroso con PEI e iones de cobre, crearon una plataforma que reúne alta carga de enzima, mayor eficiencia y sólida estabilidad a largo plazo. Tales materiales podrían integrarse en sistemas industriales o ambientales para descomponer el peróxido de hidrógeno y sustancias relacionadas de manera más fiable y con menos residuos, ofreciendo un paso práctico hacia tecnologías enzimáticas más verdes.
Cita: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Palabras clave: inmovilización de enzimas, catalasa, criogel, polímeros funcionalizados con cobre, biocatálisis