Clear Sky Science · es
La sobrecarga crónica de NH4Cl mejora la tolerancia a la glucosa sin modificar la sensibilidad a la insulina en ratones
Por qué el equilibrio ácido–base importa para el azúcar en sangre
Las personas con enfermedad renal crónica suelen desarrollar una condición llamada acidosis metabólica, en la que la sangre se vuelve ligeramente más ácida de lo normal. Los médicos suelen considerar esto perjudicial, en parte porque episodios breves de acidosis empeoran el control glucémico. Este estudio invierte esa idea: en ratones, una acidosis leve y prolongada mejoró en realidad la manera en que el organismo manejaba el azúcar, sin mejorar ni empeorar la acción de la hormona insulina. Comprender este giro sorprendente podría, a la larga, ayudar a afinar tratamientos tanto para la enfermedad renal como para la diabetes tipo 2.
Un desafío ácido a largo plazo en ratones
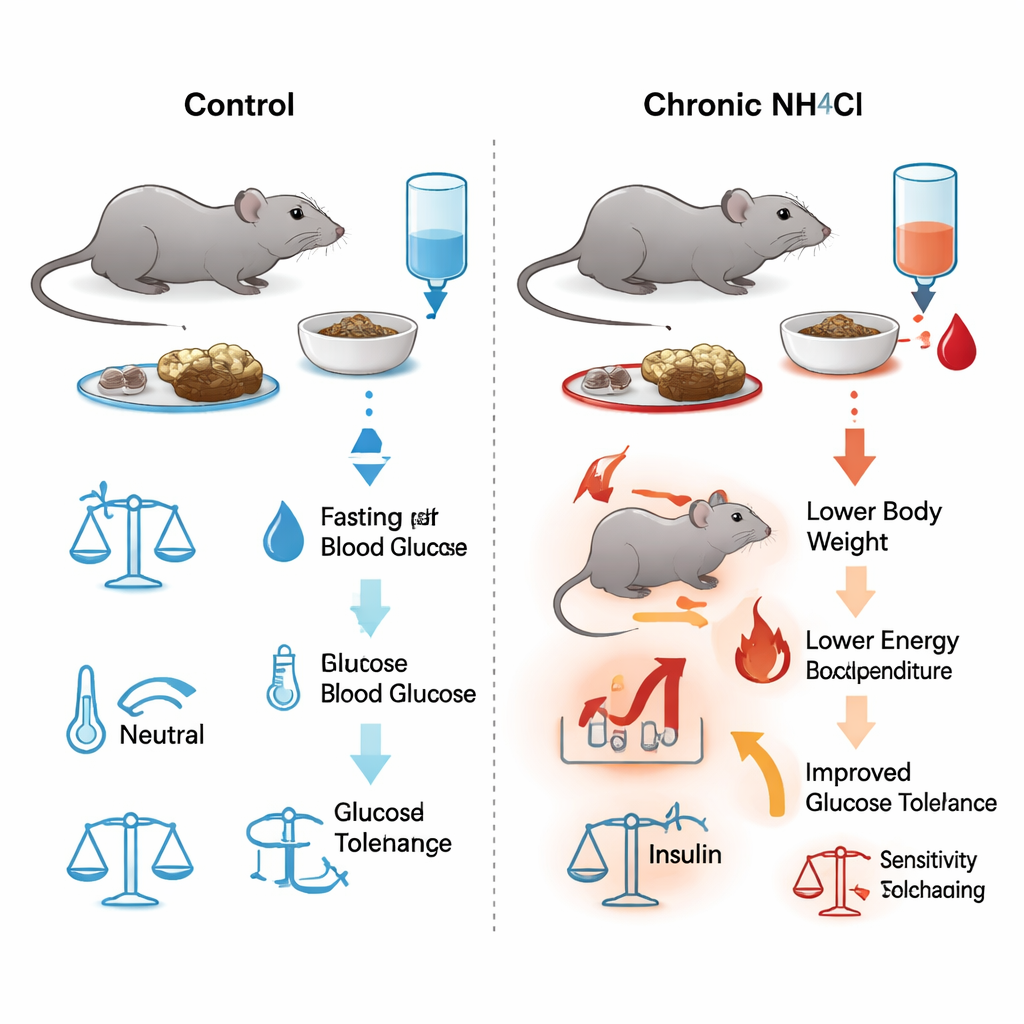
Los investigadores administraron a ratones machos agua para beber con cloruro de amonio, una sal que acidifica suavemente la sangre, durante hasta seis meses. Este tratamiento imita la carga ácida crónica observada en la enfermedad renal. Los análisis de sangre confirmaron una acidosis metabólica persistente y leve: pH y bicarbonato más bajos, cloruro más alto y, por lo demás, medidas relacionadas con el riñón estables, como la urea y el hematocrito. A pesar de comer y beber tanto o más que los ratones no tratados, los animales con carga ácida dejaron de ganar peso tras aproximadamente dos meses. Mediciones detalladas en jaulas metabólicas mostraron que estos ratones estaban quemando más energía en general, tenían menos masa magra (rica en músculo) y relativamente más grasa, lo que sugiere un mayor coste metabólico de vivir bajo acidosis crónica.
Mejor control glucémico sin ayuda extra de la insulina
El equipo evaluó de forma repetida la capacidad de los ratones para eliminar azúcar de la sangre inyectando glucosa y siguiendo los niveles sanguíneos a lo largo del tiempo. Ya una semana después de comenzar la bebida acidificante, los ratones tratados redujeron su glucosa en sangre más rápido que los controles, y esta ventaja persistió en muchos puntos temporales hasta los 180 días. La glucemia en ayunas fue consistentemente más baja en el grupo acidosis. Sin embargo, cuando los científicos midieron la insulina en sangre durante estas pruebas, los niveles eran iguales en ambos grupos. Pruebas separadas en las que se administró insulina directamente mostraron que la sensibilidad global a la insulina tampoco cambió. En otras palabras, la acidosis crónica mejoró la tolerancia a la glucosa sin exigir al páncreas producir más insulina ni a los tejidos responder más intensamente a ella.
Desplazamientos en dónde y cómo se produce y se pierde el azúcar
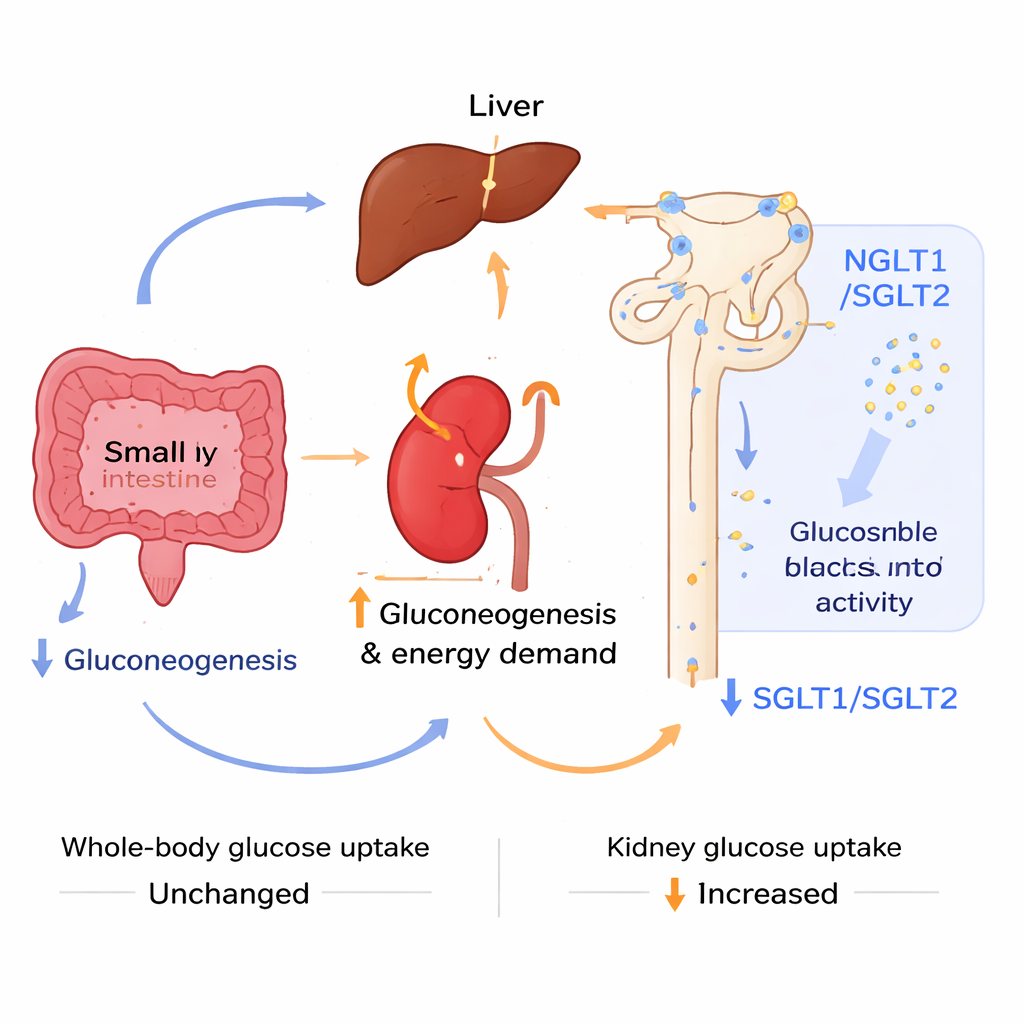
Para averiguar de dónde procedía el mejor control de la glucosa, los investigadores examinaron cómo distintos órganos producían glucosa. Usaron sustancias específicas —piruvato, alanina y glutamina— que alimentan las vías de formación de azúcar en hígado, riñón e intestino. Con el tiempo, el hígado y partes del intestino de los ratones acidosis mostraron menor actividad en la producción de nueva glucosa, especialmente a partir de alanina y glutamina. Por el contrario, el riñón mostró signos de trabajar más: genes clave implicados en la producción de glucosa y el suministro de energía estaban aumentados, y la imagen con un análogo radiactivo de la glucosa reveló una mayor captación de azúcar en riñones y vejiga, aunque la captación total corporal no cambió. Al mismo tiempo, se perdió más glucosa en la orina tras una carga de azúcar, porque los principales transportadores sodio–glucosa del riñón, que normalmente recuperan el azúcar filtrado, estaban disminuidos tanto a nivel de ARNm como de proteína. Esta combinación —menos glucosa producida por hígado e intestino, más glucosa consumida y excretada por el riñón— ayudó a mantener los niveles sanguíneos bajo control.
Cambios profundos dentro de las células renales
Instantáneas de la actividad génica en los riñones durante los primeros dos meses de tratamiento mostraron una amplia remodelación de la maquinaria celular. Se potenciaron vías implicadas en el movimiento de partículas cargadas (aniones), la recuperación de bicarbonato y el funcionamiento mitocondrial y la fosforilación oxidativa —los principales generadores de energía de la célula. Los genes vinculados al metabolismo de la glucosa y de los lípidos también se desplazaron al alza, mientras que algunas vías inmunes y de desintoxicación, incluidas partes del sistema del complemento y la familia de citocromo P450, se vieron atenuadas. Estos patrones encajan con un riñón que trabaja más para excretar ácido, consume más combustible y, al mismo tiempo, reprograma cómo maneja azúcares y lípidos para satisfacer la demanda energética adicional.
Qué significa esto para personas con problemas renales y de azúcar
En resumen, la acidosis metabólica leve y prolongada en ratones no perjudicó el control glucémico; de hecho, lo mejoró reduciendo la producción de glucosa en hígado e intestino, disminuyendo la reabsorción de glucosa en el riñón e incrementando el consumo energético renal. La insulina en sí no desempeñó un papel mayor de lo habitual. Esto no implica que la acidosis sea buena ni que los pacientes deban permanecer en acidosis; la acidosis sigue teniendo muchos efectos dañinos. Pero los hallazgos revelan que el organismo puede adaptarse de formas inesperadas y destacan al riñón como un regulador potente de la glucemia. Investigaciones futuras podrían aprovechar algunos de estos mecanismos renales —como el aumento de la pérdida urinaria de glucosa y la alteración de la producción de glucosa— sin exponer a los pacientes a los riesgos de la acidosis crónica.
Cita: Zaibi, N., Montaigne, J., Baraka-Vidot, J. et al. Chronic NH4Cl loading improves glucose tolerance without modifying insulin sensitivity in mice. Sci Rep 16, 7048 (2026). https://doi.org/10.1038/s41598-026-38007-7
Palabras clave: acidosis metabólica, tolerancia a la glucosa, función renal, gluconeogénesis, riesgo de diabetes tipo 2