Clear Sky Science · es
Identificación computacional y caracterización mecanística de productos naturales que se unen al túnel de unión prenilo de PDE6D
Volver la palanca favorita del cáncer en su contra
Muchos de los cánceres más letales —desde páncreas hasta colorrectal y de pulmón— dependen de un único “interruptor” molecular que activa la señal, llamado RAS. Cuando este interruptor se queda atascado en ON, las células crecen sin control. Durante décadas, los desarrolladores de fármacos han tenido dificultades para apagar RAS directamente. Este estudio explora una táctica diferente: buscar compuestos naturales que puedan bloquear discretamente la proteína ayudante que RAS necesita para llegar a su lugar de acción, atenuando potencialmente su señal sin tener que atacar RAS de frente. 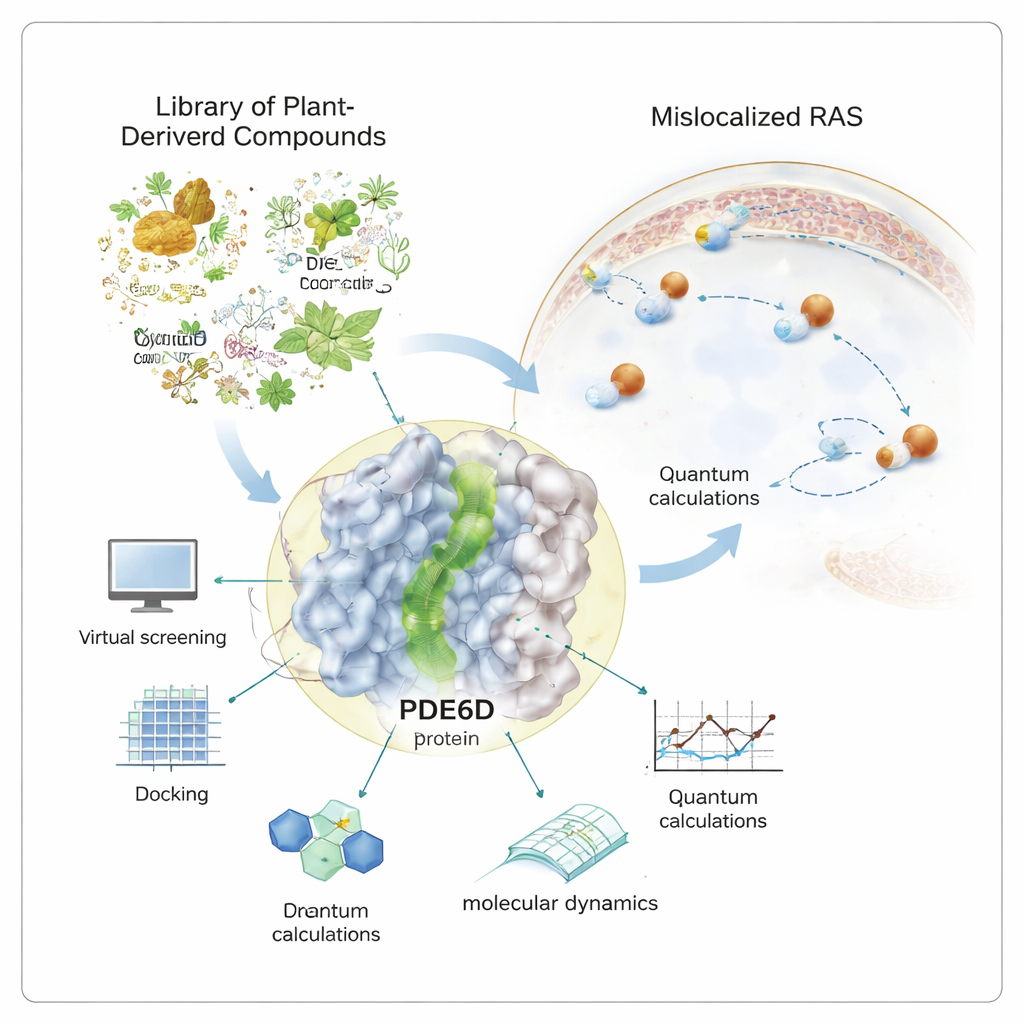
Un ayudante oculto en las células cancerosas
Las proteínas RAS deben situarse en la superficie interna de la membrana celular para enviar señales de crecimiento. Para llegar allí, llevan una cola grasosa que les permite anclarse en la membrana. Una proteína chaperona llamada PDE6D actúa como un taxi, protegiendo esa cola mientras RAS viaja por el interior acuoso de la célula. PDE6D tiene un túnel estrecho, revestido de aceite, que agarra la cola de RAS. Si ese túnel queda tapado, RAS tiene más probabilidad de acabar en el lugar equivocado, debilitando su capacidad para impulsar el cáncer. Dado que muchos fármacos existentes contra RAS solo funcionan para un subconjunto reducido de mutaciones, los investigadores están interesados en explorar PDE6D como un blanco indirecto pero potencialmente más amplio.
Usar ordenadores para registrar la biblioteca química de la naturaleza
En lugar de depender únicamente de compuestos sintéticos, el autor recurrió a una biblioteca curada de más de mil productos naturales comerciales —moléculas derivadas originalmente de plantas, microbios y otras fuentes vivas. Se emplearon potentes herramientas informáticas para cribar esta biblioteca frente a la estructura 3D de PDE6D. En esta prueba virtual, cada molécula se “ancló” (docked) en el túnel para ver qué tan ajustada y favorable podría ser su unión. Los candidatos con mejores puntuaciones se examinaron luego con cálculos a nivel cuántico, que analizan cómo se distribuyen los electrones en cada molécula y cuán fácilmente pueden participar en interacciones estabilizadoras dentro del bolsillo proteico.
Poner a prueba el estrés de los candidatos prometedores en movimiento
Las proteínas y las pequeñas moléculas no están quietas dentro de las células, por lo que el estudio fue más allá de instantáneas estáticas. Usando largas simulaciones de dinámica molecular que siguen los movimientos atómicos durante medio microsegundo, el investigador observó cómo se comportaba cada compuesto natural prometedor dentro del túnel de PDE6D a lo largo del tiempo. Dos candidatos, etiquetados MolPort-039-052-621 y MolPort-002-507-186, permanecieron alojados en el túnel con redes de contacto estables, mientras que una tercera molécula derivó hacia la salida del túnel y quedó más débilmente unida. Análisis adicionales cartografiaron qué partes de la estructura de PDE6D se flexionaban o se calmaban tras la unión, y cómo el complejo exploraba su “paisaje energético”: esencialmente, qué conformaciones eran más cómodas y duraderas. 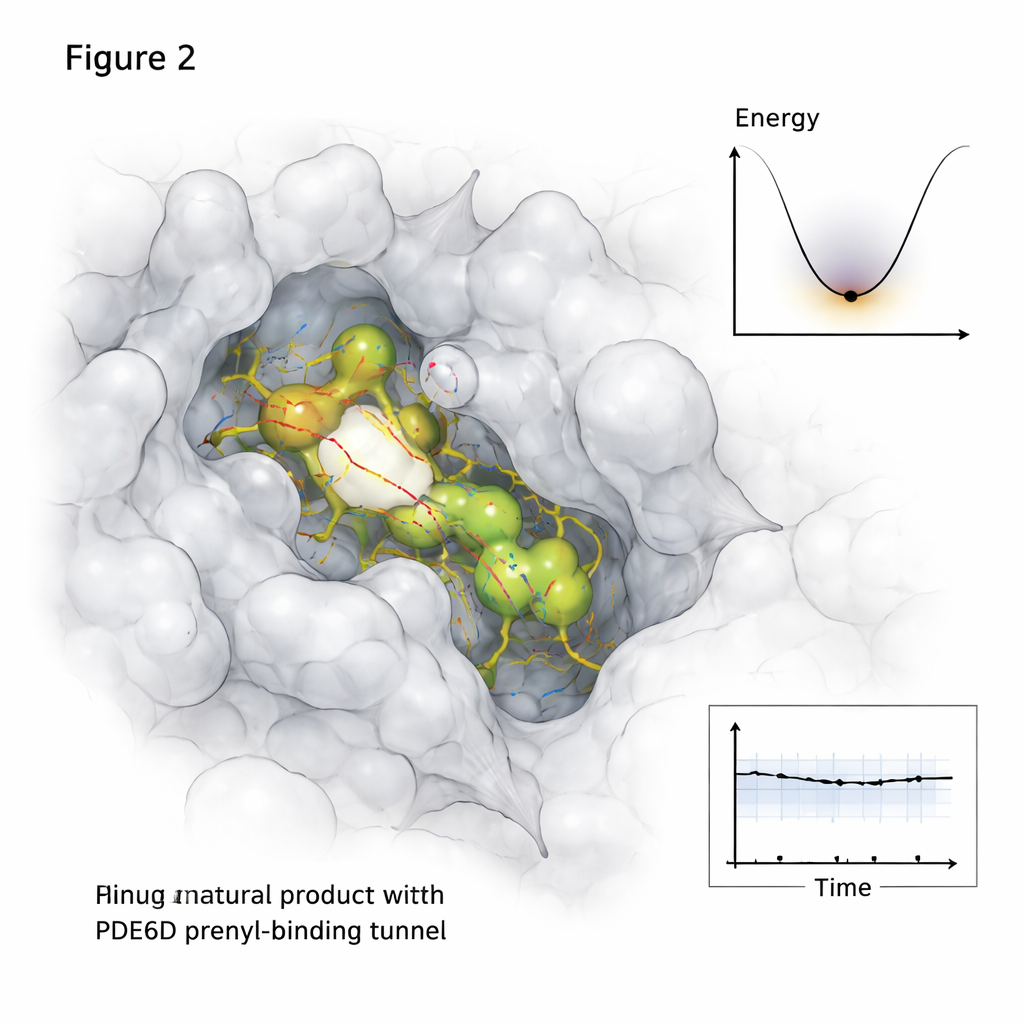
Equilibrar la fuerza de unión y el comportamiento con características de fármaco
El estudio también utilizó herramientas de predicción en línea para evaluar si estos compuestos naturales parecen puntos de partida realistas para medicamentos. Los tres principales tenían rasgos químicos consistentes con una “apariencia” básica de fármaco, pero cada uno presentaba banderas rojas. Se predijo que algunos tendrían mala absorción o solubilidad; otros mostraron indicios de posible toxicidad, como efectos sobre el ritmo cardíaco o el ADN. Estos problemas significan que las moléculas, tal como están, probablemente no sean fármacos listos para usar. En cambio, deben considerarse plantillas estructurales que los químicos podrían modificar, manteniendo las características que encajan en el túnel y recortando las partes problemáticas.
Qué significa esto para futuros tratamientos contra el cáncer
En términos sencillos, este trabajo no entrega un nuevo fármaco contra el cáncer, pero traza una ruta prometedora. Al combinar varias capas de computación —desde un anclaje rápido hasta simulaciones detalladas y cálculos cuánticos— el estudio reduce un conjunto vasto de moléculas naturales a un pequeño grupo que parecen bien adaptadas para taponar el túnel de PDE6D. Si experimentos de laboratorio futuros confirman que estos compuestos realmente desvían a RAS dentro de las células y ralentizan el crecimiento de tumores impulsados por RAS, podrían inspirar una nueva clase de tratamientos que apunten a la “logística” del cáncer en lugar de atacar directamente a su conductor principal.
Cita: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
Palabras clave: Señalización RAS, Inhibidores de PDE6D, Productos naturales, Descubrimiento de fármacos computacional, Terapia contra el cáncer