Clear Sky Science · es
La expresión de superficie de CD63 y HLA-DR en eosinófilos circulantes se correlaciona con un mejor control clínico tras la optimización del tratamiento en el asma
Por qué importan unas células sanguíneas diminutas en el asma
Para muchas personas con asma grave, los inhaladores potentes y otros fármacos siguen sin evitar la falta de aire y el riesgo de ataques. Los médicos suelen vigilar la enfermedad con recuentos sanguíneos simples, pruebas del gas espirado y medidas de alergia, pero estos no siempre reflejan cómo se siente el paciente. Este estudio pregunta si observar con más detalle una célula blanca concreta en la sangre —el eosinófilo— puede dar a los médicos una mejor ventana sobre hasta qué punto el tratamiento del asma está funcionando realmente.
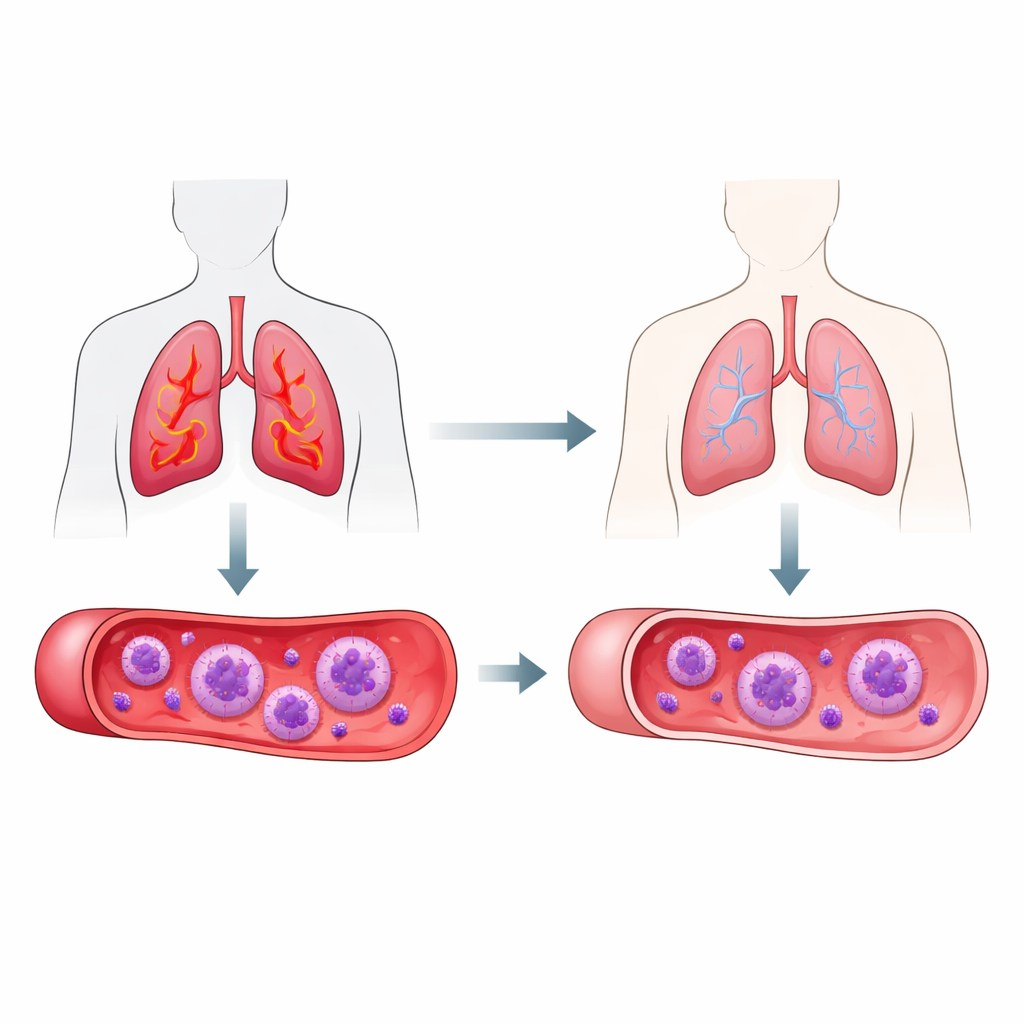
Más allá de las revisiones habituales del asma
El asma está impulsada por inflamación crónica en las vías respiratorias, y los eosinófilos están entre las células principales implicadas, sobre todo en una forma común denominada asma tipo 2 elevada. Las pruebas estándar cuentan principalmente cuántos eosinófilos hay, pero no cuán activos están. Los investigadores se centraron en dos moléculas que pueden aparecer en la superficie de los eosinófilos, llamadas CD63 y HLA-DR. Cuando estas moléculas están presentes o aumentadas, señalan que las células están más “activadas” y comprometidas en la respuesta inmunitaria. La idea era que, incluso si el número de eosinófilos se mantiene igual, los cambios en estos marcadores de superficie podrían reflejar si el asma del paciente está pasando a un mejor control.
Cómo siguió el estudio a los pacientes durante la optimización del tratamiento
El equipo estudió a adultos con asma grave que estaban siendo evaluados para inyecciones avanzadas dirigidas a los eosinófilos. Antes de comenzar estos fármacos biológicos, los pacientes pasaron por un periodo de "run-in" de tres meses en una clínica especializada, donde su tratamiento habitual se ajustó cuidadosamente siguiendo guías internacionales. Esto implicó comprobar la técnica del inhalador y aumentar los fármacos según fuera necesario, como esteroides inhalados, broncodilatadores de larga duración, bloqueadores de leucotrienos y tiotropio. Al inicio y al final de este periodo, los investigadores midieron los síntomas con el Asthma Control Test, registraron las exacerbaciones, evaluaron la función pulmonar y tomaron muestras de sangre para analizar los eosinófilos con una técnica de alta resolución llamada citometría de flujo.
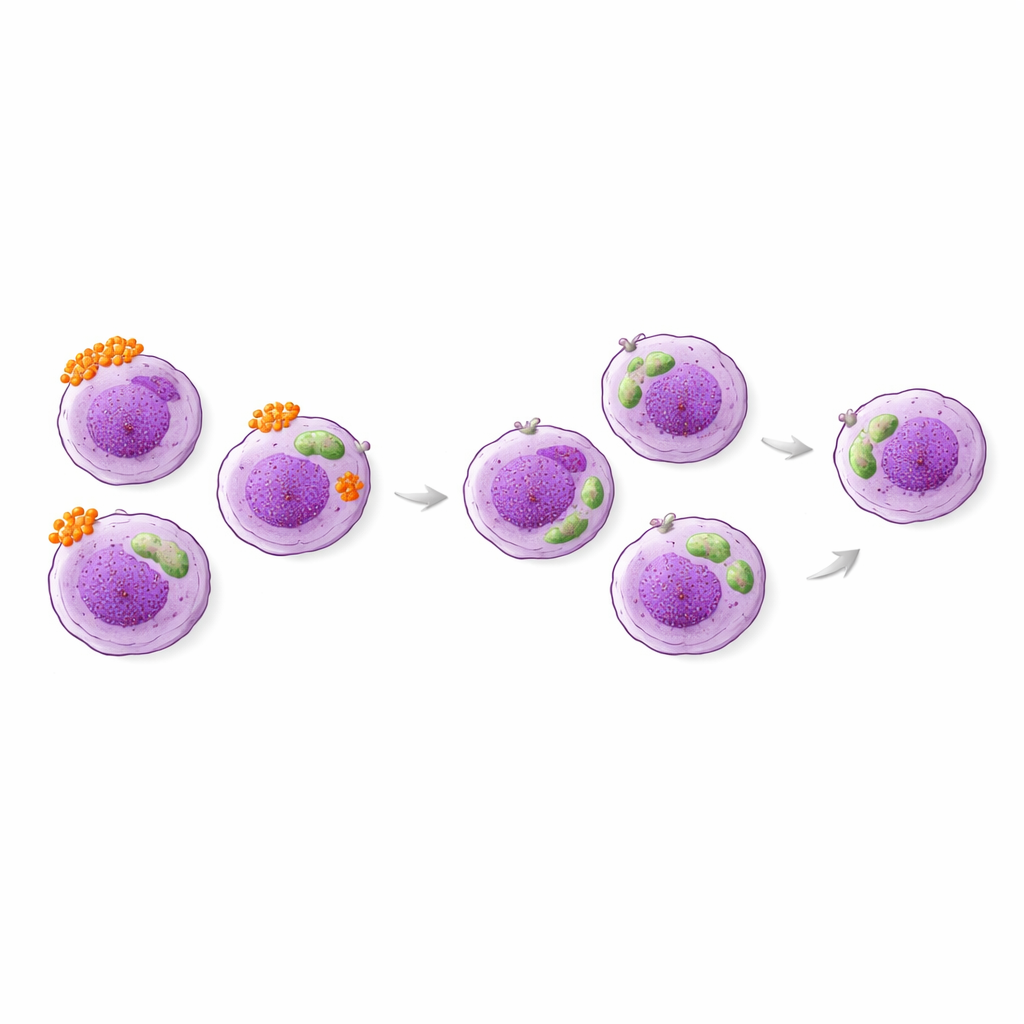
Qué cambió en la sangre y qué no
Tras tres meses de terapia optimizada, los pacientes en promedio se sintieron mejor: sus puntuaciones de control aumentaron y la proporción de personas con asma mal controlada cayó de alrededor de la mitad a aproximadamente una de cada seis. El uso de corticoides orales disminuyó y las exacerbaciones se hicieron menos frecuentes. Sorprendentemente, los recuentos simples de eosinófilos en sangre no variaron mucho, y marcadores comunes como el óxido nítrico espirado y la IgE total no se vincularon de forma sólida con los cambios en los síntomas. En contraste, una de las moléculas de superficie de los eosinófilos —HLA-DR— descendió de forma clara durante este periodo, tanto en el número de células que la expresaban como en la intensidad de su expresión. CD63, el otro marcador de activación, no cambió de media, pero tendió a mantenerse más alto en los pacientes cuyo asma siguió mal controlada.
Relacionando el comportamiento celular con cómo se sienten los pacientes
Cuando los científicos examinaron con más detalle, encontraron que los pacientes que todavía tenían niveles elevados de HLA-DR y CD63 en sus eosinófilos tras la optimización del tratamiento eran más propensos a continuar con síntomas. Los modelos estadísticos sugirieron que los cambios en HLA-DR, en particular, se correlacionaban modestamente con mejoras en las puntuaciones de síntomas, aunque el número total de eosinófilos no lo hizo. Ninguno de los marcadores se alineó de forma clara con los recuentos sanguíneos habituales, los niveles de gas espirado o las medidas de alergia, lo que implica que estas características de superficie capturan un lado diferente y más cualitativo de la enfermedad. Los autores enfatizan que estos marcadores aún no deben utilizarse para predecir quién responderá a un fármaco determinado, pero pueden servir como señales "asociativas" de que la inflamación subyacente se está calmando —o sigue activa— a pesar de la terapia estándar.
Qué podría significar esto para personas con asma de difícil control
El estudio sugiere que vigilar cómo se comportan los eosinófilos, en lugar de fijarse solo en cuántos hay, podría ayudar a personalizar la atención del asma. Una caída de HLA-DR durante el ajuste rutinario del tratamiento puede indicar que los fármacos inhalados convencionales están reduciendo con éxito la actividad inmune, incluso antes de que aparezcan grandes cambios en los síntomas. Por otro lado, eosinófilos que siguen mostrando niveles altos de HLA-DR o CD63 podrían señalar a pacientes cuya enfermedad permanece latente y que podrían beneficiarse de avanzar hacia terapias biológicas o de elegir fármacos que apunten a vías diferentes. Aunque se necesita más investigación antes de que estas pruebas formen parte de la práctica clínica cotidiana, examinar la "personalidad" de los eosinófilos añade una capa prometedora para entender y manejar el asma grave.
Cita: Scarlata, S., Mazzuca, C., Vitiello, L. et al. Surface expression of CD63 and HLA-DR in circulating eosinophils correlates with improved clinical control after treatment optimization in asthma. Sci Rep 16, 8289 (2026). https://doi.org/10.1038/s41598-026-37906-z
Palabras clave: asma grave, eosinófilos, biomarcadores, medicina personalizada, citometría de flujo