Clear Sky Science · es
Modelado de célula completa predice estrategias alternativas de asignación del proteoma en el arqueón Methanococcus maripaludis
Por qué importan estos minúsculos productores de metano
Methanococcus maripaludis es un arqueón microscópico que convierte compuestos simples como dióxido de carbono y formiato en metano, un componente principal del gas natural. Comprender cómo este microbio distribuye sus recursos internos —especialmente sus proteínas— puede revelar reglas generales de la vida en condiciones de limitación energética y orientar esfuerzos para aprovecharlo como fábrica biológica de metano o como plataforma para la química verde.
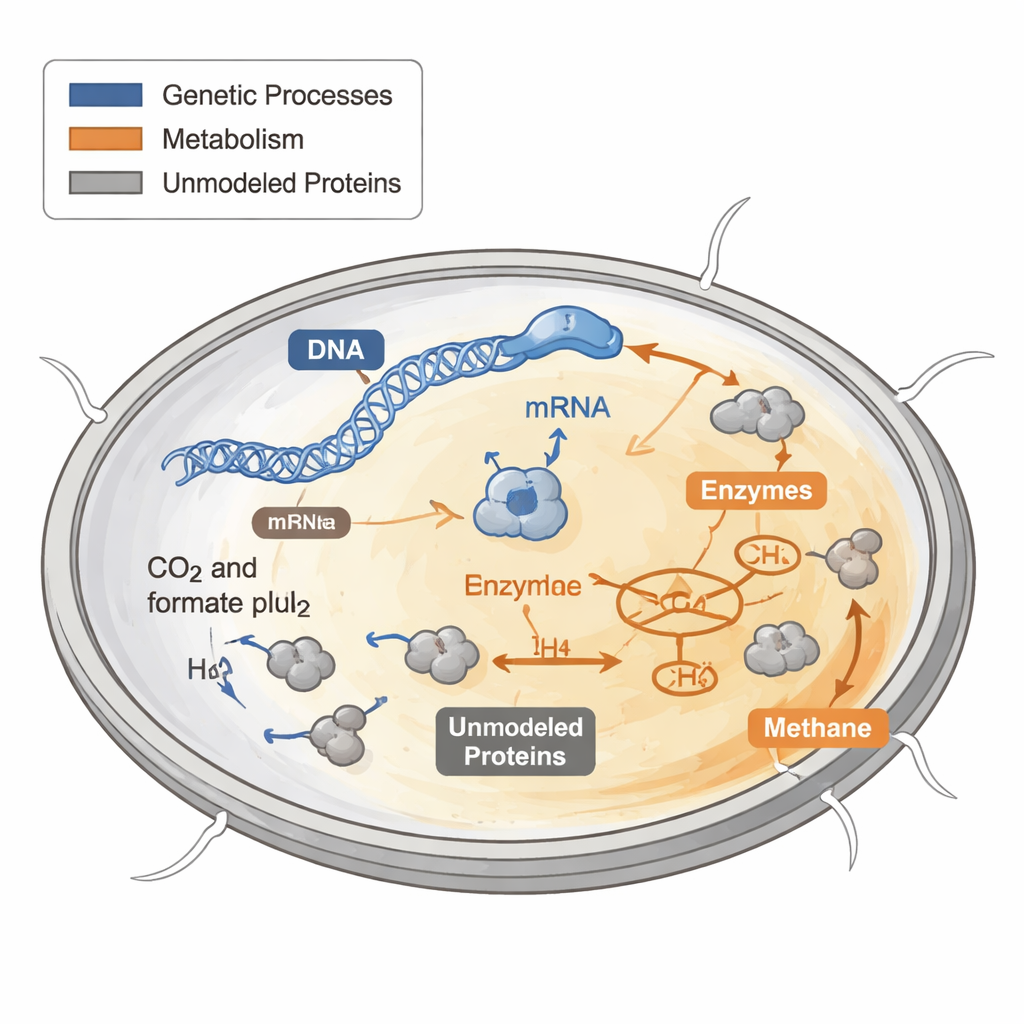
Cómo gastan las células su presupuesto proteico
Toda célula debe decidir cómo gastar su limitado “presupuesto” de proteínas. Algunas proteínas construyen partes nuevas de la célula, otras captan energía y otras realizan tareas de mantenimiento. Modelos computacionales previos del metabolismo trataron estas proteínas como si fueran gratuitas e ilimitadas, lo que funciona mal cuando se intenta predecir el crecimiento en condiciones adversas o con pocos nutrientes. En bacterias y levaduras, los experimentos han mostrado que las células de crecimiento rápido dedican una porción mayor de su presupuesto proteico a los ribosomas, las máquinas moleculares que fabrican nuevas proteínas, mientras que las células de crecimiento lento desplazan recursos a otras funciones.
Un arqueón que rompe las reglas
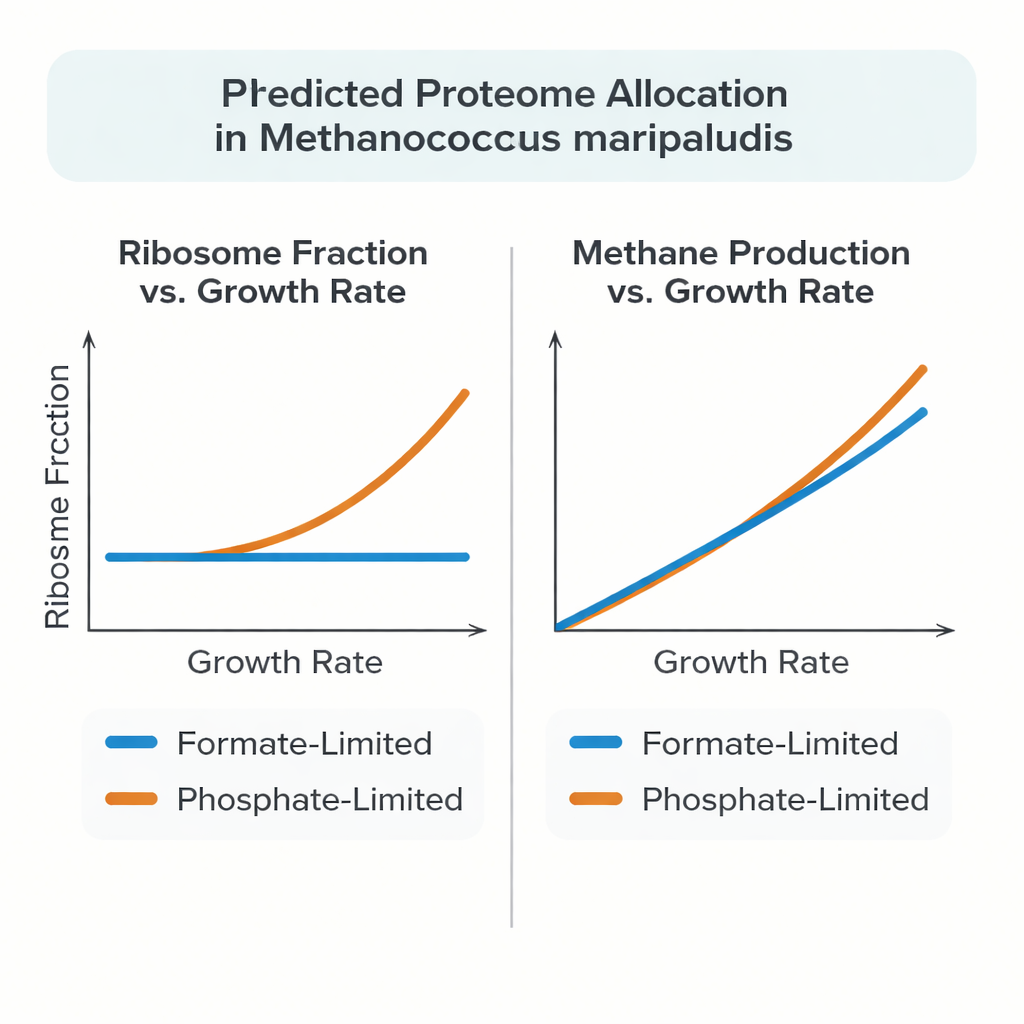
Experimentos recientes revelaron que M. maripaludis no siempre sigue ese patrón. Cuando crece usando formiato como fuente tanto de carbono como de energía, la fracción de su presupuesto proteico invertida en ribosomas se mantiene casi constante al disminuir la velocidad de crecimiento. Sin embargo, bajo limitación de fosfato, el arqueón se comporta de forma más convencional: la fracción ribosomal aumenta con la tasa de crecimiento, de manera similar a Escherichia coli y a la levadura. Para explicar este comportamiento inusual, los autores construyeron un modelo detallado de estilo de célula completa que enlaza el metabolismo con el proceso costoso de fabricar y ensamblar proteínas y ARN, en lugar de tratar las proteínas como tasas de reacción abstractas.
Construyendo un modelo de estilo célula completa
Los investigadores partieron de un mapa metabólico existente de M. maripaludis y añadieron miles de reacciones adicionales que describen la expresión génica: copiar ADN a ARN, cargar ARN de transferencia, ensamblar ribosomas y complejos enzimáticos, y diluir estos componentes durante la división celular. Reunieron límites de velocidad enzimática a partir de bases de datos bioquímicas y literatura, y estimaron qué parte de la masa proteica está formada por proteínas “no modeladas” que no están directamente vinculadas a las reacciones del mapa. Luego impusieron restricciones globales que limitan la masa total de proteína y ARN, relacionan las tasas de reacción con la cantidad de enzima disponible y atan la producción de proteínas a la capacidad ribosomal. Con estas restricciones, el modelo debe elegir cómo asignar un presupuesto proteico fijo para sostener el crecimiento.
Lo que revelaron las simulaciones
Al confrontarlo con experimentos de quimiostato de alta calidad, el modelo reprodujo con precisión las masas medidas de proteína y ARN, las tasas de producción de metano y los rendimientos de crecimiento en un rango de tasas de crecimiento lentas. Bajo limitación por formiato, la célula simulada eligió de forma natural una fracción de proteína ribosomal casi constante a medida que cambiaba el crecimiento, reflejando los datos experimentales. Bajo limitación de fosfato, el modelo coincidió con el aumento observado en la fracción ribosomal solo cuando se permitió que los ribosomas trabajaran más rápido a bajas tasas de crecimiento, consistente con mediciones que muestran más ribosomas activamente implicados en la síntesis proteica. El modelo también sugirió que una porción sustancial de la proteína en M. maripaludis no es estrictamente necesaria para el crecimiento mínimo, y que el exceso de carbono y energía puede almacenarse o desviarse hacia otras moléculas grandes como glucógeno o aminoácidos libres, según cuál nutriente sea limitante.
Explorando mutantes y límites de crecimiento
Puesto que el modelo contabiliza explícitamente el coste proteico de cada vía, puede predecir no solo si los mutantes genéticos crecen, sino qué tan bien crecen en relación con el tipo salvaje. Los autores simularon cepas carentes de distintas enzimas que procesan hidrógeno y compararon la aptitud pronosticada con mediciones de laboratorio en varias condiciones de crecimiento, incluida la presencia o ausencia de hidrógeno y monóxido de carbono. En muchos casos, el modelo captó si los mutantes podían crecer y produjo estimaciones razonables de sus tasas de crecimiento relativas, mejorando modelos anteriores que solo podían dar respuestas de sí o no. El mismo marco se utilizó para estimar las tasas máximas de crecimiento posibles en condiciones por lotes para distintas combinaciones de sustratos.
Qué significa esto para la ciencia y la tecnología
En términos sencillos, este estudio muestra que M. maripaludis emplea una estrategia alternativa para presupuestar su fuerza laboral proteica, manteniendo sus fábricas de proteínas funcionando con una participación constante del presupuesto en algunas condiciones en lugar de reducirlas a medida que el crecimiento se desacelera. Al integrar ese comportamiento en un modelo detallado y basado en datos, el trabajo ofrece un banco de pruebas para explorar cómo los microbios limitados por la energía equilibran crecimiento, mantenimiento y almacenamiento. Para la investigación aplicada, el modelo ofrece una hoja de ruta para diseñar este arqueón con el fin de producir más metano u otros productos al identificar qué enzimas y vías son las más costosas en términos de inversión proteica. Más ampliamente, extiende el potente modelado de estilo célula completa más allá de bacterias y levaduras hacia el dominio arqueal, ayudando a cerrar la brecha entre los detalles moleculares y el comportamiento a gran escala de las comunidades microbianas implicadas en el clima, la energía y la biotecnología industrial.
Cita: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Palabras clave: Methanococcus maripaludis, asignación del proteoma, modelado de célula completa, metanogénesis, metabolismo de arqueas