Clear Sky Science · es
La proteína de la nucleocápside de SARS-CoV-2 forma complejos con proteínas reguladoras solubles del complemento que pueden unirse al virión
Por qué importa este truco viral oculto
La mayoría hemos oído hablar de la proteína “spike” del coronavirus, porque es el principal objetivo de las vacunas. Pero en el interior del virus hay otra proteína, llamada nucleocápside o proteína N, que resulta ser mucho más que un simple empaquetador estructural. Este estudio muestra que la proteína N puede enganchar reguladores inmunitarios humanos clave en la sangre y transportarlos hasta la superficie del virus. Al hacerlo, SARS-CoV-2 podría apagar en parte uno de nuestros primeros sistemas de defensa —el sistema del complemento—, ayudando al virus a sobrevivir y posiblemente contribuyendo a la gravedad de la COVID-19.
Una mirada más cercana a la proteína interna del virus
La proteína N es el “envoltorio” del genoma del virus, y ayuda a empaquetar y estabilizar su ARN. Los médicos han detectado altos niveles de proteína N circulando en la sangre de pacientes con COVID-19, especialmente en los casos graves, y trabajos anteriores sugieren que puede provocar señales inflamatorias. Los autores se preguntaron si N también podría interferir con el complemento, una red de proteínas en la sangre que marca a los invasores para su destrucción y puede perforar microbios. Muchos virus han evolucionado maneras ingeniosas de apoderarse o imitar los reguladores del complemento del propio cuerpo para evitar ser atacados. El equipo planteó tres preguntas: ¿se une N a la proteína spike y al virus mismo?, ¿se une a proteínas reguladoras del complemento humanas en la sangre?, y ¿puede transportar estos reguladores hasta la superficie viral?
Cómo se encuentran N y spike en el virus
Usando varias pruebas de unión de proteínas, los investigadores demostraron que la proteína N puede adherirse directamente a la proteína spike, tanto si la spike se produce en el laboratorio como si está presentada en partículas reales de SARS-CoV-2. Confirmaron esta interacción en diferentes montajes experimentales y midieron su afinidad, encontrando una fuerza similar a la de muchos anticuerpos. Al recortar la proteína spike en fragmentos e identificar qué piezas seguían unidas a N, cartografiaron las zonas de contacto probables, principalmente en el dominio N-terminal de la spike, una región ya conocida como punto caliente para la unión de anticuerpos y para el acoplamiento de ciertas moléculas del hospedador. Esto sugiere que N puede formar un puente ajustada y biológicamente significativa con la spike en viriones reales.
Secuestrando los interruptores de seguridad del cuerpo
El sistema del complemento está estrictamente controlado por “frenos” solubles llamados proteínas reguladoras del complemento, que protegen a nuestras propias células del fuego amigo. El equipo se centró en cuatro de ellas —el inhibidor C1, la proteína fijadora de C4, el factor H y la vitronectina— porque actúan en diferentes etapas de la cascada del complemento. En ensayos con suero sanguíneo y en ensayos con proteínas purificadas, la proteína N se unió a las cuatro reguladoras, mientras que la spike no se unió a ninguna de ellas en las mismas condiciones. Esto significa que N puede formar complejos N–PRC en plasma. De forma crucial, cuando N se mezcló previamente con suero humano y luego se expuso a partículas virales, los investigadores detectaron estas proteínas reguladoras adheridas a los viriones —pero solo cuando N estaba presente. Cuanta más N usaron, más reguladores del complemento aparecieron en el virus, lo que apunta a un mecanismo de reclutamiento dependiente de la dosis. 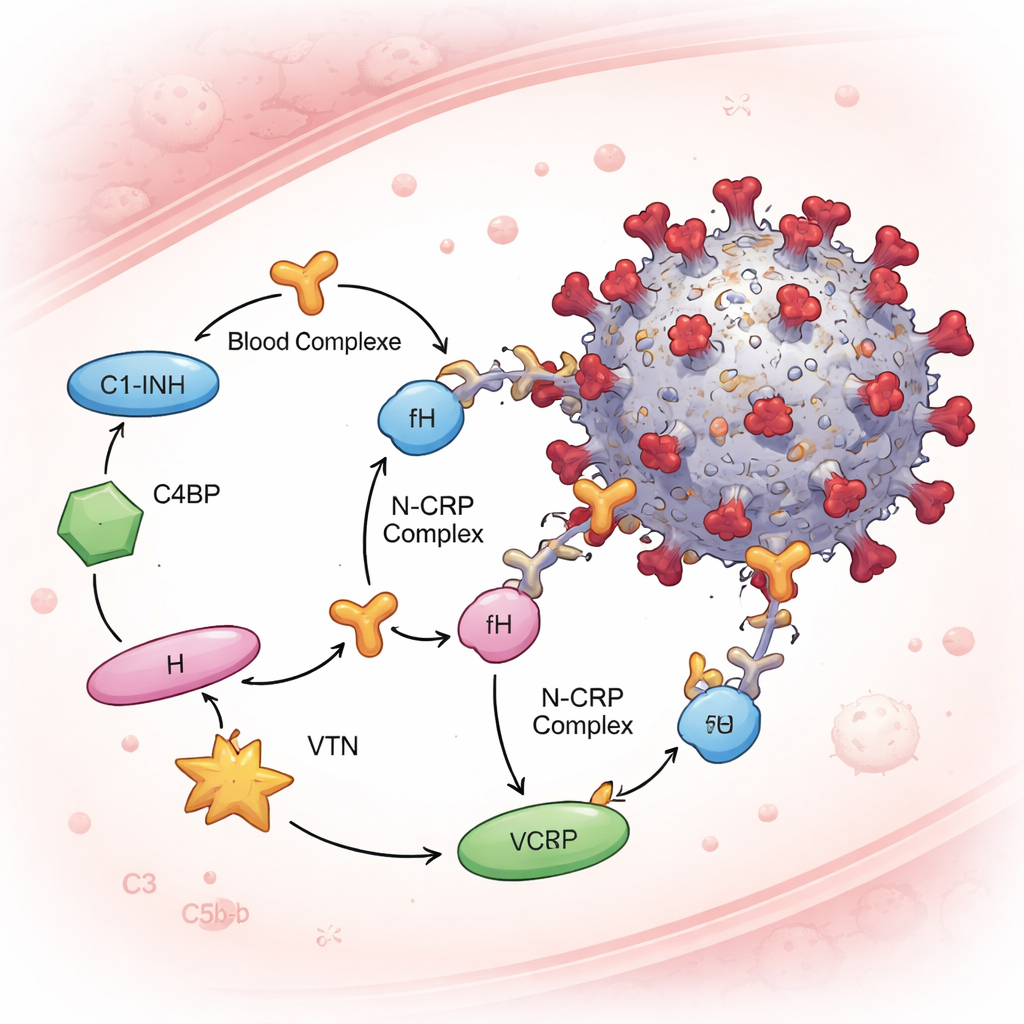
Atenuando el paso final del ataque
El arma definitiva del sistema del complemento es el complejo de ataque de membrana (MAC), una estructura en forma de anillo que forma poros en las membranas de células o envolturas virales. Los autores probaron si N podía modificar la formación del MAC sobre SARS-CoV-2. Incubaron virus purificado con suero humano, con o sin adición de proteína N, y luego midieron cuánto del complejo C5b-9 del MAC acabó en los viriones. Sin N, el virus acumuló C5b-9, lo que indica un ataque activo del complemento. Cuando N estuvo presente, la deposición del MAC disminuyó de forma dependiente de la concentración: más N significó menos C5b-9 en el virus. Esto encaja con la idea de que N, al decorar el virión con reguladores del complemento, lo protege de ser llenado de poros. 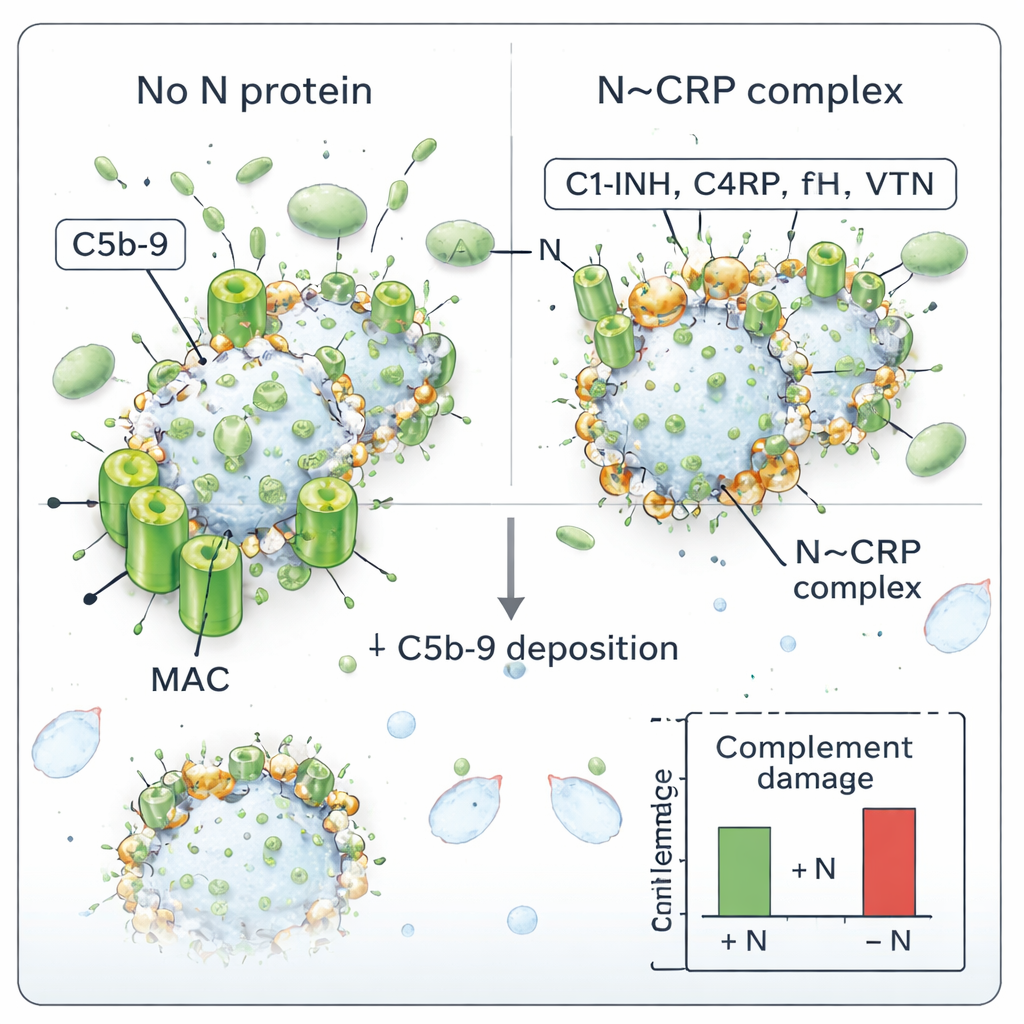
Qué significa esto para los pacientes y las terapias futuras
Para un público no especializado, la conclusión principal es que SARS-CoV-2 no depende únicamente de su famosa spike para burlar al sistema inmunitario. Su proteína interna N puede escapar al torrente sanguíneo, captar los “frenos” del complemento del propio cuerpo y llevarlos de vuelta a la superficie viral. Allí, pueden ayudar al virus a ocultarse de un brazo potente de la inmunidad innata y reducir el daño directo mediado por el complemento. Esto podría contribuir tanto a la persistencia de la infección como a las alteraciones complejas del complemento observadas en los casos graves de COVID-19. Aunque estos experimentos se realizaron en condiciones controladas de laboratorio, ponen de relieve las interacciones N–complemento como un posible nuevo objetivo: terapias que bloqueen la unión de N a estas proteínas reguladoras, o que restauren la actividad equilibrada del complemento, podrían algún día ayudar a inclinar la balanza de nuevo a favor del sistema inmunitario.
Cita: Víglaský, J., Bhide, K., Talpasova, L. et al. SARS-CoV-2 nucleocapsid protein forms complexes with soluble complement regulatory proteins that can bind to the virion. Sci Rep 16, 6599 (2026). https://doi.org/10.1038/s41598-026-37866-4
Palabras clave: nucleocápside de SARS-CoV-2, sistema del complemento, evasión inmunitaria, proteínas reguladoras del complemento, gravedad de COVID-19