Clear Sky Science · es
Estrategias computacionales para desentrañar información a partir de inhibidores conocidos para una posterior optimización de candidatos: estudio de caso en análogos de celecoxib
Por qué importan los cambios diminutos en los analgésicos
Los analgésicos modernos no solo atenúan el dolor; modifican la química del cuerpo de maneras muy precisas. El celecoxib, un antiinflamatorio popular, se dirige a una enzima implicada en el dolor y la inflamación mientras respeta en gran medida a una enzima hermana que protege el estómago. Sin embargo, docenas de parientes químicos cercanos del celecoxib se comportan de forma muy distinta en el organismo. Este estudio utiliza modelos por ordenador para plantear una pregunta aparentemente simple con grandes implicaciones para medicinas más seguras: ¿cuánto importa un solo cambio pequeño en una molécula?
La enzima que activa el dolor
Cuando un tejido resulta dañado o inflamado, el cuerpo libera una molécula lipídica llamada ácido araquidónico. Una enzima denominada COX-2 convierte esa molécula en prostaglandinas, que provocan dolor, fiebre e hinchazón. Una enzima relacionada, COX-1, contribuye a proteger la mucosa gástrica y las plaquetas. Analgésicos más antiguos como el ibuprofeno actúan sobre ambas enzimas, aliviando el dolor pero a menudo irritando el intestino. El celecoxib fue diseñado para encajar en un bolsillo ligeramente más amplio que se encuentra principalmente en COX-2, bloqueando las señales de dolor y dejando intactas gran parte de las funciones protectoras de COX-1. Comprender la forma detallada de ese bolsillo y cómo se acomodan en él las moléculas de fármaco es clave para diseñar medicamentos nuevos que sean potentes y seguros.
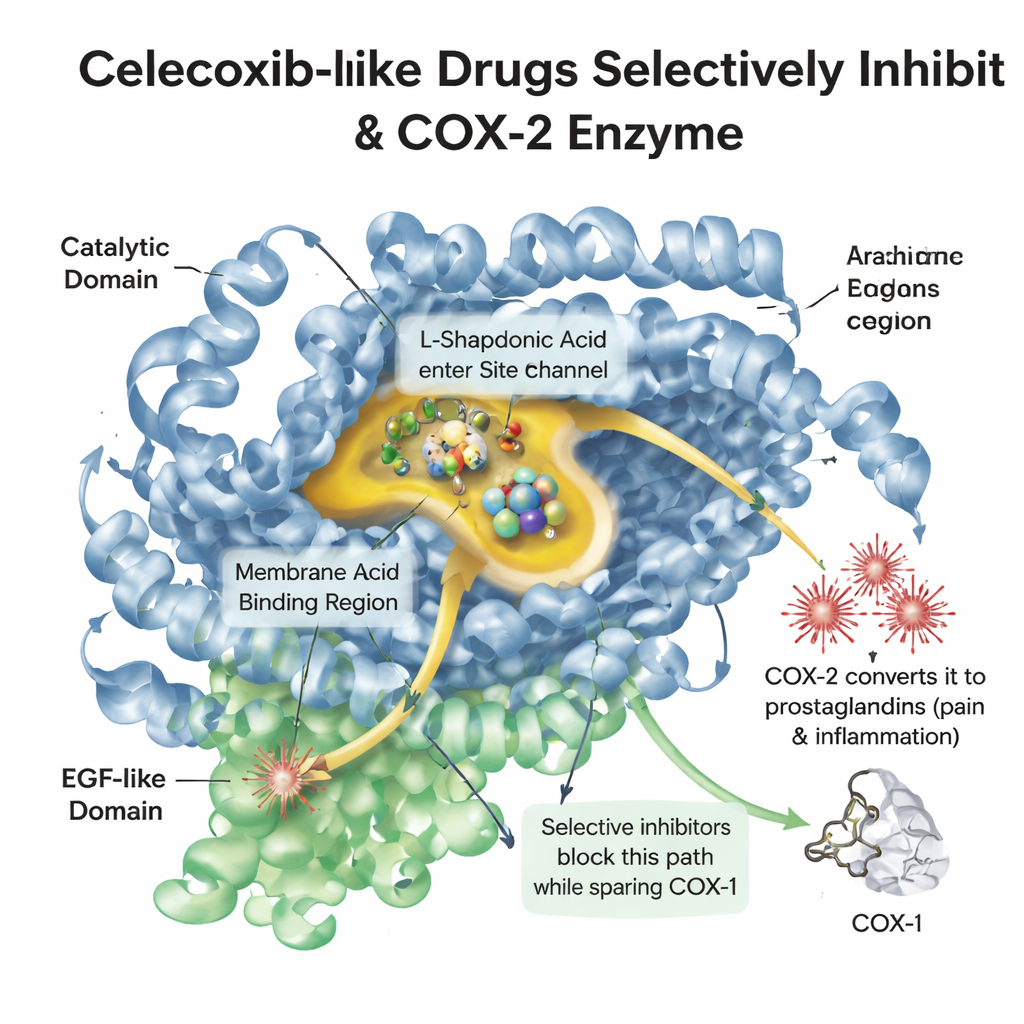
Una biblioteca digital de fármacos similares
Los investigadores reunieron un conjunto de 375 moléculas que comparten el marco básico de tres anillos del celecoxib pero difieren en pequeños detalles, como el intercambio de un solo átomo o de un grupo lateral. Obtuvieron estas estructuras y sus potencias medidas de bloqueo de COX-2 de una base de datos pública de fármacos. Con software químico generaron modelos 3D de cada molécula, calcularon casi 2.000 descriptores numéricos de sus formas y propiedades, y las acoplaron (docking) en una estructura de alta resolución de la enzima COX-2. En el docking, un ordenador posiciona una molécula en el bolsillo de la enzima de muchas formas y puntúa qué tan ajustada queda cada pose.
Qué controla realmente la potencia y la selectividad
El equipo centró la atención en tres regiones clave del celecoxib. “Sitio‑1” es un anillo que se sitúa en una zona apolar del bolsillo; “Sitio‑2” es un anillo con una cola rica en flúor; y “Sitio‑3” es un anillo que porta un grupo sulfonamida que forma enlaces de hidrógeno fuertes. Su análisis mostró que el Sitio‑1 prefiere grupos pequeños y no polares que preserven los contactos hidrofóbicos; hacer esta región más hidrofílica, por ejemplo añadiendo un –OH o un grupo ácido, suele debilitar el fármaco. En el Sitio‑2, grupos electronegativos pequeños como el flúor a menudo aumentan la potencia al mejorar las interacciones en un bolsillo estrecho, mientras que colas más voluminosas o polares tienden a perjudicar la actividad. En el Sitio‑3, el nitrógeno de la sulfonamida, capaz de donar un enlace de hidrógeno, fue crucial; sustituirlo por una versión no enlazante redujo notablemente la unión.
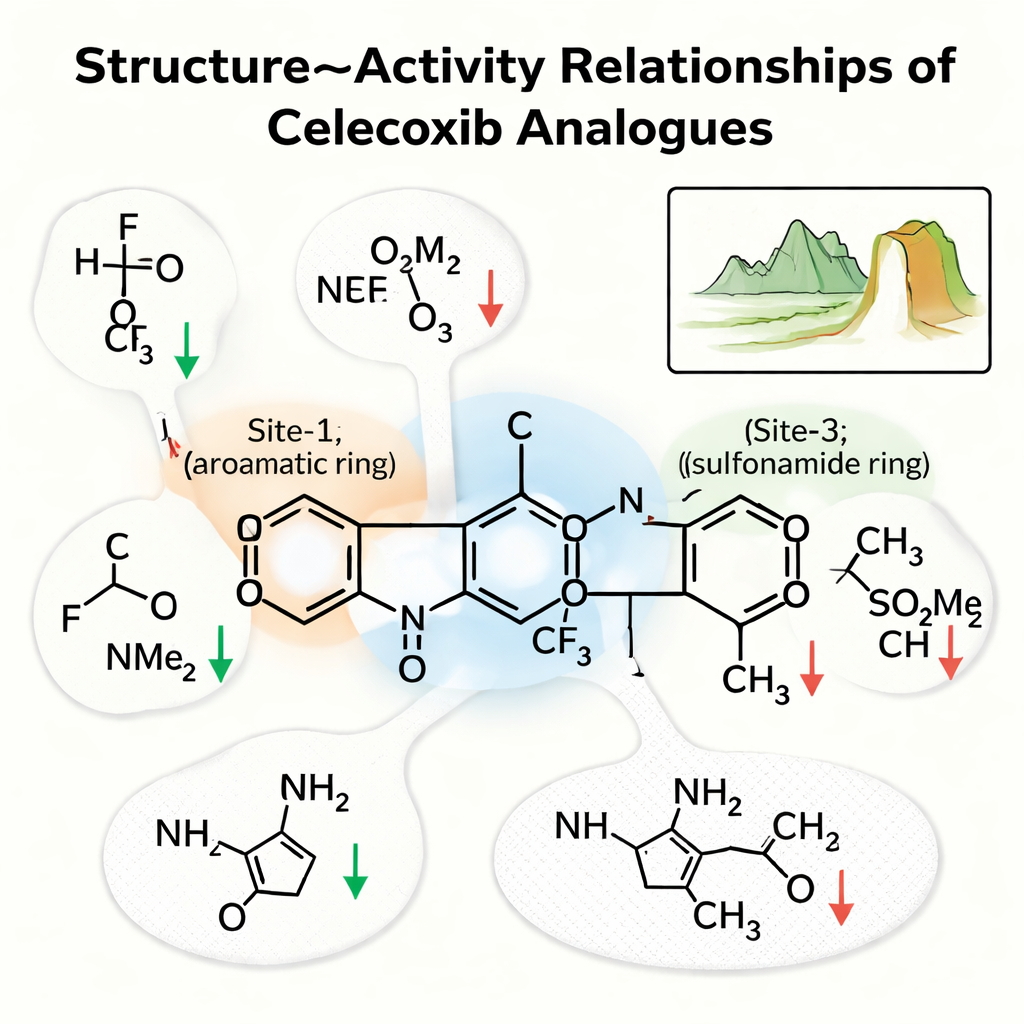
Acantilados en el paisaje químico
Para ir más allá de las tendencias simples, los autores construyeron un “paisaje estructura‑actividad”, que pregunta cuánto salta la potencia de un fármaco cuando la estructura cambia solo un poco. En esta visión, la mayoría de los compuestos similares al celecoxib se encuentran en colinas suaves: modificarlos —por ejemplo, desplazando un halógeno o añadiendo un pequeño grupo flexible— ajusta la potencia hacia arriba o hacia abajo de manera predecible. Pero algunos pares forman agudos “acantilados de actividad”, donde un cambio diminuto, como sustituir un metilo por un trifluorometilo o añadir un solo átomo de flúor, provoca una ganancia o pérdida dramática de actividad. El estudio también realizó simulaciones completas de dinámica molecular —películas virtuales de los complejos fármaco‑enzima en movimiento— que confirmaron que los mejores análogos se mantienen estables en el bolsillo durante cientos de nanosegundos.
Guiando la próxima generación de analgésicos más seguros
Para un público no especialista, la conclusión es que en el diseño de fármacos los detalles pequeños importan enormemente. Dos compuestos que parecen casi idénticos en papel pueden diferir mil veces en la intensidad con que bloquean COX-2, simplemente porque un átomo extra mejora el encaje en un bolsillo microscópico o interrumpe un contacto clave. Al mapear de forma sistemática qué cambios ayudan o perjudican en cada uno de los tres sitios clave del celecoxib, y al resaltar los peligrosos “acantilados” donde pequeños ajustes tienen efectos desproporcionados, este trabajo computacional ofrece una hoja de ruta para los químicos. Señala el camino hacia nuevos antiinflamatorios que conserven la eficacia analgésica del celecoxib mientras elevan aún más la seguridad y la selectividad.
Cita: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
Palabras clave: inhibidores de COX-2, análogos de celecoxib, fármacos antiinflamatorios, diseño de fármacos por ordenador, relaciones estructura-actividad