Clear Sky Science · es
El exosoma derivado de células epiteliales amnióticas humanas con miR-25-3p mejora la expresión de mucinas en células caliciformes conjuntivales al regular a la baja BCL2L11
Por qué importa una superficie ocular más lisa
Cualquiera que haya sufrido ojos secos y ásperos sabe cuánto influye una película lagrimal sana en una visión nítida y cómoda. Una parte clave de esta capa protectora es el moco producido por pequeñas fábricas llamadas células caliciformes, que recubren la esclerótica y la cara interna de los párpados. Cuando estas células se dañan o se pierden, como en la enfermedad del ojo seco o en procesos inflamatorios graves, la superficie ocular queda más expuesta. Este estudio explora una terapia emergente “sin células” que emplea paquetes microscópicos liberados por tejido placentario donado para ayudar a las células caliciformes a sobrevivir y a producir más del moco que mantiene nuestros ojos hidratados y protegidos.
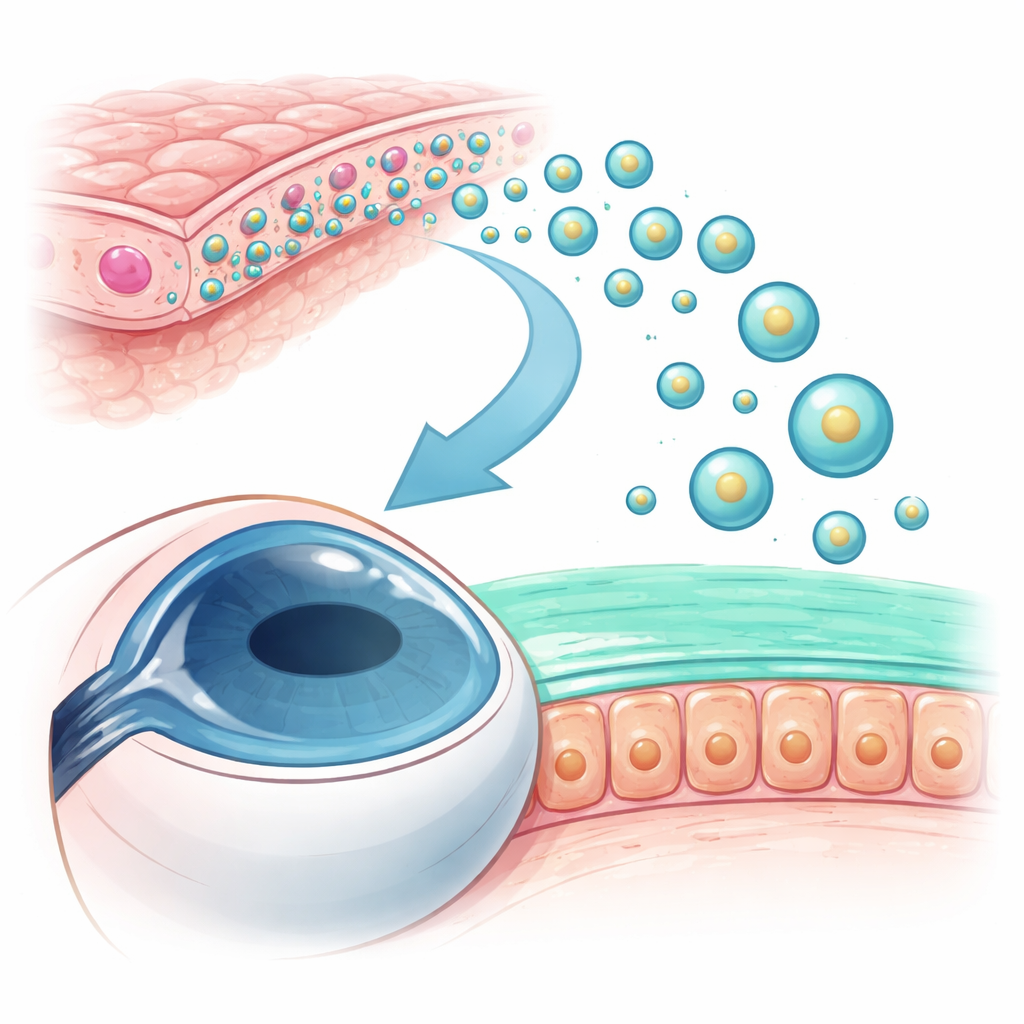
Pequeños paquetes de entrega procedentes del tejido natal
Los investigadores se centraron en las células epiteliales de la amnios humana, que provienen de la membrana delgada que rodea al feto durante el embarazo y ya son conocidas por sus propiedades reparadoras y antiinflamatorias. Estas células liberan burbujas de tamaño nanométrico, llamadas exosomas, que transportan proteínas y reguladores genéticos entre células. El equipo aisló estas vesículas de cultivos de células amnióticas, confirmó su morfología típica en forma de copa y su rango de tamaño mediante microscopía electrónica, y verificó la presencia de proteínas marcadoras conocidas de exosomas. Este paso de caracterización mostró que obtuvieron una preparación limpia de los pequeños paquetes que querían probar.
Un mensaje microscópico para las células de la superficie ocular
La siguiente pregunta fue si estos exosomas podían alcanzar e influir en las células caliciformes conjuntivales, las células productoras de moco tan importantes para la comodidad ocular. Los científicos marcaron los exosomas con un tinte fluorescente y los añadieron a células caliciformes humanas cultivadas en placas. Bajo el microscopio observaron señales brillantes dentro de las células, especialmente a dosis más altas de exosomas, lo que confirmó que las células caliciformes los incorporan con facilidad. Dentro de los exosomas encontraron una molécula de ARN pequeña en particular, miR-25-3p, protegida frente a enzimas degradativas, y mostraron que bloquear la producción de exosomas en las células fuente reducía drásticamente la liberación de esta molécula. En conjunto, estas pruebas revelaron que miR-25-3p se exporta principalmente dentro de exosomas y puede entregarse directamente a las células caliciformes.
Ayudando a que las fábricas de moco funcionen mejor y sobrevivan
Una vez establecido este conducto de entrega, los autores examinaron qué sucede con las células caliciformes tras recibir exosomas derivados de la amnios. Las células tratadas con exosomas produjeron más MUC5AC, un componente mucoso principal que forma la capa resbaladiza y protectora en la superficie del ojo. Las mediciones tanto de la proteína dentro de las células como de la cantidad secretada al fluido circundante mostraron un aumento claro dependiente de la dosis. Al mismo tiempo, menos células caliciformes presentaron marcadores de muerte celular programada, lo que indica que el tratamiento favoreció su supervivencia. Cuando los investigadores aumentaron directamente los niveles de miR-25-3p, estos efectos beneficiosos se intensificaron, lo que señala a este ARN pequeño como un ingrediente activo clave dentro de los exosomas.
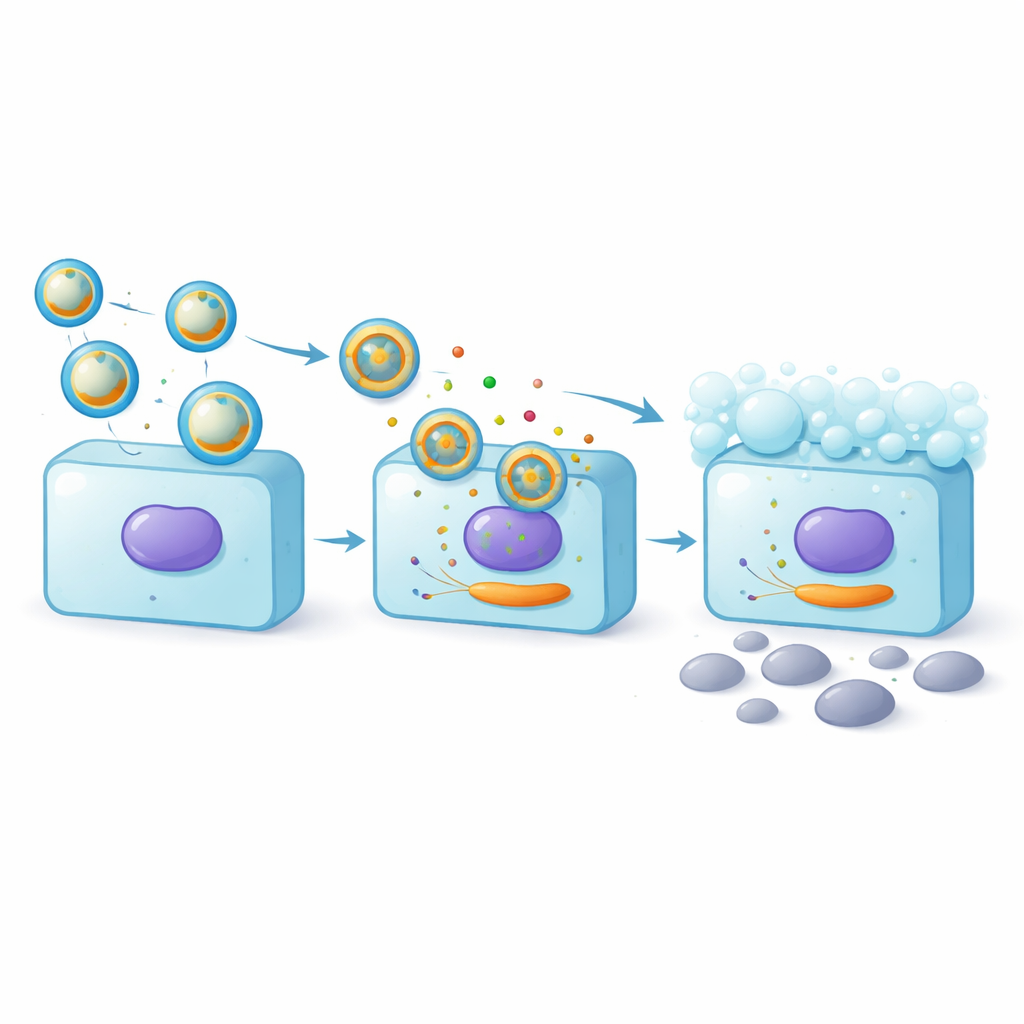
Apagar un disparador de muerte celular
Para entender cómo miR-25-3p protege a las células caliciformes, el equipo buscó su objetivo molecular y se centró en BCL2L11, un gen que promueve la muerte celular. Usando un sistema reportero, confirmaron que miR-25-3p puede unirse al mensajero de BCL2L11 dentro de la célula y atenuar su actividad. Las células caliciformes expuestas a exosomas amnióticos mostraron niveles más bajos de BCL2L11, especialmente cuando los exosomas estaban enriquecidos en miR-25-3p. Cuando los investigadores aumentaron artificialmente BCL2L11, algunos de los efectos protectores de miR-25-3p se perdieron: la muerte celular volvió a aumentar y la producción de moco disminuyó. Este tira y afloja demostró que una parte importante del beneficio de los exosomas proviene de que miR-25-3p reduce la expresión de BCL2L11 y así apoya tanto la supervivencia de las células caliciformes como su producción de mucina.
Qué podría significar esto para las personas con ojos secos
En términos sencillos, este estudio muestra que paquetes microscópicos liberados por tejido natal donado pueden entregar un mensaje genético protector a las células productoras de moco del ojo. Ese mensaje, transportado por miR-25-3p, ayuda a apagar un interruptor interno de autodestrucción y anima a las células caliciformes a fabricar más del moco que mantiene la superficie ocular lisa y defendida. Aunque estos experimentos se realizaron en cultivos celulares y se necesitan más estudios en modelos animales y pacientes, los hallazgos delinean una estrategia prometedora sin células: usar exosomas purificados en lugar de células enteras para restaurar una película lagrimal sana y posiblemente aliviar enfermedades en las que la superficie ocular se vuelve seca, inflamada y frágil.
Cita: Zhang, Y., Wu, W., Meng, T. et al. Human amnion epithelial cell-derived exosomal miR-25-3p enhances mucin expression in conjunctival goblet cells via downregulating BCL2L11. Sci Rep 16, 7958 (2026). https://doi.org/10.1038/s41598-026-37794-3
Palabras clave: enfermedad del ojo seco, moco de la película lagrimal, exosomas, terapia de la superficie ocular, células caliciformes