Clear Sky Science · es
Evaluación preliminar de la biodistribución y el direccionamiento de la sonda molecular fluorescente Cy7-SYL3C en un modelo murino de cáncer colorrectal EpCAM-positivo
Por qué esto importa para la detección del cáncer
El cáncer colorrectal es uno de los mayores responsables de muertes por cáncer en el mundo, en parte porque muchos tumores se detectan tarde. La herramienta de cribado principal hoy en día, la colonoscopia, es eficaz pero invasiva y molesta, por lo que mucha gente la evita. Este estudio explora un nuevo tipo de "trazador inteligente" luminoso que podría, en el futuro, ayudar a los médicos a ver los tumores intestinales antes y con mayor claridad, usando luz en lugar de un bisturí o un tubo largo.
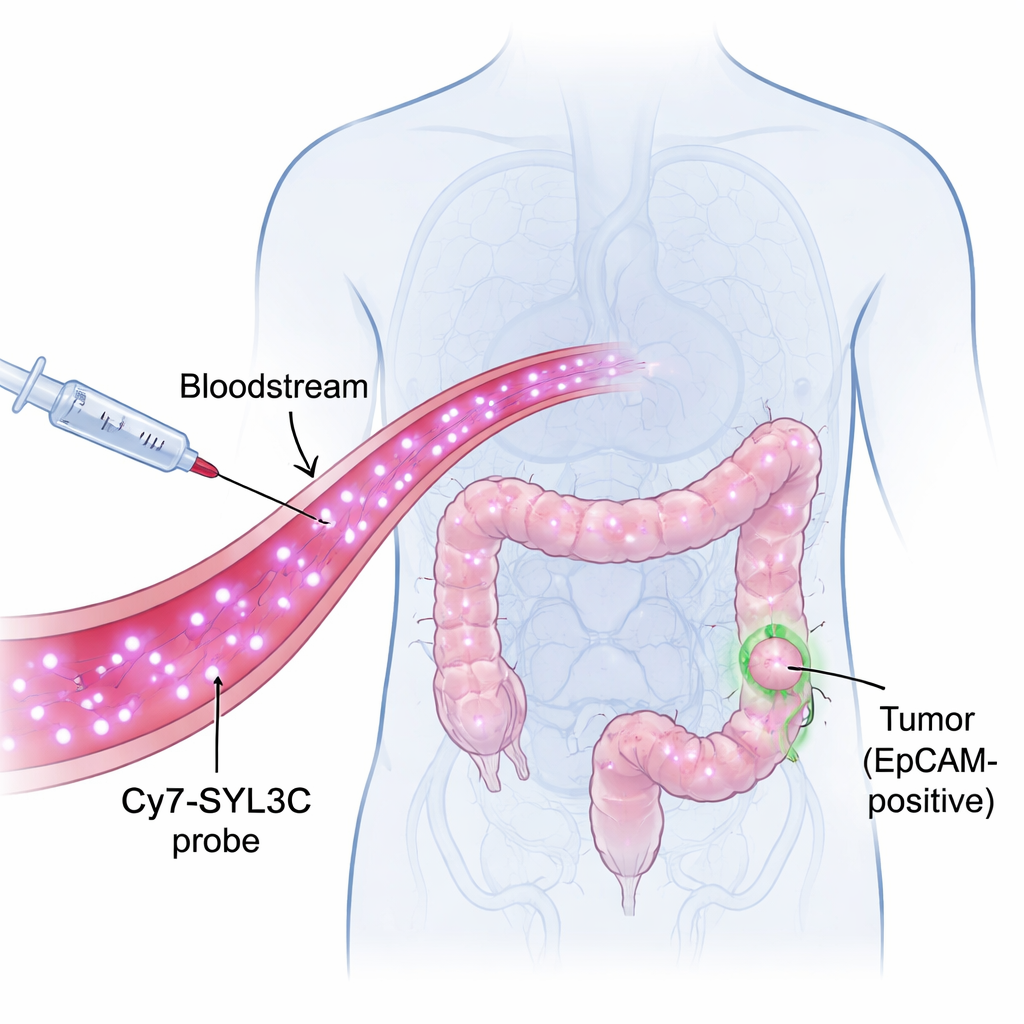
Una etiqueta luminosa que reconoce las células tumorales
Los investigadores se centraron en una molécula llamada EpCAM, que se encuentra en la superficie de muchas células de cáncer colorrectal pero es escasa en los tejidos sanos. Construyeron una sonda denominada Cy7-SYL3C uniendo un tinte de infrarrojo cercano (Cy7) a una corta cadena de ADN llamada aptámero (SYL3C) que puede reconocer EpCAM de manera parecida a como una llave encaja en una cerradura. La luz del infrarrojo cercano es invisible al ojo pero puede penetrar varios milímetros en el tejido, lo que permite que las cámaras capten señales desde el interior del cuerpo con alto contraste. La idea es simple: inyectar Cy7-SYL3C en el torrente sanguíneo, dejar que busque las células tumorales ricas en EpCAM y luego usar una cámara especial para hacer que esas células se iluminen sobre un fondo más oscuro.
Pruebas de seguridad y estabilidad en el laboratorio
Antes de probar la sonda en animales vivos, el equipo verificó si era estable y segura. Mezclaron Cy7-SYL3C con suero sanguíneo de ratón y de bovino y encontraron que la mayor parte de la sonda permaneció intacta durante al menos ocho horas, tiempo suficiente para realizar imágenes durante un procedimiento médico. Luego expusieron células humanas de cáncer colorrectal y células normales de colon a diferentes concentraciones de la sonda. El crecimiento celular prácticamente no cambió y, cuando la sonda se mezcló con glóbulos rojos, no provocó su hemólisis. Estas pruebas sugieren que Cy7-SYL3C es químicamente estable y suave con las células—requisitos clave para cualquier agente de imagen que pudiera usarse en pacientes.
Por dónde viaja la sonda en el cuerpo
Los científicos siguieron a continuación la ruta de Cy7-SYL3C en ratones sanos usando un sistema de imagen para pequeños animales. Poco después de la inyección, la señal más fuerte apareció en el hígado y los riñones, órganos que filtran y eliminan sustancias de la sangre. La señal hepática alcanzó su máximo alrededor de la primera hora y luego se desvaneció, mientras que los riñones continuaron brillando durante más tiempo, apuntando a la orina como una vía principal de eliminación de la sonda. Tras dos días, solo quedó una pequeña fracción de la señal original, y el examen microscópico de los órganos principales no mostró daños tisulares evidentes. Esto significa que la sonda se elimina con relativa rapidez y no parece dañar visiblemente los órganos vitales en este estudio a corto plazo.
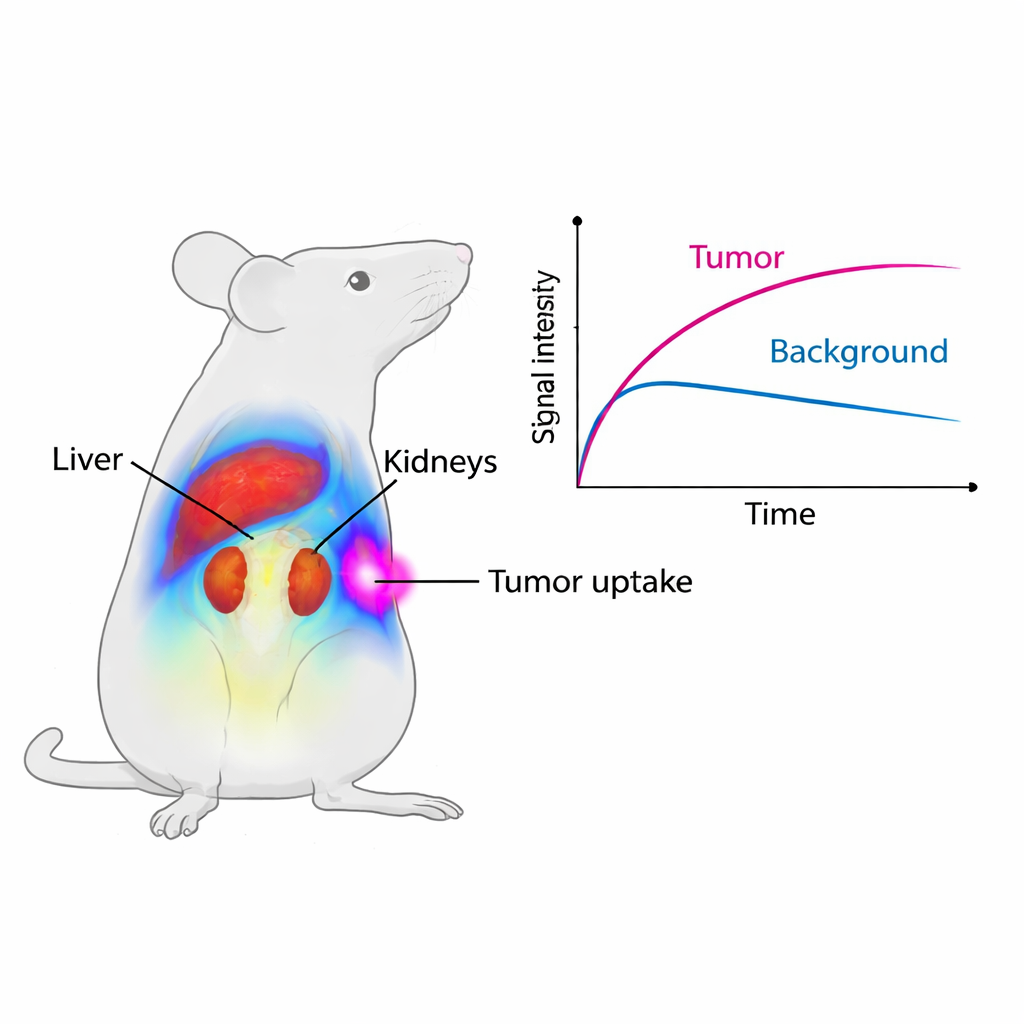
Localizándose en los tumores colorrectales
Para comprobar si Cy7-SYL3C realmente se dirige al cáncer, el equipo usó ratones implantados con tumores humanos colorrectales que expresan EpCAM. En solo cinco minutos tras la inyección, los tumores comenzaron a brillar en el sistema de imagen. Durante las primeras cuatro horas, la señal media en los tumores fue casi el doble que en los ratones cuyas lesiones habían sido "bloqueadas" previamente con un exceso de SYL3C no marcado, que ocupó temporalmente los sitios de EpCAM e impidió que la sonda fluorescente se uniera. La relación señal tumoral/músculo circundante superó el valor de uno y alcanzó su pico alrededor de las ocho horas, lo que significa que los tumores eran claramente más brillantes que su entorno durante una ventana de imagen útil. Estudios microscópicos detallados confirmaron que la sonda fluorescente se solapaba con la tinción de EpCAM en las células tumorales, mientras que los órganos normales mostraron poca o ninguna EpCAM.
Cómo podría guiar futuras cirugías y diagnósticos
Para un público no especialista, el mensaje principal es que Cy7-SYL3C actúa como un tinte inteligente que busca células de cáncer colorrectal y luego se elimina mayormente por los riñones. Parece estable, poco agresivo para las células y capaz de hacer que los tumores brillen de forma rápida y durante varias horas, lo que podría ayudar a los cirujanos a ver los bordes tumorales con más claridad en tiempo real o ayudar a los radiólogos a detectar áreas sospechosas durante procedimientos mínimamente invasivos. Aunque estos resultados provienen de experimentos tempranos en ratones y se necesita más trabajo antes de su uso en humanos, el estudio sienta una base importante para una nueva clase de trazadores basados en la luz que podrían hacer la detección y cirugía del cáncer colorrectal más precisas y menos invasivas.
Cita: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
Palabras clave: imagen del cáncer colorrectal, fluorescencia en el infrarrojo cercano, direccionamiento a EpCAM, sonda aptámero, guía para cirugía tumoral