Clear Sky Science · es
Clasificación del cáncer con radiómica en modelos preclínicos controlados
Leer el cáncer a partir de exploraciones y sangre
La atención oncológica moderna depende cada vez más de ordenadores que filtran imágenes médicas y pruebas de laboratorio en busca de patrones que a los humanos les resultan difíciles de ver. Este estudio plantea una pregunta simple pero importante: si queremos saber qué tipo de cáncer tiene un paciente, ¿es mejor leer la información oculta en sus exploraciones o en su sangre? Mediante experimentos cuidadosamente controlados en ratones, los investigadores compararon directamente estos dos enfoques para ver cuál ofrece respuestas más fiables.
Qué significa tomar una “biopsia virtual”
La radiómica es una técnica en rápido crecimiento que trata cada exploración médica como una fuente rica de datos en lugar de solo una imagen. Un software especializado recorre imágenes tridimensionales de TC de un tumor y las convierte en cientos de características numéricas que describen su forma, brillo y textura fina. En principio, estos patrones podrían reflejar la biología del tumor de manera similar a una biopsia, pero sin agujas ni cirugía —una llamada “biopsia virtual”. Sus defensores esperan que la radiómica ayude a clasificar cánceres, evaluar su agresividad y orientar decisiones de tratamiento. Pero hay preocupaciones: los resultados pueden ser difíciles de reproducir, fáciles de confundir por detalles técnicos y complicados de interpretar para los médicos.
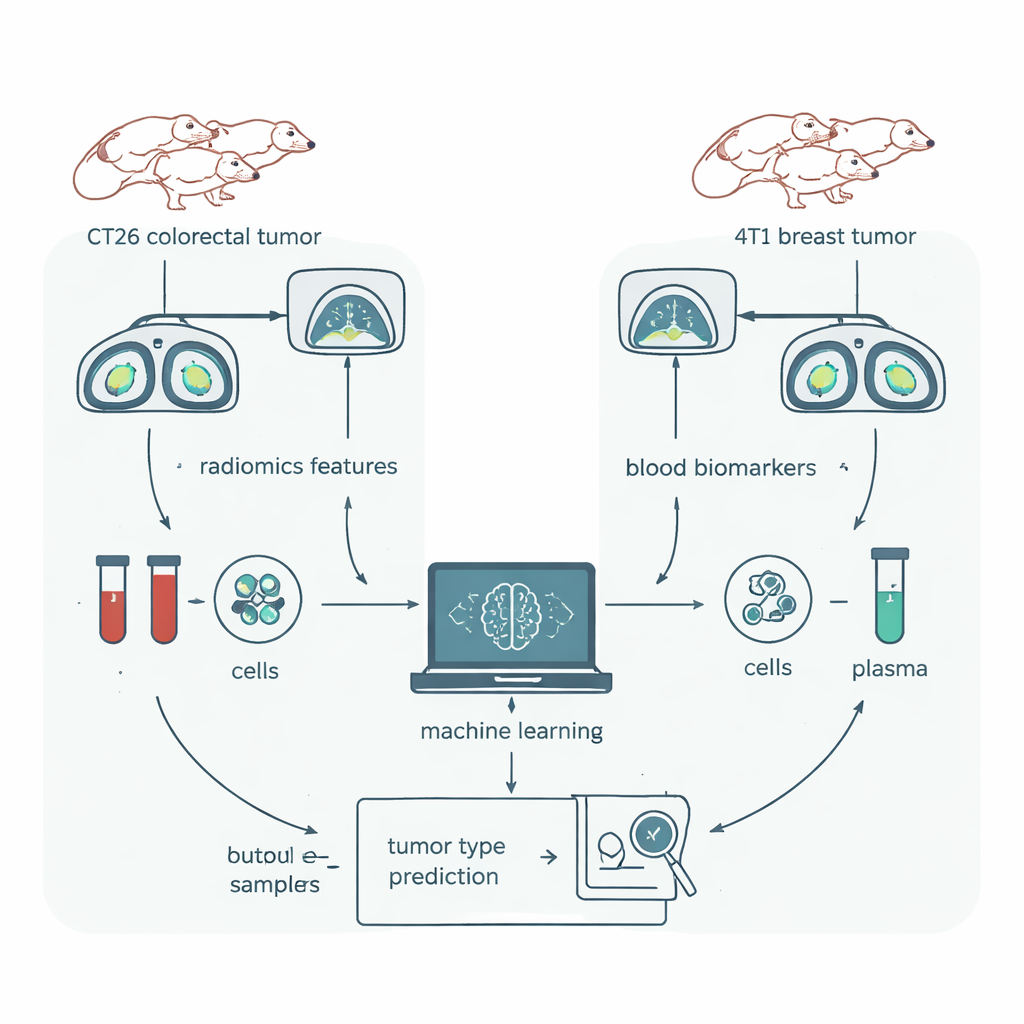
Una prueba justa cara a cara en ratones
Para someter a la radiómica a una prueba rigurosa, el equipo recurrió a un modelo murino donde casi todo podía controlarse. Se implantó en grupos de ratones genéticamente idénticos uno de dos tipos de tumor: CT26, un modelo de cáncer colorrectal, y 4T1, un modelo de cáncer de mama. Todos los animales eran de la misma cepa, sexo y edad similar, se mantuvieron en el mismo entorno y se escanearon en la misma máquina de TC. Los tumores se delinearon cuidadosamente en software 3D y un paquete de radiómica popular extrajo 1.409 características numéricas de cada exploración. En paralelo, los investigadores obtuvieron muestras de sangre de los mismos animales y midieron tipos de células inmunes y docenas de proteínas —biomarcadores que trabajos previos suyos ya habían demostrado capaces de distinguir estos modelos de cáncer casi a la perfección.
Comprimir miles de detalles de la imagen en una señal útil
La mayoría de las características de imagen crudas resultaron poco útiles: algunas apenas variaban entre ratones y muchas eran casi duplicados entre sí. Tras varias rondas de filtrado estadístico, solo quedaron 18 características radiómicas no redundantes, que describían en gran medida patrones sutiles de textura más que el tamaño o la forma simples. El equipo usó entonces un método estándar de aprendizaje automático, Random Forest, para ver qué tan bien estas características de imagen refinadas podían distinguir entre los dos tipos de tumor. También aplicaron herramientas de visualización para comprobar si los datos formaban naturalmente conglomerados separados para cada tipo de cáncer sin conocer las etiquetas de antemano.
Las señales de la sangre superan a las de la imagen
El contraste entre sangre e imagen fue llamativo. Cuando los investigadores redujeron los datos de células sanguíneas y proteínas plasmáticas a dos dimensiones, los dos tipos de tumor formaron conglomerados claramente separados, lo que confirmó que la sangre capturaba señales fuertes y específicas del tumor. En los datos de radiómica, sin embargo, aparecieron tres conglomerados mezclados, cada uno con una combinación de los dos cánceres, lo que sugiere que otros factores desconocidos estaban influyendo en las imágenes. En pruebas supervisadas, la radiómica sola clasificó el tipo de tumor con una precisión de alrededor del 87 por ciento —bueno, pero notablemente peor que el 96 por ciento de precisión obtenido con recuentos de células inmunes y el 99 por ciento logrado con proteínas plasmáticas. Añadir radiómica a los marcadores sanguíneos no mejoró el rendimiento; en algunas combinaciones redujo ligeramente la precisión. Un experimento adicional mostró que usar solo una pequeña región esférica dentro del tumor, en lugar de delinear toda la masa, empeoraba aún más el rendimiento de la radiómica, subrayando lo sensibles que son estas características a cómo se traza el tumor en la exploración.
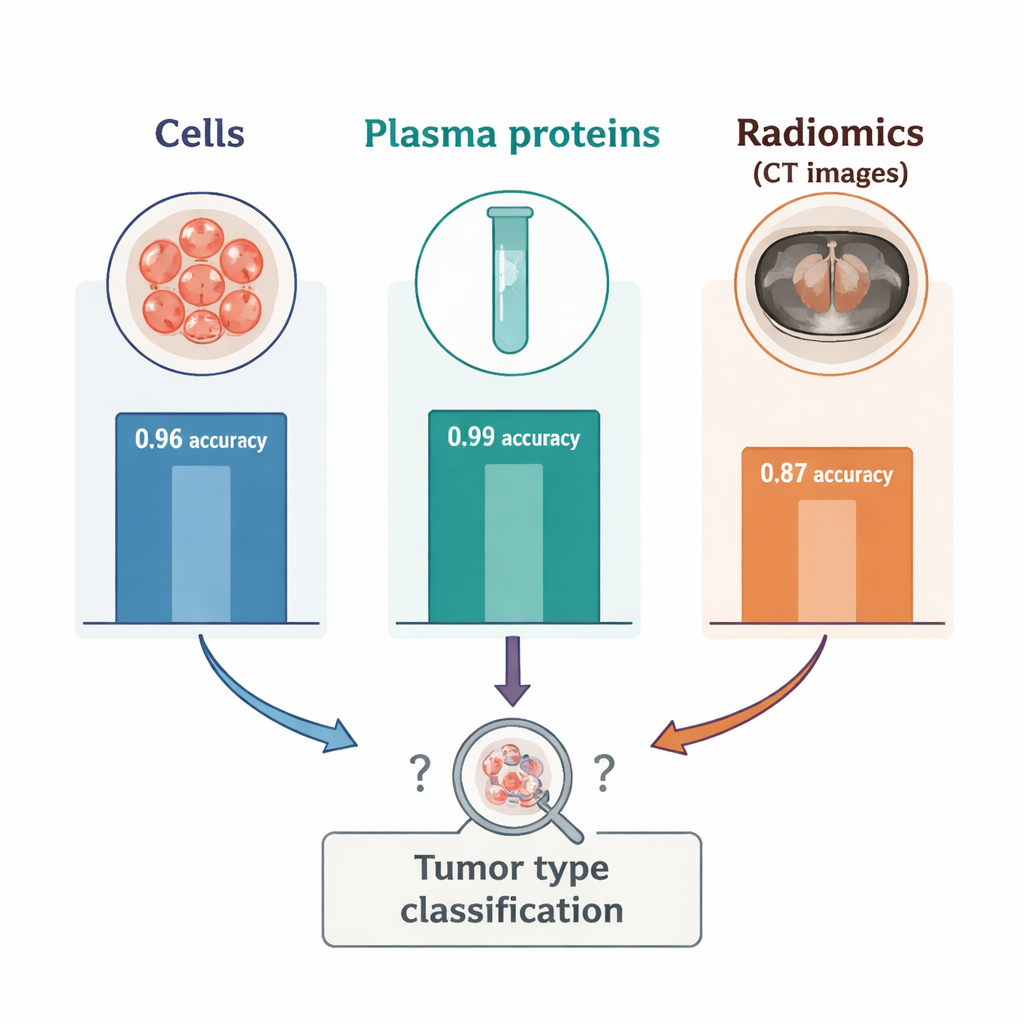
Qué significa esto para las pruebas de cáncer futuras
Para el lector no especializado, la conclusión es clara: aunque el análisis avanzado de imágenes puede aportar algunas pistas útiles, en este estudio fue superado por pruebas de sangre relativamente sencillas a la hora de distinguir entre dos tipos de cáncer. Incluso en un entorno de laboratorio estrechamente controlado con ratones idénticos e imágenes estandarizadas, pequeñas diferencias técnicas y la complejidad del procesamiento de imágenes parecieron difuminar la señal radiómica. Los autores concluyen que la radiómica aún no está lista para funcionar como un clasificador de cáncer autónomo y altamente fiable. En cambio, sostienen que será necesaria una estandarización más estricta de la imagen, mejores herramientas de contorno y vínculos más claros entre los patrones de imagen y la biología subyacente antes de que las biopsias virtuales puedan guiar con fiabilidad las decisiones clínicas junto con, o en lugar de, los biomarcadores sanguíneos bien establecidos.
Cita: Drover, K., Davis, D.A.S., Gosling, K. et al. Cancer classification with radiomics in controlled preclinical models. Sci Rep 16, 6647 (2026). https://doi.org/10.1038/s41598-026-37757-8
Palabras clave: radiómica, biomarcadores del cáncer, imagen médica, aprendizaje automático en oncología, análisis de sangre para cáncer