Clear Sky Science · es
Estrategia multidimensional permite ampliar de forma escalable la diversidad del metaboloma en fermentaciones microbianas
Por qué importan pequeños ajustes en la “fábrica” para nuevos medicamentos
Muchos de los medicamentos actuales proceden de compuestos naturales producidos por bacterias y hongos. Pero convertir un hallazgo prometedor en el laboratorio en un candidato farmacológico real suele fallar en un paso sorprendentemente terrenal: cultivar el mismo microbio en un recipiente distinto o a mayor escala. Este estudio plantea una pregunta simple pero crucial: ¿cómo mantener la producción química de un microbio estable y diversa cuando lo trasladamos de pequeñas placas de ensayo a matraces y biorreactores más grandes? La respuesta podría acelerar la búsqueda de la siguiente generación de antibióticos y otras terapias.
Tres formas de cultivar el mismo microbio
Los investigadores se centraron en una bacteria del suelo, Streptomyces griseochromogenes, conocida por producir muchos «metabolitos secundarios», pequeñas moléculas con potencial farmacológico. Compararon tres sistemas de cultivo comunes en la etapa inicial del descubrimiento: matraces agitados con deflectores (baffled shake flasks), placas microtituladoras de 48 pocillos tipo “flower” y un biorreactor agitado por paletas. En cada sistema midieron el crecimiento, la morfología y estructura celular y, de manera crucial, el patrón de señales químicas detectadas por espectrometría de masas, usada aquí como huella digital del metaboloma secretado por la bacteria. Primero aplicaron una regla clásica de ingeniería: mantener la disponibilidad de oxígeno igual en todos los sistemas y esperar un comportamiento similar. En lugar de ello, observaron que las curvas de crecimiento, las formas celulares y las huellas químicas diferían notablemente entre recipientes.
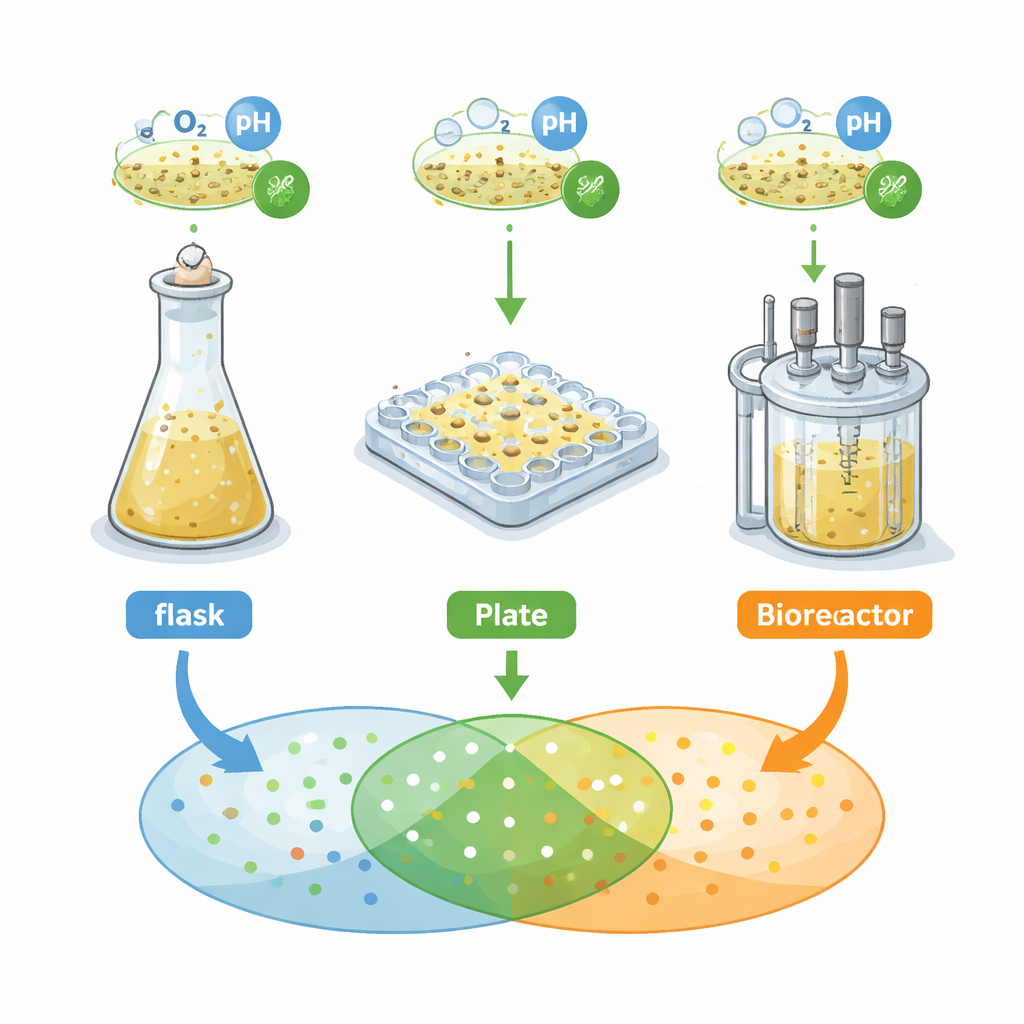
Cuando una sola regla no basta
Igualar solo el oxígeno produjo «huellas metabólicas» muy distintas —los conjuntos de señales de masa correspondientes a moléculas individuales. Solo alrededor del 18 % de estas señales se compartieron entre los tres sistemas. Las placas microtituladoras generaron muchas más señales distintas que los matraces o el biorreactor. El equipo probó después otro enfoque de un solo factor, cambiando la cantidad de etanol en el medio (una pequeña molécula que puede estimular la producción de metabolitos) o la velocidad de agitación, que altera la transferencia de oxígeno. Estos ajustes unidimensionales mejoraron modestamente la superposición en las huellas químicas, pero solo en torno a otro 18 % aproximadamente. En otras palabras, recetas simples como «añadir más oxígeno» o «añadir más etanol» no garantizan que un metabolito observado en un pocillo pequeño aparezca de forma fiable en un fermentador más grande.
Cómo la forma celular orienta la diversidad química
Para desentrañar qué importa realmente, los autores agruparon datos de 80 cultivos distintos y usaron un método estadístico que busca factores ocultos que modelan los resultados. Este análisis resaltó dos temas principales: el propio sistema de cultivo y la morfología de las células —si las bacterias crecían en gránulos compactos, mantos miceliales sueltos o filamentos finamente dispersos. Las condiciones que producían morfologías similares tendían a generar huellas metabólicas más parecidas y facilitaban el «escalado» de moléculas desde sistemas pequeños hasta el tanque agitado. Al seleccionar deliberadamente conjuntos de condiciones que generaran formas celulares comparables en los tres sistemas, los investigadores aumentaron la superposición en las señales químicas en aproximadamente un 50 % frente a igualar únicamente el oxígeno según la regla clásica.
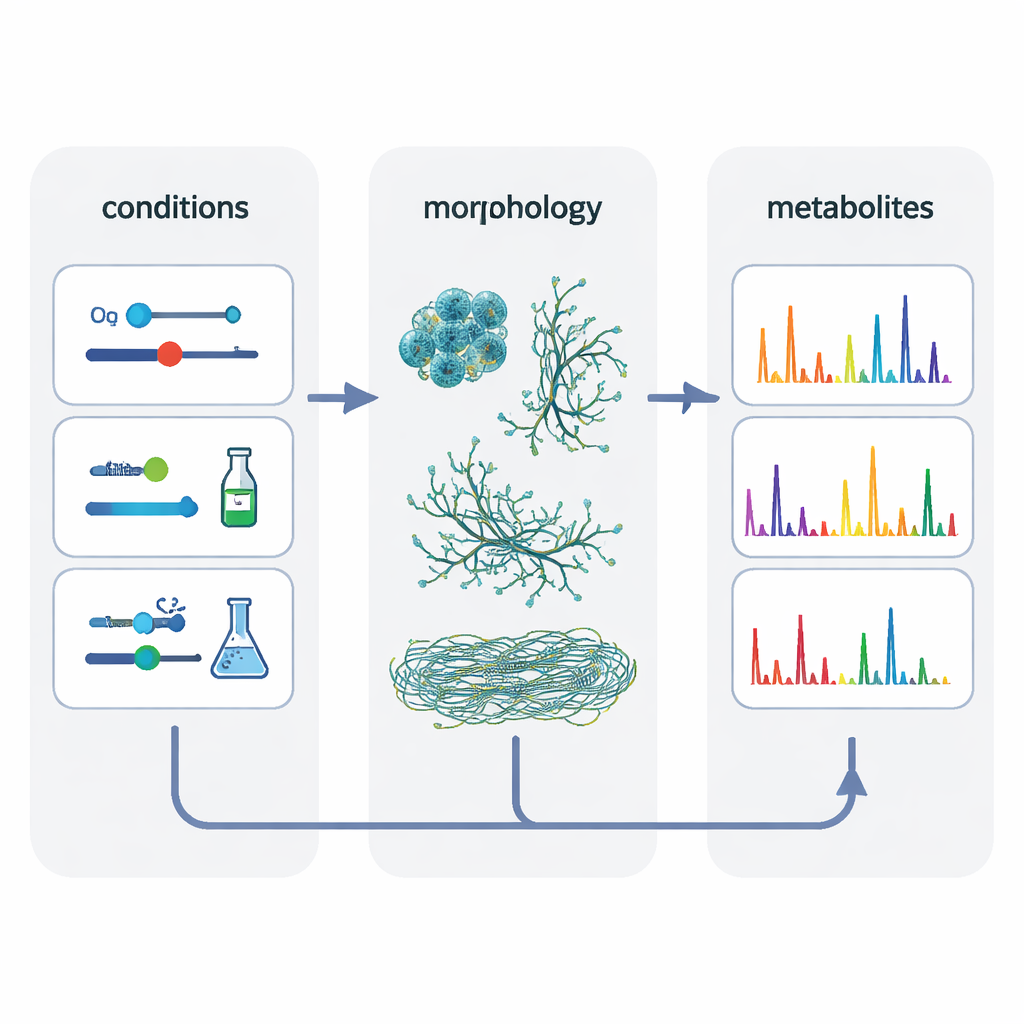
Familias químicas ocultas y moléculas específicas de cada sistema
Más allá de los recuentos simples de señales, el equipo construyó redes moleculares que agruparon señales relacionadas en familias de metabolitos estructuralmente similares. Las familias grandes a menudo contenían al menos un miembro presente en todos los sistemas de cultivo, lo que sugiere una química central robusta frente al cambio de escala. Pero muchas familias más pequeñas —y algunas moléculas individuales— aparecían solo en un tipo de recipiente. En particular, las placas de poliestireno microtituladoras produjeron la variedad más rica de compuestos, incluyendo muchas variantes de quelantes de hierro llamados desferrioxaminas y varios péptidos no ribosómicos. Los autores sugieren que tensiones sutiles en estas placas, como niveles más altos de especies reactivas de oxígeno, pueden empujar a las bacterias a diversificar su química, mientras que el biorreactor bien mezclado favorece un conjunto más reducido de estructuras «centrales».
Qué significa esto para encontrar nuevos productos naturales
Para los equipos de descubrimiento de fármacos, el mensaje es claro: no se puede confiar en una única regla de ingeniería o en una condición «óptima» si se desea tanto una rica diversidad química como un escalado fiable. En su lugar, se necesita una estrategia multidimensional que tenga en cuenta el tipo de recipiente, la transferencia de oxígeno, aditivos como el etanol y, de forma importante, el monitoreo en tiempo real de la morfología celular. Usar placas microtituladoras que imiten rasgos clave de los biorreactores y ajustar condiciones para producir formas de crecimiento similares puede aumentar mucho la probabilidad de que las moléculas prometedoras descubiertas a microlitros reaparezcan al cultivarlas en litros. Este enfoque ayuda a convertir hallazgos tempranos frágiles en candidatas robustas y reproducibles, aumentando las posibilidades de que nuevos productos naturales sobrevivan el viaje desde la bancada hasta el botiquín.
Cita: Lindig, A., Fataeri, M., Hubmann, G. et al. Multidimensional strategy enables scalable metabolome diversity in microbial fermentations. Sci Rep 16, 4084 (2026). https://doi.org/10.1038/s41598-026-37748-9
Palabras clave: descubrimiento de productos naturales, fermentación de Streptomyces, metabolómica, escalado en biorreactor, metabolitos secundarios