Clear Sky Science · es
Apuntamiento sinérgico del eje ARID2–MYC por pomalidomida y panobinostat supera la resistencia intrínseca a IMiD en el mieloma múltiple
Por qué esta investigación importa para los pacientes
El mieloma múltiple es un cáncer de las células que producen anticuerpos en la médula ósea que se ha vuelto más tratable pero sigue siendo rara vez curable. Muchos pacientes acaban dejando de responder a los fármacos estándar, lo que deja a los médicos con menos opciones. Este estudio explora por qué la combinación de dos tipos de medicamentos ya existentes —los llamados IMiD como la pomalidomida y fármacos que afectan el empaquetamiento del ADN denominados inhibidores de la histona deacetilasa (HDAC) como el panobinostat— puede trabajar en conjunto para matar células de mieloma, incluso cuando el cáncer ya es resistente a los IMiD por sí solos. Comprender esta cooperación a nivel molecular podría guiar mejores combinaciones terapéuticas y ayudar a más pacientes a beneficiarse de fármacos que ya tenemos.
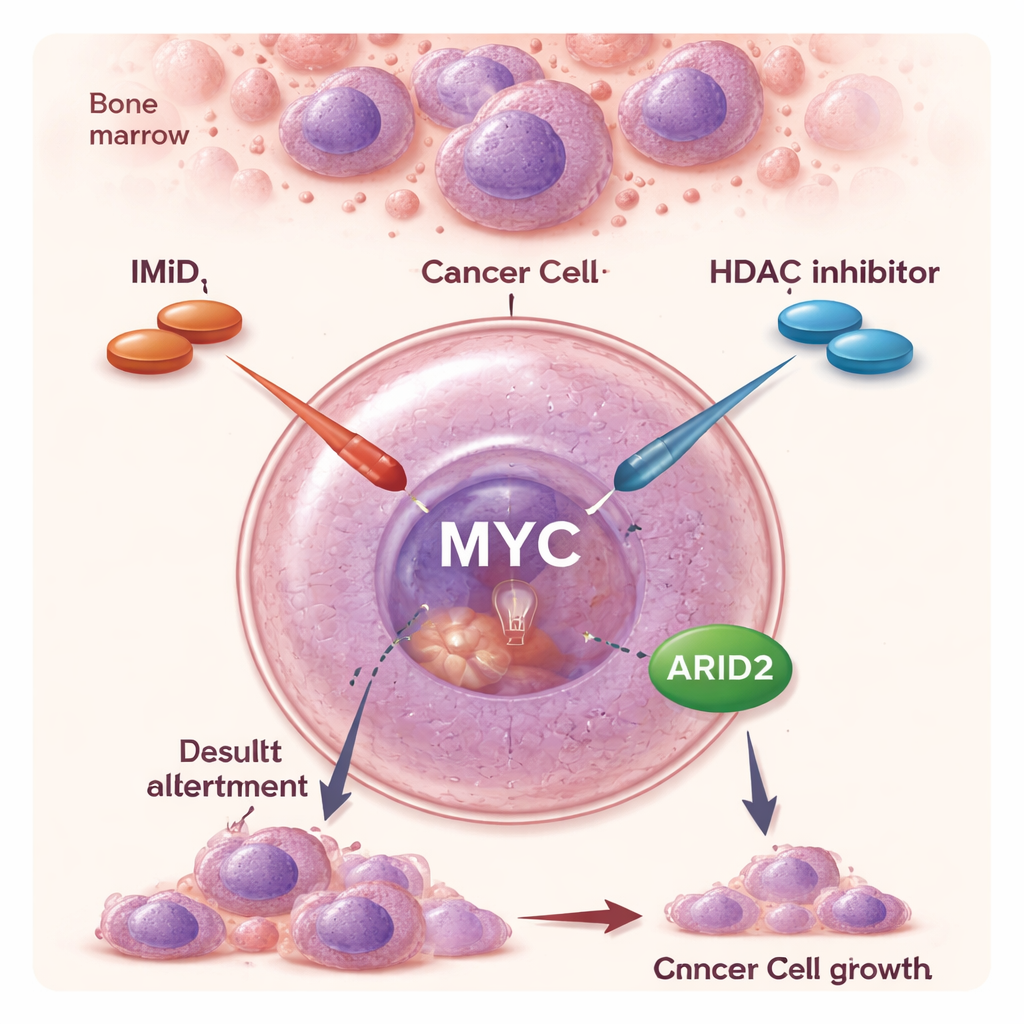
Dos clases antiguas de fármacos, una nueva alianza
En las últimas dos décadas, los IMiD y otros fármacos dirigidos han extendido considerablemente la supervivencia de las personas con mieloma múltiple. Los IMiD actúan de forma inusual: en lugar de simplemente bloquear una proteína, provocan que ciertas proteínas sean marcadas para su destrucción, borrándolas efectivamente de la célula. Con ello, debilitan señales clave de supervivencia de las que dependen las células de mieloma. Los inhibidores de HDAC como el panobinostat funcionan de otro modo: aflojan el empaquetamiento estrecho del ADN, remodelando de forma amplia qué genes se activan o se silencian. Como agentes únicos, los inhibidores de HDAC tienen efectos modestos y pueden causar efectos secundarios, pero ensayos clínicos sugirieron que combinarlos con IMiD produce una respuesta anticancerígena mucho más fuerte, incluso en pacientes cuyo tumor ya no responde a IMiD solos. Sin embargo, la razón molecular de esta sinergia había permanecido poco clara.
Un punto de presión común: reducir MYC
Los investigadores probaron sistemáticamente combinaciones de varios IMiD con distintos inhibidores de HDAC en un panel de líneas celulares de mieloma, usando un sistema de puntuación estandarizado para medir cuánto más potentes eran las combinaciones respecto a cada fármaco por separado. Encontraron que la combinación de pomalidomida y panobinostat mostró sinergia particularmente fuerte en la mayoría de los modelos celulares, y que este efecto dependía de una proteína llamada cereblón, que los IMiD utilizan para dirigir sus “victimas” proteicas hacia la destrucción. Al analizar la actividad génica global, el equipo descubrió que panobinostat y un inhibidor de HDAC de acción amplia relacionado apagaban con fuerza a MYC, un gen maestro del crecimiento descrito a menudo como el “motor oncogénico” en células cancerosas, y que los IMiD añadían presión adicional sobre ese mismo nodo. Cuando los científicos forzaron a las células de mieloma a seguir produciendo MYC desde una fuente insensible al fármaco, el potente efecto de la pareja farmacológica desapareció en gran medida, demostrando que la supresión de MYC es central en su cooperación.
Rompiendo la resistencia por una vía alternativa
Algunas células de mieloma son intrínsecamente resistentes a los IMiD: aunque los objetivos tempranos esperados se destruyen, MYC y otras señales de supervivencia no se silencian correctamente, por lo que las células siguen proliferando. En uno de esos modelos resistentes, la vía estándar de IMiD que enlaza los objetivos tempranos con MYC estaba “desacoplada”. El equipo se preguntó si una ruta alternativa aún podría conectar a los IMiD con MYC. Se centraron en ARID2, un componente de una gran máquina de remodelado del ADN llamada complejo SWI/SNF. Trabajos previos habían mostrado que la pomalidomida puede marcar ARID2 para su destrucción y que esto ayuda a reducir MYC. En las células resistentes, la pomalidomida sola redujo ARID2 solo modestamente, en parte porque la célula aumentó su producción de ARID2 en respuesta. Al añadir panobinostat, se suprimió el gen ARID2 en sí, superando este bucle de retroalimentación. Juntos, los dos fármacos redujeron con fuerza la proteína ARID2 y luego MYC, llevando a una potente eliminación de células cancerosas incluso en líneas resistentes a IMiD.
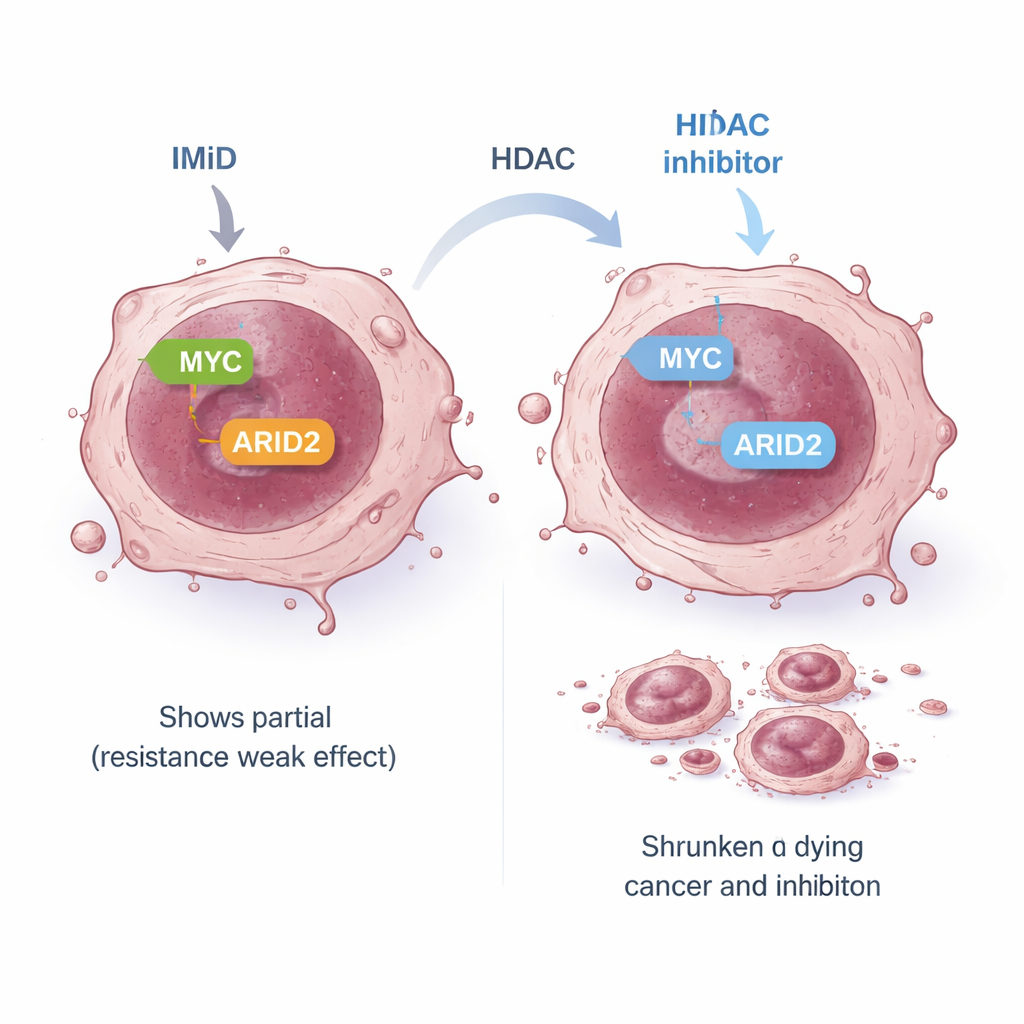
Exponiendo una vulnerabilidad más amplia en las células cancerosas
Como ARID2 es solo un miembro del complejo SWI/SNF, los autores se preguntaron si todo el complejo podría ser un punto débil terapéutico. Encontraron que los inhibidores de HDAC reducen los niveles de varios componentes de SWI/SNF, y que una pequeña molécula distinta diseñada para bloquear los motores centrales del complejo (BRG1/BRM) por sí sola puede frenar el crecimiento de las células de mieloma y reducir MYC. De manera importante, este inhibidor de SWI/SNF también funcionó de forma sinérgica con tanto pomalidomida como panobinostat, y una combinación de tres fármacos redujo aún más ARID2 y MYC mientras suprimía de forma potente la proliferación celular. Al sondear qué enzimas HDAC específicas estaban implicadas, los investigadores señalaron a HDAC1 como un actor clave que ayuda a sostener la vía ARID2–MYC, mientras que otras HDAC parecen influir en MYC a través de rutas paralelas.
Qué significa esto para el tratamiento futuro del mieloma
Para no especialistas, el mensaje central es que las células de mieloma parecen depender de un “centro de control del crecimiento” compartido centrado en MYC, y que hay más de un camino que conduce a ese centro. La terapia estándar con IMiD golpea principalmente una vía; en algunos cánceres resistentes, esa vía está bloqueada, por lo que MYC permanece activo. Este estudio muestra que existe una ruta alternativa —que pasa por ARID2 y el complejo SWI/SNF— que sigue abierta, y que usar panobinostat junto con pomalidomida puede cerrarla. Al combinar deliberadamente fármacos que presionan sobre MYC desde múltiples direcciones, los clínicos podrían ser capaces de superar algunas formas de resistencia intrínseca y, potencialmente, usar dosis más bajas de cada medicación. Aunque se necesitan más estudios preclínicos y clínicos, los hallazgos proporcionan un plan más claro para diseñar combinaciones inteligentes, basadas en mecanismos, para pacientes con mieloma múltiple de difícil tratamiento.
Cita: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Palabras clave: mieloma múltiple, resistencia a fármacos, pomalidomida, panobinostat, MYC