Clear Sky Science · es
Modificaciones alteradas de histonas en los intestinos de Aedes aegypti tras la exposición al virus de la fiebre de la cuenca del Rift
Por qué los genes del mosquito importan para la salud humana
La fiebre de la cuenca del Rift es un virus que enferma al ganado y a las personas en partes de África, y se transmite por mosquitos. Para controlar los brotes, los científicos necesitan entender no solo el virus en sí, sino también cómo responden los mosquitos cuando ingieren sangre infectada. Este estudio explora el interior del intestino del mosquito a un nivel inusualmente detallado, preguntando cómo el virus modifica el empaquetamiento del ADN del mosquito para activar o silenciar genes críticos, cambios que podrían influir en si el insecto se convierte en un transmisor eficaz o pobre de la enfermedad.
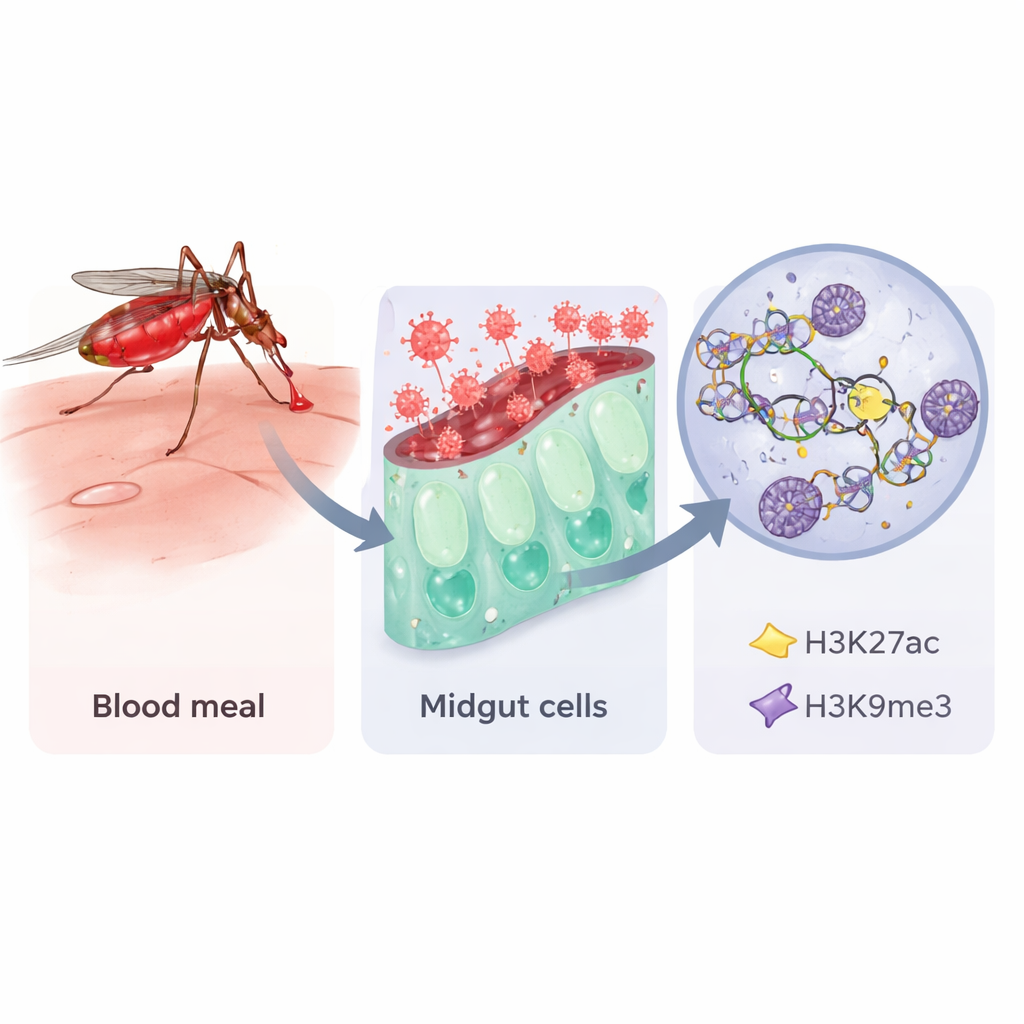
Abriendo el libro del ADN del mosquito
Al igual que las personas, los mosquitos no cambian las letras de su ADN cuando encuentran una infección, pero sí pueden alterar cuán compactado está ese ADN. Los autores se centraron en dos etiquetas químicas en proteínas histonas, que actúan como carretes para el ADN. Una etiqueta, denominada H3K27ac, suele marcar tramos de ADN abiertos y activos; la otra, H3K9me3, se asocia a regiones silenciadas. Usando un método sensible conocido como CUT&RUN, combinado con secuenciación de ARN, el equipo examinó estas marcas y la actividad génica en los intestinos de Aedes aegypti tras tres tipos de comidas: azúcar simple, una comida de sangre normal o sangre que contenía una cepa vacunal del virus de la fiebre de la cuenca del Rift. Muestrearon los intestinos a los uno, tres y siete días después de la ingesta para capturar etapas tempranas, intermedias y tardías de la infección.
Cómo una simple comida de sangre reconfigura el intestino
Una comida de sangre por sí sola, incluso sin virus, provocó cambios generalizados en la actividad génica del intestino medio. Miles de genes modificaron su actividad un día después de alimentarse, especialmente los implicados en la digestión de proteínas, el manejo de la energía y la construcción de nuevos componentes celulares. Muchos de estos genes se encontraban cerca de regiones marcadas por H3K27ac, coherente con la idea de que la sangre desencadena la apertura de barrios genómicos específicos necesarios para la digestión y la producción de huevos. En los días siguientes, a medida que se digería la sangre, el patrón evolucionó: la maquinaria productora de energía permaneció activa y, más tarde, se vieron afectados genes implicados en la organización de los cromosomas y el ciclo celular. Los mosquitos alimentados con azúcar, en contraste, mostraron patrones más estables, lo que sugiere que no tomar una comida de sangre puede dar lugar a un paisaje del ADN diferente, posiblemente relacionado con el envejecimiento.
Cuando el virus se encuentra con las defensas del intestino
Añadir el virus de la fiebre de la cuenca del Rift a la sangre cambió el panorama. Al principio, uno y tres días después de alimentarse, los intestinos de los mosquitos expuestos al virus intensificaron la expresión de genes vinculados a la defensa inmune y la señalización celular, más allá de los cambios provocados solo por la sangre. Al mismo tiempo, las relaciones habituales entre las marcas de histonas y los genes cercanos se volvieron más complejas. En particular, el día tres muchas regiones marcadas por la etiqueta normalmente represiva H3K9me3 perdieron esa marca, y cientos de genes próximos se activaron, incluidos genes implicados en el control de la expresión génica, la transmisión de señales dentro de la célula y la gestión de la forma y la polaridad celular. Para el día siete, cuando aproximadamente la mitad de los mosquitos portaba virus infeccioso, la actividad génica global en los intestinos expuestos disminuyó, los genes relacionados con la respuesta inmune se atenuaron y las marcas activadoras H3K27ac se vieron ampliamente reducidas en comparación con los controles alimentados solo con sangre.
Pistas sobre trucos virales y defensas del mosquito
Al correlacionar la actividad génica con los cambios de histonas cercanos, los investigadores identificaron un pequeño conjunto de genes cuyo comportamiento resulta especialmente sugestivo. Algunos genes que ayudan a organizar estructuras de membrana o a mover materiales dentro de las células aumentaron su actividad mientras sus marcas activadoras locales disminuían, lo que los convierte en candidatos para ayudar al virus a ensamblarse o desplazarse dentro de la célula. Otros, como genes relacionados con la detoxificación de moléculas reactivas o el reconocimiento de patógenos, mostraron patrones coherentes con funciones antivirales. Un gen destacado, que porta un dominio proteico conocido por factores antivirales humanos, aumentó su ARN mientras perdía tanto marcas activadoras como represoras, lo que sugiere una fuerte presión reguladora durante la infección. El estudio también resaltó una vía de polaridad celular, denominada smoothened/hedgehog, cuyos componentes se vieron atenuados en la fase tardía de la infección, en consonancia con evidencia de que muchos virus prefieren células altamente polarizadas.
Qué implica esto para el control de las enfermedades transmitidas por mosquitos
Para un no especialista, el mensaje clave es que las células del intestino del mosquito no aceptan pasivamente la invasión viral. En cambio, remodelan rápidamente cómo empaquetan su ADN, primero para impulsar la digestión y la reproducción después de una comida de sangre y luego para desplegar—o a veces relajar—defensas contra el virus de la fiebre de la cuenca del Rift. Dos marcas de histonas, H3K27ac y H3K9me3, cambian de forma compleja durante este tira y afloja, influyendo en qué genes pueden responder. Aunque solo una fracción de los cambios génicos pudo vincularse directamente a estas marcas, el trabajo muestra que las señales epigenéticas son una capa importante de la respuesta del mosquito a la infección. A largo plazo, comprender estos interruptores podría ayudar a los científicos a diseñar nuevas estrategias para hacer a los mosquitos menos capaces de portar virus, añadiendo otra herramienta en la lucha contra las enfermedades emergentes transmitidas por mosquitos.
Cita: Ogg, H.A., Mikol, Z.M., King, D.C. et al. Altered histone modifications in Aedes aegypti midguts following Rift Valley fever virus exposure. Sci Rep 16, 6605 (2026). https://doi.org/10.1038/s41598-026-37729-y
Palabras clave: virus de la fiebre de la cuenca del Rift, Aedes aegypti, epigenética de mosquitos, modificaciones de histonas, competencia del vector