Clear Sky Science · es
Mecanismo y divergencia evolutiva de una nueva hidrolasa de polivinil alcohol oxidado en Stenotrophomonas rhizophila QL-P4
Por qué un plástico “verde” común sigue presente en la naturaleza
El alcohol polivinílico, o PVA, aparece en todo, desde cápsulas de detergente para la ropa hasta recubrimientos textiles y papel. A menudo se comercializa como respetuoso con el medio ambiente porque, en principio, los microbios pueden degradarlo. Sin embargo, en ríos, suelos y océanos reales, este material similar al plástico se descompone muy lentamente y puede persistir durante décadas en forma de microplásticos y nanoplásticos. Este estudio examina de cerca una de las herramientas naturales para combatir el PVA: una enzima recién descubierta procedente de una bacteria del suelo que puede cortar este polímero resistente en fragmentos más pequeños y menos peligrosos.
Un pequeño ayudante del suelo con una gran tarea
Investigadores aislaron previamente una bacteria llamada Stenotrophomonas rhizophila QL-P4 de suelo de montaña en China y observaron que puede crecer utilizando PVA como fuente de carbono. En el trabajo nuevo se centraron en un único gen sospechoso, denominado BAY15_0160, que parecía codificar una enzima capaz de cortar PVA oxidado. Mediante la eliminación cuidadosa de este gen, su reincorporación y la sobreexpresión forzada en la bacteria, demostraron que BAY15_0160 es esencial para una degradación eficiente del PVA. Cuando se eliminó el gen, el microbio perdió alrededor del 40 % de su capacidad para consumir PVA; al restaurar el gen, el rendimiento volvió, confirmando que su producto es un actor clave en la vía de degradación.
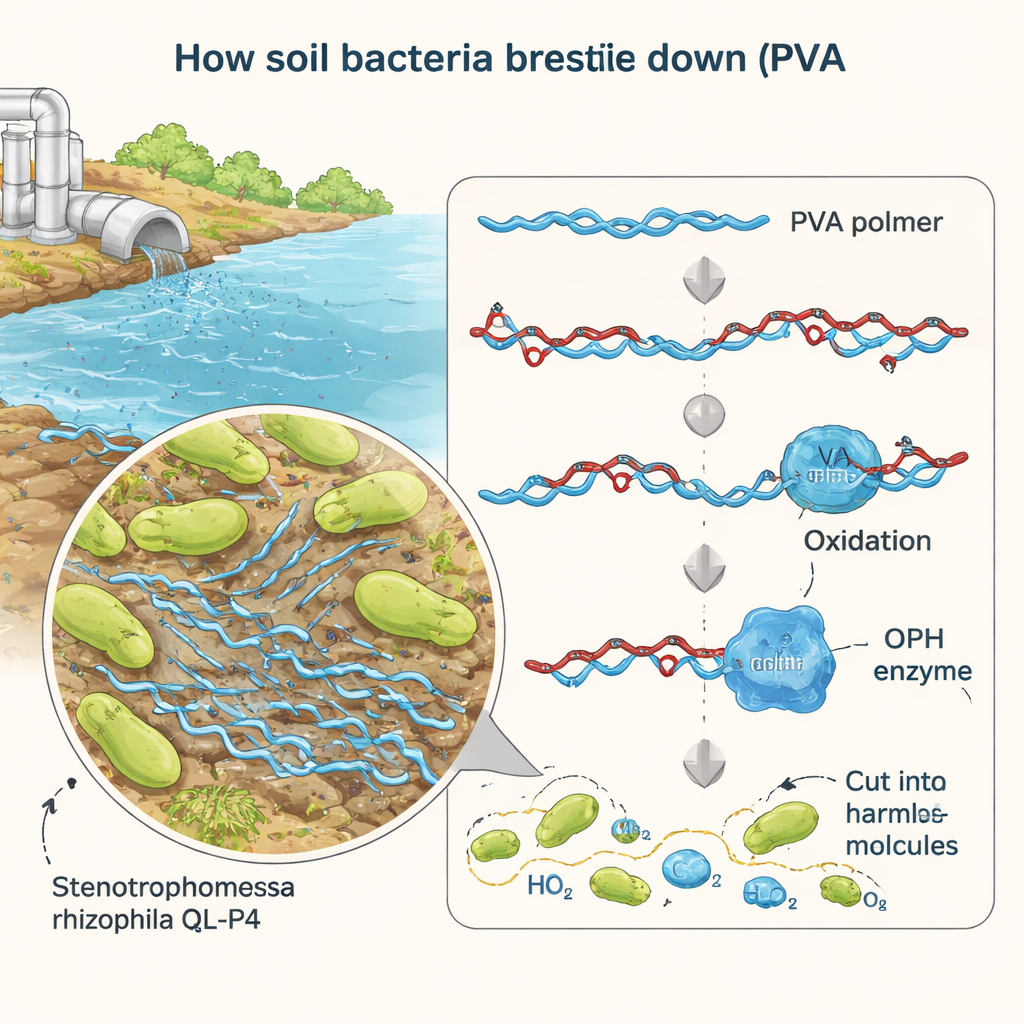
Midiendo cómo realiza su trabajo la enzima
Para estudiar la enzima en detalle, el equipo la produjo en grandes cantidades usando cepas de laboratorio de Escherichia coli. Purificaron la proteína, que resultó tener aproximadamente 35 kilodaltons, y probaron su actividad en distintas condiciones. Usando una molécula de ensayo simple que libera un tinte amarillo cuando se corta, siguieron la velocidad de trabajo de la enzima a varias temperaturas y niveles de acidez. La enzima fue más activa alrededor de la temperatura ambiente (30 °C) y en un pH neutro similar al de muchas aguas naturales. Bajo estas condiciones suaves mostró alta eficiencia catalítica, lo que significa que cada molécula de enzima puede procesar muchas moléculas de sustrato por segundo; una noticia alentadora para posibles aplicaciones de limpieza en el mundo real.
Acercándose a las tijeras moleculares
Las enzimas son las máquinas diminutas de la naturaleza, y su forma determina lo que pueden hacer. Los investigadores utilizaron programas de predicción de vanguardia, RoseTTAFold y AlphaFold, para construir modelos tridimensionales de la enzima que corta PVA, ahora reconocida como una nueva hidrolasa de PVA oxidado, u OPH. Ambas herramientas coincidieron en que la enzima presenta el plegamiento clásico de una “hidrolasa alfa/beta” que se encuentra en muchas tijeras biológicas. En su núcleo se halla un motivo corto—a menudo escrito como Gly–X–Ser–X–Gly—que ayuda a posicionar un trío de aminoácidos (serina, aspartato e histidina) para atacar enlaces químicos. Simulaciones por ordenador mostraron fragmentos de PVA oxidado alojándose en esta ranura, con la serina clave probablemente realizando el primer corte en la cadena.
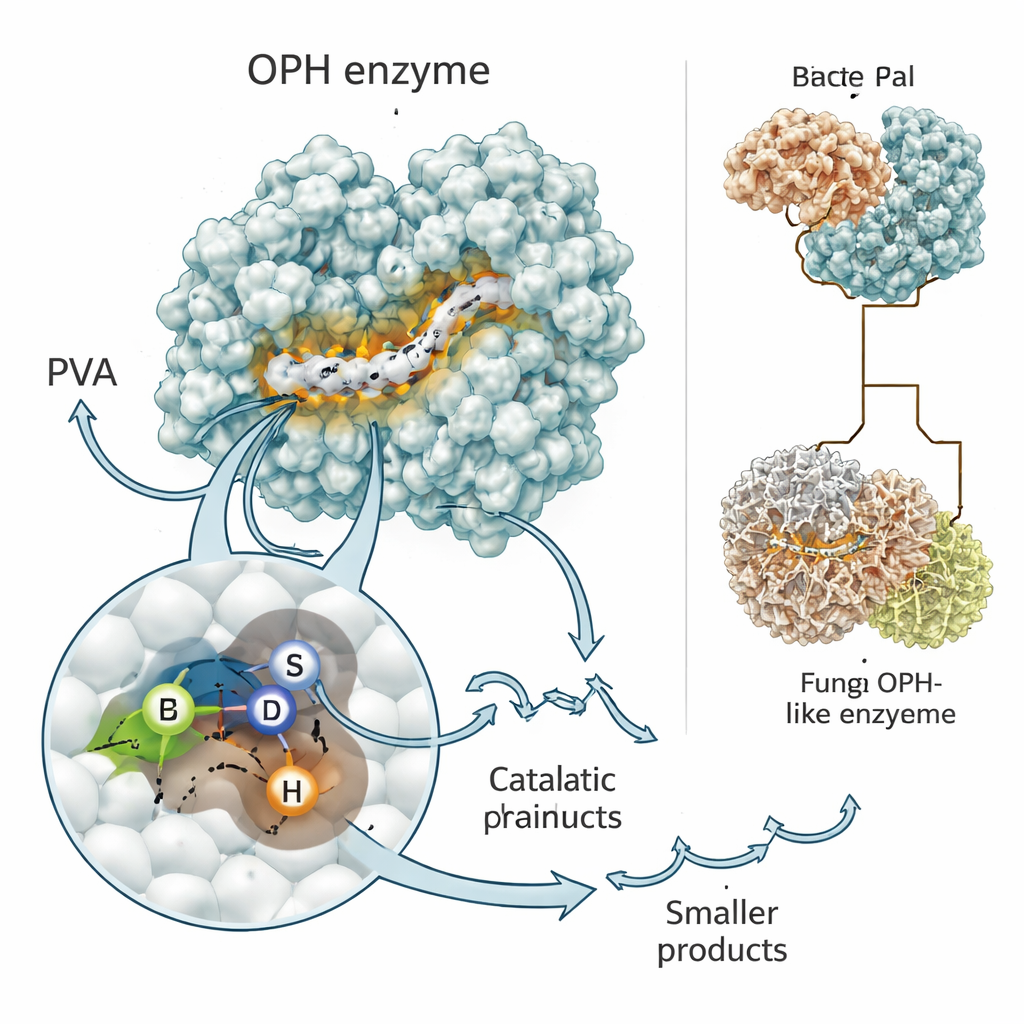
Señales, conmutadores y giros evolutivos
El equipo también exploró qué partes de la enzima son absolutamente necesarias para que funcione en la bacteria. Una región cercana al extremo inicial de la proteína actúa como un código postal, dirigiendo la enzima hacia el exterior de la célula, donde realmente está el polímero PVA. Otra región contiene el motivo activo que sujeta y corta los enlaces carbono–carbono del plástico. Cuando los científicos diseñaron versiones del gen que carecían ya sea del segmento señal o del motivo del sitio activo, la bacteria seguía sintetizando ARN del gen pero ya no podía digerir el PVA de forma eficiente. Al comparar muchas bacterias y hongos, hallaron parientes de esta enzima que comparten la misma región central de “corte” pero difieren en partes adicionales, incluida una llamativa versión fúngica que fusiona el dominio cortante con un transportador integrado, lo que sugiere una estrategia de importación y digestión aún más eficiente en entornos extremos como las rocas antárticas.
Qué significa esto para la limpieza de la contaminación por plástico
Para el público general, el mensaje principal es que los científicos están aprendiendo cómo algunos microbios degradan de forma natural un plástico supuestamente biodegradable que de otro modo permanece demasiado tiempo. Este estudio identifica una única enzima, OPH de S. rhizophila QL-P4, como unas tijeras moleculares potentes que operan en condiciones suaves y atacan un paso crucial en la descomposición del PVA. Al comprender su estructura, condiciones de trabajo y parientes evolutivos, los investigadores pueden comenzar a diseñar cepas microbianas mejores o mezclas de enzimas adaptadas a plantas de tratamiento de aguas residuales, efluentes industriales o suelos contaminados. A largo plazo, estos conocimientos nos acercan a soluciones prácticas basadas en la biología para gestionar los residuos plásticos, en lugar de dejarlos acumularse en el medio ambiente.
Cita: Zhou, Y., Bold, N., Feng, J. et al. Mechanism and evolutionary divergence of a novel oxidized polyvinyl alcohol hydrolase in Stenotrophomonas rhizophila QL-P4. Sci Rep 16, 6411 (2026). https://doi.org/10.1038/s41598-026-37715-4
Palabras clave: alcohol polivinílico, biodegradación, contaminación por plástico, enzimas microbianas, biorremediación