Clear Sky Science · es
Clasificación del metabolismo de lípidos en gliomas
Por qué importan las grasas en los tumores cerebrales
Los tumores cerebrales llamados gliomas están entre los cánceres más peligrosos, pero pacientes con un diagnóstico aparentemente igual pueden tener resultados muy diferentes. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿cómo influyen las formas en que los tumores usan las grasas —los lípidos del organismo— en su agresividad, en su respuesta al tratamiento y en si podemos detectar estas diferencias en las exploraciones cerebrales de rutina? Siguiendo el uso de lípidos en cientos de tumores, los autores revelan subtipos ocultos de glioma que podrían cambiar cómo los médicos predicen el pronóstico y diseñan terapias.
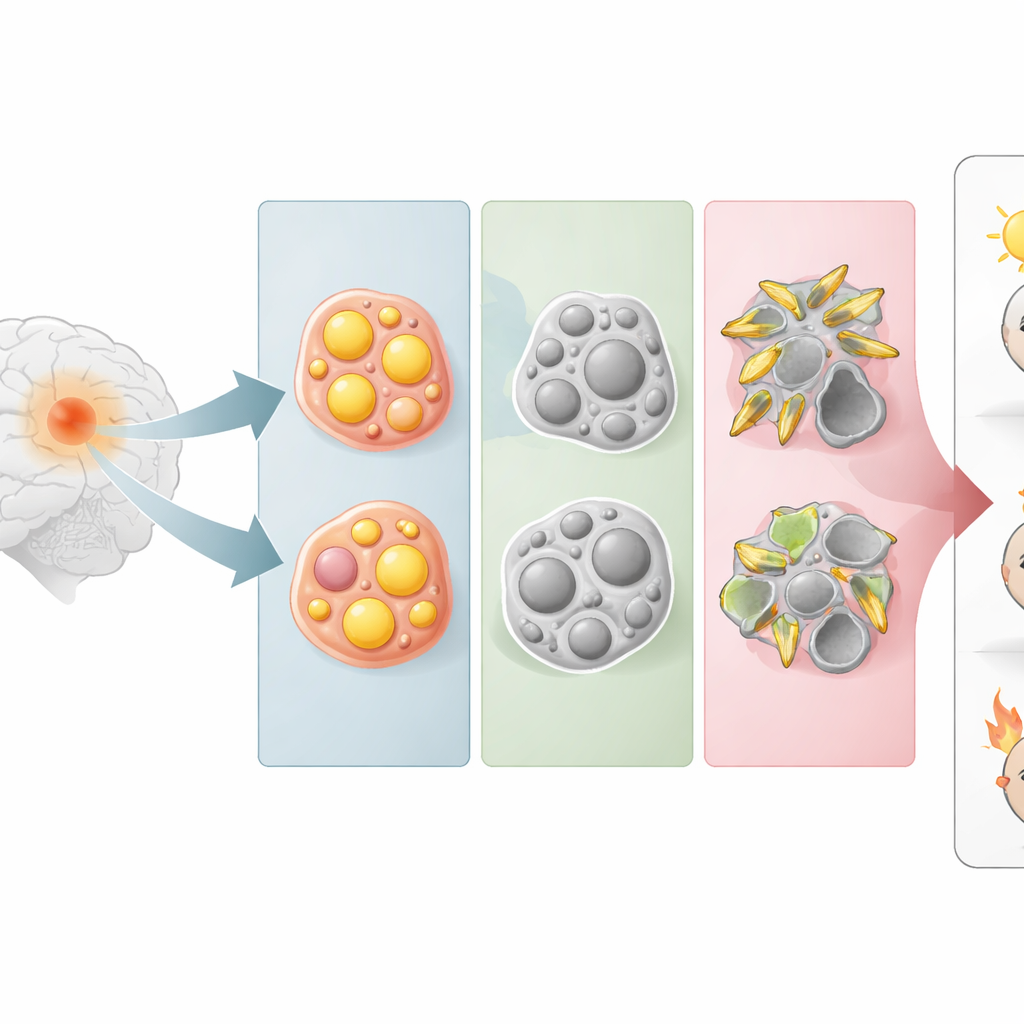
Tres caras ocultas del mismo tumor cerebral
En lugar de partir de la apariencia de las células tumorales al microscopio, los investigadores agruparon los gliomas según la intensidad con que activan cinco vías lipídicas principales, incluidas las que manejan grasas esteroides, triglicéridos y esfingolípidos (componentes clave de las membranas celulares). Usando perfiles de actividad génica de grandes bases de datos públicas de tumores, encontraron que los gliomas se distribuían naturalmente en tres grupos. Un grupo dependía en gran medida del metabolismo de esteroides (tipo ST), otro del metabolismo de triglicéridos (tipo TC) y un tercero del metabolismo de esfingolípidos (tipo SP). Estos agrupamientos metabólicos atraviesan las categorías tumorales clásicas, revelando que células con hábitos lipídicos similares pueden encontrarse en gliomas que por otros criterios parecen distintos.
Del metabolismo al pronóstico del paciente
El equipo preguntó luego cómo se relacionaban estos tres estilos de uso de grasas con resultados reales. Los pacientes cuyos tumores se clasificaron como tipo ST generalmente tuvieron la supervivencia más larga, y sus tumores eran con mayor frecuencia de grado más bajo y presentaban cambios genéticos conocidos como favorables. En el otro extremo, los tumores tipo SP eran por lo general glioblastomas de alto grado sin mutaciones protectoras y se daban más en pacientes de mayor edad. Incluso tras ajustar estadísticamente por grado tumoral y marcadores genéticos clave, pertenecer al tipo SP siguió prediciendo un pronóstico mucho peor, lo que sugiere que cómo el tumor maneja los esfingolípidos captura una dimensión independiente de riesgo que las pruebas estándar no detectan.
Un vecindario hostil dentro del cerebro
Ahondando más, los autores examinaron el microambiente tumoral —la mezcla de células inmunitarias, vasos sanguíneos y tejido de soporte alrededor del cáncer. Los tumores tipo SP mostraron un paisaje inmune concurrido y conflictivo, con presencia tanto de células inmunes orientadas al ataque como de células supresoras, además de señales fuertes que atenúan respuestas antitumorales efectivas. Vías vinculadas al crecimiento celular rápido, la invasión, la formación de nuevos vasos sanguíneos, la cicatrización y la inflamación estaban todas más activas en este subtipo. Medidas que estiman la respuesta tumoral a la radiación sugirieron que los gliomas tipo SP son los más resistentes a la radioterapia, coherente con su peor supervivencia. En contraste, los tumores tipo ST parecían más “calmados”, con niveles más bajos de estas características agresivas.
Leer el metabolismo tumoral a partir de resonancias magnéticas
Dado que extraer tejido tumoral mediante cirugía es invasivo y no siempre posible, los investigadores exploraron si la resonancia magnética (RM) convencional podía sugerir el comportamiento lipídico de un tumor. Extraíeron más de dos mil características sutiles de textura y forma de dos secuencias comunes de RM y entrenaron un modelo de aprendizaje automático para distinguir el tipo SP de todos los demás tumores. El modelo funcionó bien tanto en un conjunto de entrenamiento hospitalario como en un conjunto de validación público independiente, separando correctamente los tumores tipo SP con mucha más frecuencia que el azar. Esto sugiere que la huella metabólica de un subtipo de glioma especialmente agresivo deja una señal detectable en exploraciones cerebrales de rutina.
Un gen clave en el centro de una red agresiva
Para pasar de vías amplias a objetivos concretos, el equipo buscó genes centrales en redes relacionadas con lípidos, fuertemente sobreactivos en tumores tipo SP, asociados a peor supervivencia y precisos para distinguir tumores tipo SP de otros. Tres genes —GLA, GLB1 y HSD3B7— cumplieron todos los criterios. Los tres estaban más activos en gliomas tipo SP y juntos formaban una firma diagnóstica potente. Los autores se centraron en HSD3B7, cuyo papel en tumores cerebrales había sido en gran medida inexplorado. Tinciones de tejido de 100 pacientes con glioma mostraron que la proteína HSD3B7 era más alta en tumores más avanzados y más malignos, y los pacientes cuyos tumores presentaban niveles elevados de esta proteína vivieron significativamente menos.
Cómo un gen lipídico remodela el ecosistema tumoral
Análisis a nivel de célula única, que perfilan células individuales dentro de tumores, revelaron que HSD3B7 está activo no solo en células cancerosas sino también en varios tipos de células inmunitarias y de soporte. Niveles altos de este gen se asociaron con una red de señales que promueven el crecimiento de vasos sanguíneos, la inflamación crónica y la evasión inmune. La comunicación entre ciertos tipos celulares protectores pareció debilitada, mientras que bucles autorreforzantes dentro de células que respaldan al tumor se fortalecieron. En conjunto, estos patrones sugieren que la actividad aumentada de HSD3B7 ayuda a crear y mantener un microambiente hostil que favorece el crecimiento tumoral y la resistencia a la terapia.
Qué significa esto para los pacientes y la atención futura
En términos prácticos, este trabajo muestra que los gliomas pueden dividirse de forma significativa en tres subtipos basados en lípidos, con el tipo SP, rico en esfingolípidos, destacando como especialmente peligroso y resistente a las terapias. Estas diferencias no son solo académicas: pueden leerse en RM de rutina mediante análisis avanzado de imágenes y rastrearse hasta genes concretos como HSD3B7, que podrían convertirse en futuros dianas farmacológicas. Aunque aún se necesita trabajo experimental para probar si bloquear estas vías lipídicas podría frenar los tumores o mejorar la radioterapia, el estudio ofrece una nueva lente metabólica para ver el cáncer cerebral y acerca el campo a decisiones terapéuticas más personalizadas e informadas por la biología.
Cita: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
Palabras clave: glioma, metabolismo de lípidos, imagen del tumor cerebral, radiómica, microambiente tumoral