Clear Sky Science · es
Dieta alta en grasas remodela las redes regulatorias de genes en el área preóptica
Por qué tu cerebro importa en la diabetes
La mayoría de la gente piensa en la diabetes como un problema del páncreas y del azúcar en sangre, pero el cerebro también participa de forma importante. Este estudio explora cómo una dieta alta en grasas y un tratamiento experimental potente modifican la actividad génica en una región pequeña pero relevante del cerebro llamada área preóptica. Al cartografiar qué células cerebrales “se reinician” cuando la diabetes entra en remisión, los investigadores esperan señalar rutas para nuevas terapias que aprovechen la capacidad intrínseca del cerebro para ayudar a controlar la glucosa en sangre.
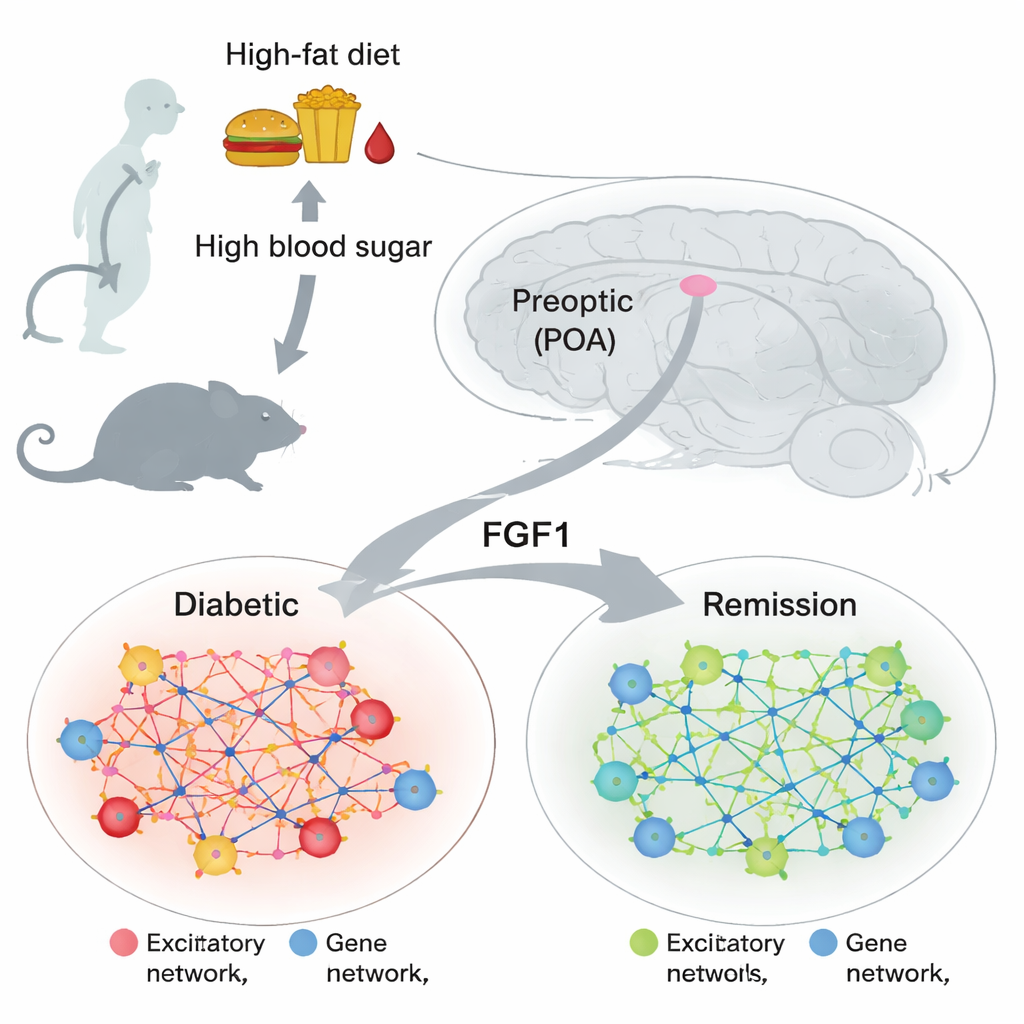
Un pequeño centro cerebral con gran influencia metabólica
El área preóptica se sitúa en la parte anterior del hipotálamo, una región que ayuda a regular la temperatura corporal, el sueño, la alimentación y las señales hormonales. Trabajos previos mostraron que las células en esta región pueden influir en cómo el cuerpo maneja la glucosa y responde al calor, pero su papel en la diabetes no estaba bien comprendido. Al mismo tiempo, otros estudios hallaron que una única dosis de una proteína llamada factor de crecimiento de fibroblastos 1 (FGF1), administrada en el cerebro, puede llevar a ratones obesos diabéticos a una remisión duradera. Esto planteó una cuestión clave: qué células cerebrales y programas génicos cambian cuando la glucemia se normaliza, y si aparecen cambios similares en el área preóptica.
Leer la actividad génica célula por célula
Para responder a esto, el equipo recurrió a la secuenciación de ARN unicelular, una técnica que mide qué genes están activados en miles de células individuales a la vez. Reanalizaron un conjunto de datos existente de ratones cuya diabetes había entrado en remisión tras el tratamiento con FGF1, centrándose en las neuronas del hipotálamo. Con herramientas estadísticas identificaron grupos de genes que aumentaban o disminuían de forma coordinada cuando los animales pasaban de un estado diabético a la remisión. Estos “módulos de remisión” actúan como huellas digitales de la recuperación: en lugar de seguir un gen a la vez, capturan cambios coordinados en muchos genes dentro de tipos neuronales concretos.
Dieta alta en grasas, células cerebrales y menor consumo energético
Los investigadores compararon después estos módulos de remisión con la actividad génica en otro conjunto de datos que muestreó células del área preóptica de ratones normales. Primero separaron las neuronas en dos clases amplias: células excitatorias, que tienden a aumentar la actividad en sus circuitos, y células inhibitorias, que la atenúan. En los ratones diabéticos tratados con FGF1, ambos tipos neuronales mostraron reducciones generalizadas en genes vinculados a la producción de energía, especialmente aquellos implicados en la fosforilación oxidativa, la respiración celular y la maquinaria mitocondrial que alimenta a las células activas. En las neuronas excitatorias, un gran módulo génico “turquesa” asociado al uso de energía y a la actividad sináptica se atenuó notablemente en la remisión, lo que sugiere que estas células se vuelven menos exigentes metabólicamente cuando la glucosa en sangre se controla.
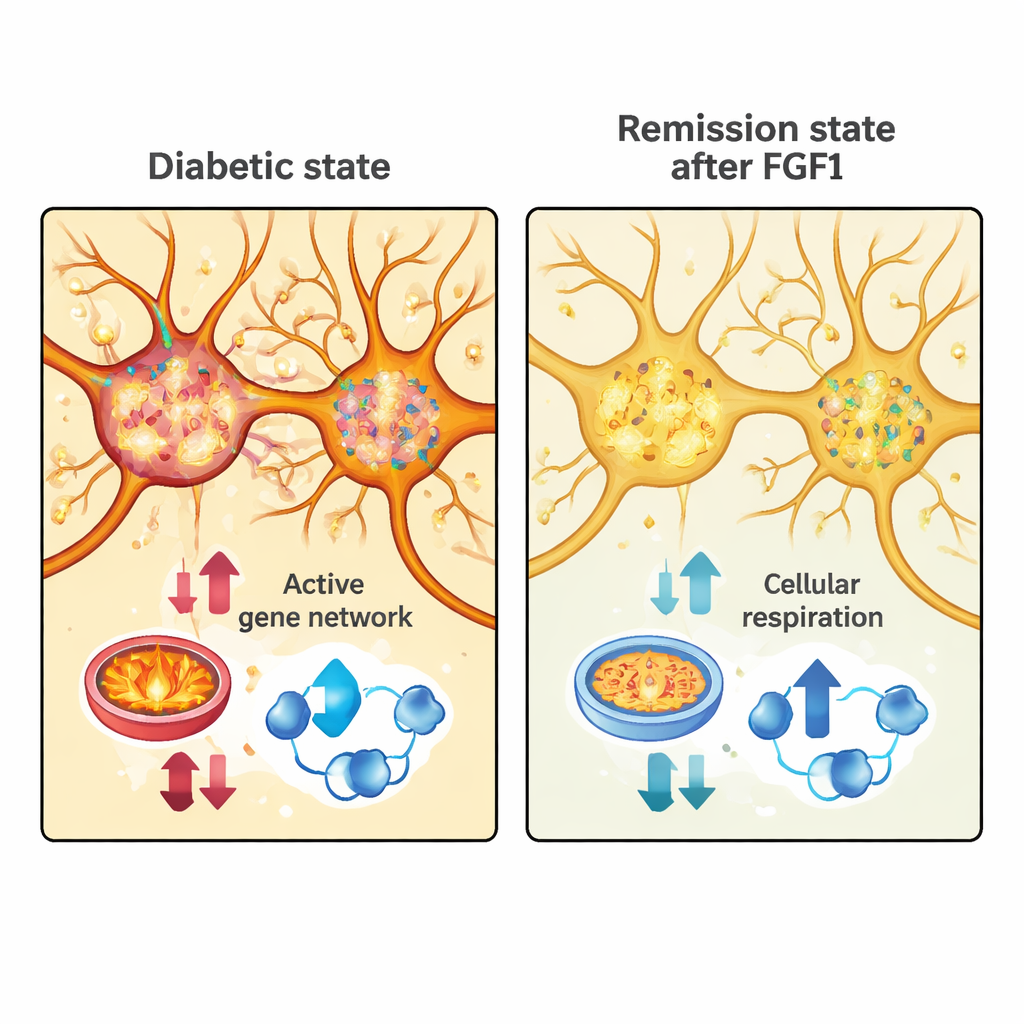
Rastrear las firmas de remisión hasta grupos neuronales concretos
A continuación, el equipo preguntó si estos patrones génicos relacionados con la remisión coincidían con poblaciones celulares particulares en el área preóptica. Al fusionar computacionalmente los dos conjuntos de datos, encontraron que algunos clústeres neuronales preópticos expresaban muchos de los mismos genes que cambiaron con la remisión inducida por FGF1. Señalaron varios genes —como Trpc4, Dgkg y Ryr3— que ocupaban el cruce de estos análisis. Empleando un método de microscopía muy sensible llamado RNAscope, demostraron que estos genes se expresan efectivamente en zonas diferenciadas del área preóptica del ratón, mayormente en subregiones dorsales. Esto los valida como marcadores reales de grupos neuronales concretos que pueden participar en la respuesta cerebral a la enfermedad metabólica.
Qué significa esto para futuros tratamientos de la diabetes
Para el público no especializado, la conclusión es que la diabetes no es solo un problema de azúcar en sangre: también es un problema de redes cerebrales. El estudio muestra que cuando la diabetes entra en remisión en ratones, ciertas neuronas preópticas pasan a un estado de menor demanda energética y cambian su actividad génica de forma coordinada. Al definir estos módulos de remisión y vincularlos a tipos celulares y genes marcadores concretos, el trabajo ofrece una hoja de ruta para experimentos futuros: los investigadores pueden ahora dirigir estas neuronas específicas para probar cómo influyen en el control de la glucosa, la obesidad y las complicaciones asociadas. A largo plazo, una mejor comprensión de estos circuitos cerebrales podría ayudar a inspirar tratamientos que complementen o incluso sustituyan a órganos fallidos del cuerpo aprovechando el control inherente del cerebro sobre el metabolismo.
Cita: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Palabras clave: cerebro y diabetes, área preóptica, dieta alta en grasas, redes génicas, remisión por FGF1