Clear Sky Science · es
Identificación en todo el transcriptoma de variantes deletéreas en genes candidatos vinculados a la paratuberculosis bovina
Genes ocultos tras una costosa enfermedad bovina
La paratuberculosis bovina, también conocida como enfermedad de Johne, debilita discretamente la salud y la productividad de los hatos lecheros de todo el mundo, costando a los ganaderos cientos de millones de dólares cada año y suscitando preocupación por posibles vínculos con trastornos intestinales humanos. Este estudio examina el “capó” genético de vacas Holstein para plantear una pregunta simple pero crucial: ¿qué diferencias en sus genes podrían ayudar a algunos animales a resistir esta infección mientras otros sucumben? Al leer el ARN —las copias activas de los genes— en sangre y tejido intestinal, los investigadores trazaron cómo cambios sutiles en el ADN de genes inmunitarios clave pueden orientar el curso de la enfermedad.
Por qué importa esta enfermedad bovina
La paratuberculosis la provoca la bacteria Mycobacterium avium subespecie paratuberculosis (MAP). Las vacas suelen infectarse temprano en la vida, pero los signos clínicos aparecen a menudo años después. En las etapas silenciosas y subclínicas, los animales parecen sanos pero pueden eliminar bajas cantidades de la bacteria y producir menos leche. En las fases clínicas desarrollan diarrea crónica, pérdida de peso severa y caídas importantes en la producción de leche. Las tasas de infección a nivel de rebaño pueden superar el 50 % en muchas regiones, incluidas partes de Europa y Norteamérica, creando un problema económico y de bienestar animal. Dado que la bacteria también podría actuar como disparador ambiental de enfermedades inflamatorias humanas como la enfermedad de Crohn, existe una presión creciente para mejorar las estrategias de control en el ganado.
Leer el genoma en funcionamiento
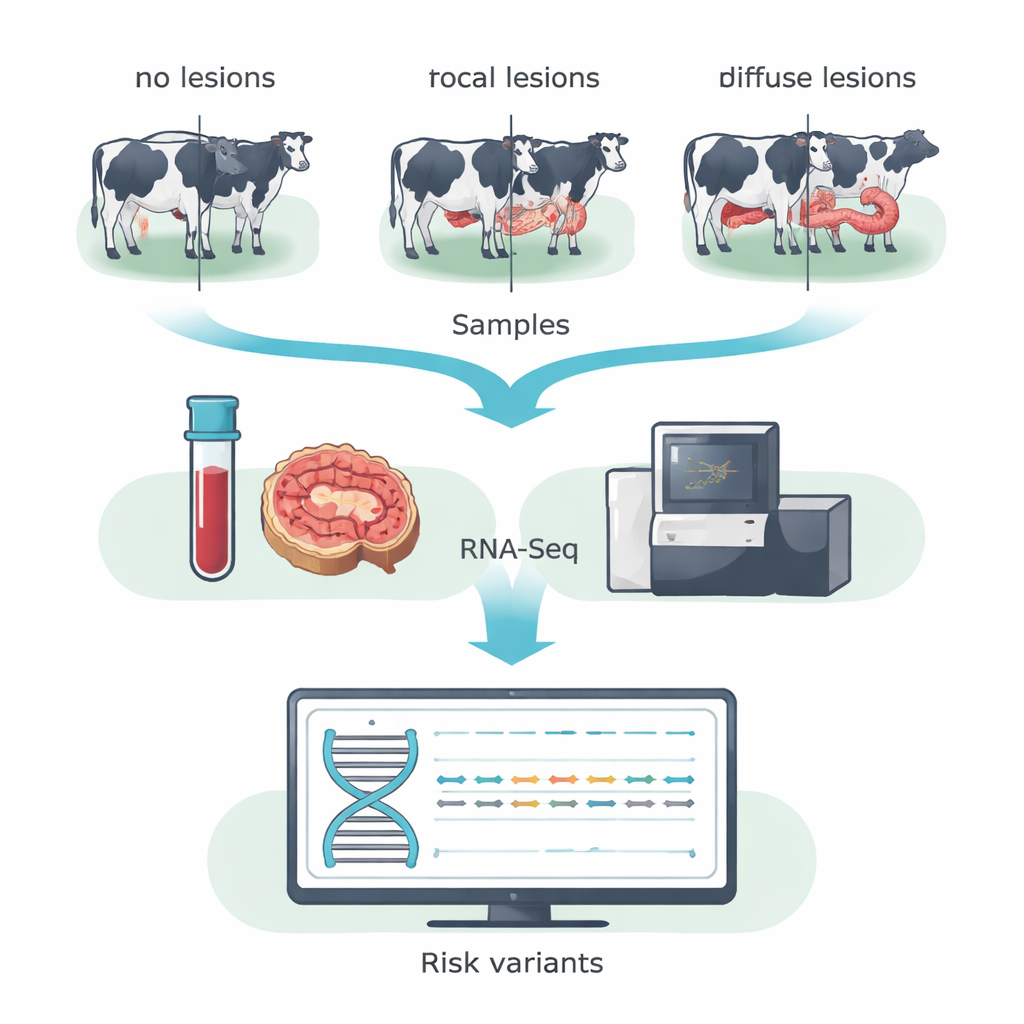
En lugar de escanear la secuencia completa del ADN, el equipo usó la secuenciación de ARN (RNA-Seq) para centrarse en los genes que están realmente activos en el animal. Recolectaron sangre y muestras de la válvula ileocecal —una región intestinal altamente afectada por MAP— de 14 vacas Holstein en un rebaño lechero español. En base al examen microscópico de los tejidos intestinales, las vacas se agruparon en tres categorías: animales sin lesiones detectables, animales con lesiones pequeñas y localizadas (focales) típicas de una infección subclínica prolongada, y animales con lesiones severas y generalizadas (difusas) asociadas a enfermedad clínica. Al fusionar los datos de sangre e intestino dentro de cada grupo, los investigadores aumentaron su capacidad para detectar cambios de una sola letra en el ADN de genes expresados, conocidos como SNPs codificantes.
Encontrar cambios nocivos en genes inmunitarios clave
De cientos de miles de variantes, el equipo se centró en aquellas que alteran la secuencia proteica y se predice que dañan la función de la proteína —las llamadas variantes deletéreas. Aplicaron filtros estrictos para garantizar alta confianza y luego usaron herramientas de predicción establecidas para marcar cambios riesgosos. Este proceso de depuración reveló 31 variantes de este tipo únicas en vacas sin lesiones, 15 únicas en vacas con lesiones focales y 31 únicas en vacas con lesiones difusas. Muchas de estas recayeron en genes que guían cómo las células inmunitarias reconocen y eliminan infecciones, regulan la muerte celular y gestionan el metabolismo. Destacó la familia de genes BOLA, la versión bovina del complejo mayor de histocompatibilidad clase II, que ayuda a las células inmunitarias a presentar fragmentos bacterianos a los linfocitos T. Se hallaron diferentes variantes potencialmente dañinas en BOLA en los tres grupos de vacas, lo que sugiere que versiones específicas de BOLA pueden inclinar a los animales hacia la resistencia, el control de la infección o la inflamación dañina.
De variantes del ADN a rutas de enfermedad
Para entender qué podrían significar esos cambios genéticos en la práctica, los investigadores examinaron qué rutas biológicas estaban enriquecidas en cada grupo. Las vacas sin lesiones mostraron variantes alteradas en genes vinculados al procesamiento de antígenos, el tráfico de vesículas y el equilibrio inmunitario intestinal, incluidos BOLA, AP3B1 y CHGA. Estos cambios podrían favorecer una digestión eficiente de bacterias dentro de las células inmunitarias y un entorno intestinal estable que limite el daño. En las vacas con lesiones focales, las variantes dañinas se agruparon en genes (ORMDL3 y KANK2) que atenúan la muerte celular programada y ajustan el metabolismo celular, lo que potencialmente ayuda al huésped a mantener bajos los números bacterianos durante una larga fase subclínica. En las vacas con lesiones difusas, los genes afectados apuntaron a vías inmunitarias sobreactivadas como la diferenciación de células Th1/Th2 y la presentación de antígenos, junto con rutas de transporte de bilis y respuesta a fármacos. Aquí, genes alterados de la familia BOLA podrían impulsar una reacción inflamatoria fuerte y a veces autodañina, reflejando patrones observados en muchas enfermedades autoinmunes e inflamatorias humanas.
Pistas para criar hatos más resistentes
Además de aclarar cómo diferentes variantes genéticas moldean la respuesta inmune a MAP, el estudio también vinculó estos cambios riesgosos con regiones conocidas del genoma bovino asociadas a rasgos de salud, incluida la susceptibilidad a la paratuberculosis y otras infecciones. Aunque estos resultados aún requieren validación en hatos más grandes y no pueden usarse todavía como marcadores diagnósticos independientes, ofrecen un catálogo prometedor de variantes y genes candidatos. Dicho de forma simple, el trabajo sugiere que algunas vacas llevan versiones génicas que las ayudan a controlar la infección silenciosamente, mientras que otras llevan versiones que favorecen la inflamación descontrolada y la enfermedad severa. En el futuro, esta información podría respaldar programas de cría selectiva y pruebas genéticas que orienten los hatos hacia una mayor resistencia natural, reduciendo tanto las pérdidas económicas como la necesidad de medidas intensivas de control de la enfermedad.
Cita: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Palabras clave: paratuberculosis bovina, genética de la enfermedad de Johne, inmunidad en vacas lecheras, secuenciación de ARN, crianza para resistencia a enfermedades